解答题-工业流程题 较难0.4 引用2 组卷879
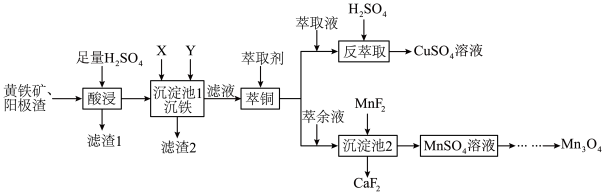
电解金属锰阳极渣(主要成分MnO2,杂质为PbCO3、Fe2O3、CuO)和黄铁矿(FeS2)为原料可制备Mn3O4,其流程如图所示:
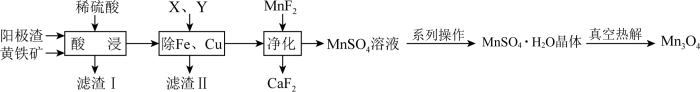
已知:部分阳离子以氢氧化物形式完全沉淀时的pH如下:Fe3+ 3.7,Fe2+ 9.7,Cu2+ 7.4,Mn2+ 9.8
回答下列问题:
(1)“酸浸”过程中,滤渣Ⅰ的主要成分为S、______ (填化学式)。
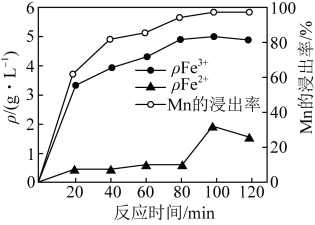
(2)“酸浸”过程中Fe2+、Fe3+的质量浓度、Mn浸出率与时间的关系如图1所示。
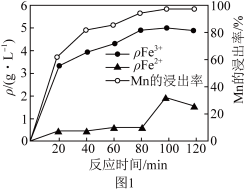
20~80min,浸出Mn元素的主要离子方程式为______ 。80~100min时,Fe2+浓度上升的原因可能是______ 。
(3)“除Fe、Cu”过程中依次加入的试剂X、Y为______ (填序号)。
A.NH3•H2O、H2O2 B.H2O2、CaCO3 C.SO2、MnCO3
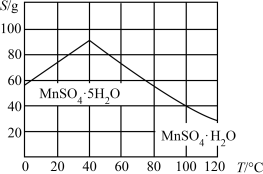
(4)硫酸锰晶体的溶解度曲线如图2,由MnSO4溶液获得MnSO4•H2O晶体的系列操作为______ 、洗涤、干燥。
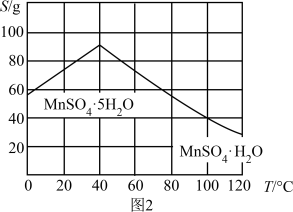
(5)“真空热解”过程中,测得固体的质量随温度变化如图3所示。需控制的温度为______ 。
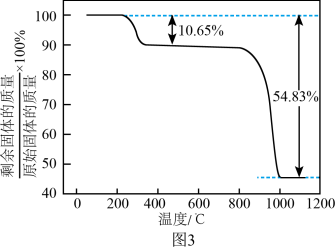
(6)由MnSO4溶液制取Mn3O4的另一种方案是:向MnSO4溶液中加入氨水,产生Mn(OH)2沉淀和少量Mn2(OH)2SO4,滤出,洗净,加水打成浆,浆液边加热边持续通空气,制得Mn3O4。沉淀加热通空气过程中,7小时之前,溶液的pH=6,7小时之后迅速下降,原因是______ 。

已知:部分阳离子以氢氧化物形式完全沉淀时的pH如下:Fe3+ 3.7,Fe2+ 9.7,Cu2+ 7.4,Mn2+ 9.8
回答下列问题:
(1)“酸浸”过程中,滤渣Ⅰ的主要成分为S、
(2)“酸浸”过程中Fe2+、Fe3+的质量浓度、Mn浸出率与时间的关系如图1所示。

20~80min,浸出Mn元素的主要离子方程式为
(3)“除Fe、Cu”过程中依次加入的试剂X、Y为
A.NH3•H2O、H2O2 B.H2O2、CaCO3 C.SO2、MnCO3
(4)硫酸锰晶体的溶解度曲线如图2,由MnSO4溶液获得MnSO4•H2O晶体的系列操作为

(5)“真空热解”过程中,测得固体的质量随温度变化如图3所示。需控制的温度为

(6)由MnSO4溶液制取Mn3O4的另一种方案是:向MnSO4溶液中加入氨水,产生Mn(OH)2沉淀和少量Mn2(OH)2SO4,滤出,洗净,加水打成浆,浆液边加热边持续通空气,制得Mn3O4。沉淀加热通空气过程中,7小时之前,溶液的pH=6,7小时之后迅速下降,原因是
2023·山东泰安·二模
类题推荐  可用于电子工业生产软磁铁氧体,工业上常以电解金属锰阳极渣(主要成分
可用于电子工业生产软磁铁氧体,工业上常以电解金属锰阳极渣(主要成分 ,杂质为
,杂质为 )和黄铁矿
)和黄铁矿 为原料制备
为原料制备 其流程如图。
其流程如图。
回答下列问题:
(1) 的价层电子排布图
的价层电子排布图_______ ,“酸浸”过程中,滤渣1的主要成分为S、_______ (填化学式)。
(2)“酸浸”过程中 、
、 的质量浓度、Mn的浸出率与时间的关系如图所示。
的质量浓度、Mn的浸出率与时间的关系如图所示。_______ 。
②80~100min时, 浓度上升的原因可能是
浓度上升的原因可能是_______ 。
(3)“沉铁”过程中依次加入的试剂X、Y为_______ (填字母)。
A. B.
B. C.
C.
(4)“滤液”萃取前调 ,若有机萃取剂用表HR示,则发生萃取的反应可表示为
,若有机萃取剂用表HR示,则发生萃取的反应可表示为 。若,
。若, 多次萃取后水相中
多次萃取后水相中 为
为 ,则铜的萃取率为
,则铜的萃取率为_______ (结果保留小数点后一位,溶液体积变化忽略不计)。
(5)利用 溶液,用空气氧化法制备
溶液,用空气氧化法制备 。在
。在 溶液中滴入一定浓度的氨水,加压通氧气反应7小时制备
溶液中滴入一定浓度的氨水,加压通氧气反应7小时制备 。写出上述反应的离子方程式:
。写出上述反应的离子方程式:_______ 。
(6)结合图像分析,若要获得 晶体的系列操作步骤为加热
晶体的系列操作步骤为加热_______ 得到_______ ℃饱和溶液,_______ ,过滤酒精洗涤,低温干燥。
| 完全沉淀时的pH | 3.7 | 9.7 | 7.4 | 9.8 |
(1)
(2)“酸浸”过程中
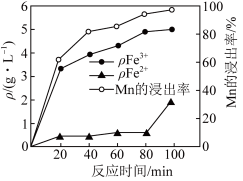
②80~100min时,
(3)“沉铁”过程中依次加入的试剂X、Y为
A.
(4)“滤液”萃取前调
(5)利用
(6)结合图像分析,若要获得
电解金属锰阳极渣(主要成分MnO2,杂质为PbCO3、Fe2O3、CuO)和黄铁矿(FeS2)为原料可制备Mn3O4,其流程如图所示:
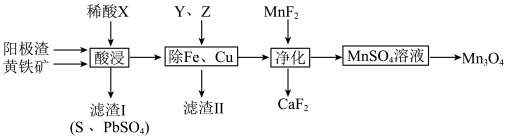
已知:室温下CaF2和MnF2均难溶于水且前者的溶解度更小。回答下列问题:
(1)基态Mn原子的价电子的轨道表示式为___________ 。
(2)“酸浸”过程中,所用的稀酸X是___________ (填化学式)。
(3)“酸浸”过程中
 的质量浓度、Mn浸出率与时间的关系如图所示。20~80min,浸出Mn元素的主要离子方程式为
的质量浓度、Mn浸出率与时间的关系如图所示。20~80min,浸出Mn元素的主要离子方程式为___________ 。80~100min时,
 浓度上升的原因可能是
浓度上升的原因可能是___________ 。
(4)“除Fe、Cu”过程中依次加入的试剂Y、Z为___________(填序号)。
(5)“净化”中加入MnF2的目的是除去
 ,其反应的离子方程式为
,其反应的离子方程式为___________ 。
(6)硫酸锰在空气中加热可以生产相应的氧化物,称取151mg硫酸锰充分煅烧后刷余固体的质量为79mg,则此时固体的化学式为___________ 。下图为不同温度下硫酸锰隔绝空气焙烧2小时后残留固体的X-射线衍射图,若由MnSO4固体制取活性Mn2O3方案为:将MnSO4固体置于可控温度的反应管中,___________ ,将
 冷却、研磨、密封包装。(可选用的试剂有:
冷却、研磨、密封包装。(可选用的试剂有:
 溶液,1mol/LNaOH溶液)
溶液,1mol/LNaOH溶液)


已知:室温下CaF2和MnF2均难溶于水且前者的溶解度更小。回答下列问题:
(1)基态Mn原子的价电子的轨道表示式为
(2)“酸浸”过程中,所用的稀酸X是
(3)“酸浸”过程中

(4)“除Fe、Cu”过程中依次加入的试剂Y、Z为___________(填序号)。
| A. | B. | C. | D. |
(5)“净化”中加入MnF2的目的是除去
(6)硫酸锰在空气中加热可以生产相应的氧化物,称取151mg硫酸锰充分煅烧后刷余固体的质量为79mg,则此时固体的化学式为

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网





