解答题-实验探究题 较难0.4 引用1 组卷376
I.硫铁矿(主要成分为FeS2杂质为Al2O3、SiO2)是重要的矿产资源,以硫铁矿为原料制备绿矾(FeSO4•7H2O)的工艺流程如图:
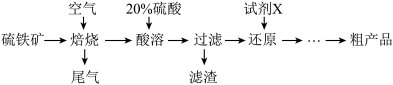
(1)硫铁矿中S元素的价态为______ ,滤渣的成分为______ 。
(2)还原步骤中,加入的试剂X的化学式为______ 。
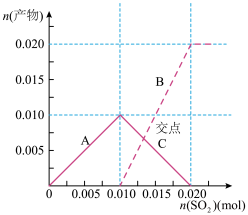
(3)实验室中可用NaOH溶液回收将SO2气体通入到0.100mol•L-1200mLNaOH溶液中,溶液中含硫元素的离子的物质的量与SO2的通入量的关系如图:实线A是______ 的变化曲线,虚线B是______ 的变化曲线(填离子符号)交点C处发生反应的离子方程式为_______ 。
II.硫酸亚铁(FeSO4)加热至高温会分解,生成一种金属氧化物和两种非金属氧化物。

组装好仪器(已省略夹持仪器),在一定温度下按上述图示装置进行实验。
(4)组装好实验装置后,要进行的下一步操作是______ ;实验开始时通入氮气的目的是______ 。
(5)B中实验现象证明分解产物中含有______ (写化学式)。依据实验2硬质玻璃管中加热冷却后的固体性质确定分解产物有______ (写化学式)。
(6)某同学欲通过下列实验验证分解产物中含有的另一种非金属氧化物。
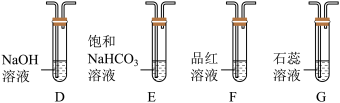
①从实验装置D、E、F、G中,选用两个装置与装置A连接进行实验,依次连接的合理顺序为A→______
②能证明生成了另一种非金属氧化物的现象是______ 。该现象体现了该物质的______ 性。写出该条件下硫酸亚铁受热分解的化学方程式______ 。

(1)硫铁矿中S元素的价态为
(2)还原步骤中,加入的试剂X的化学式为
(3)实验室中可用NaOH溶液回收将SO2气体通入到0.100mol•L-1200mLNaOH溶液中,溶液中含硫元素的离子的物质的量与SO2的通入量的关系如图:实线A是

II.硫酸亚铁(FeSO4)加热至高温会分解,生成一种金属氧化物和两种非金属氧化物。

组装好仪器(已省略夹持仪器),在一定温度下按上述图示装置进行实验。
| 序号 | 操作步骤 | 实验现象 |
| 1 | 打开K,通入一段时间的N2,关闭活塞K,加热A中的玻璃管一段时间 | B中产生大量白色沉淀 |
| 2 | A中固体不再分解后,停止加热,打开K,缓慢通入氮气至玻璃管冷却 | 硬质玻璃管中最终可以看到红棕色固体物质 |
(5)B中实验现象证明分解产物中含有
(6)某同学欲通过下列实验验证分解产物中含有的另一种非金属氧化物。

①从实验装置D、E、F、G中,选用两个装置与装置A连接进行实验,依次连接的合理顺序为A→
②能证明生成了另一种非金属氧化物的现象是
22-23高一下·广东广州·期中
类题推荐
硫酸亚铁(FeSO4)加热至高温会分解,生成Fe2O3和非金属氧化物。
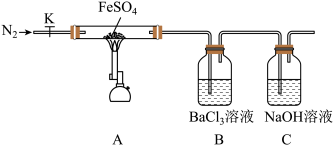
(1)按图组装好仪器(已省略夹持仪器)并检查装置的气密性,在一定温度下按上述图示装置进行实验。
①实验开始时通入氮气的目的是_______ 。
②B中现象证明分解产物中含有_______ (写化学式)。
(2)某同学欲验证分解产物中含有的另一种非金属氧化物。

①从实验装置D、E、F、G中,选用两个装置与装置A连接进行实验,依次连接的合理顺序为A →_______ →_______ 。
②能证明生成了另一种非金属氧化物的现象是_______ 。
(3)写出该条件下硫酸亚铁受热分解的化学方程式_______ 。

(1)按图组装好仪器(已省略夹持仪器)并检查装置的气密性,在一定温度下按上述图示装置进行实验。
| 操作步骤 | 实验现象 |
| 打开K,通入一段时间的N2,关闭活塞K,加热A中的玻璃管一段时间 | B中产生大量白色沉淀 |
| A中固体不再分解后,停止加热,打开K,缓慢通入氮气至玻璃管冷却 | 硬质玻璃管中最终可以看到红棕色固体 |
②B中现象证明分解产物中含有
(2)某同学欲验证分解产物中含有的另一种非金属氧化物。

①从实验装置D、E、F、G中,选用两个装置与装置A连接进行实验,依次连接的合理顺序为A →
②能证明生成了另一种非金属氧化物的现象是
(3)写出该条件下硫酸亚铁受热分解的化学方程式
硫酸亚铁(FeSO4)加热至高温会分解,生成一种金属氧化物M和两种非金属氧化
物。某化学研究小组利用下列装置加热至高温使FeSO4分解。

实验步骤:
将一定量FeSO4固体置于硬质玻璃管中,打开活塞K,通入一段时间N2,关闭活塞K。加热A中的玻璃管一段时间,待A中固体不再分解后,停止加热,打开K,缓慢通入氮气至玻璃管冷却。
(1)已知M中铁元素的质量分数为70%,M的化学式为__________ 。
(2)按图组装好仪器(已省略夹持仪器)并检查装置的气密性,在一定温度下按上述图示装置进行实验。
(3)某同学欲验证硫酸亚铁分解产物中含有的另一种非金属氧化物N。
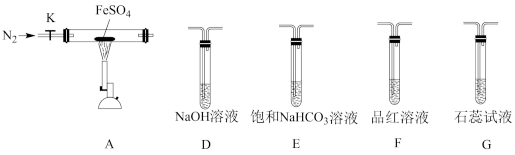
①从实验装置D、E、F、G中,选用两个装置与装置A连接进行实验,依次连接的合理顺序为A →________ →________ 。
②能证明生成了非金属氧化物N的现象是______ 。
物。某化学研究小组利用下列装置加热至高温使FeSO4分解。

实验步骤:
将一定量FeSO4固体置于硬质玻璃管中,打开活塞K,通入一段时间N2,关闭活塞K。加热A中的玻璃管一段时间,待A中固体不再分解后,停止加热,打开K,缓慢通入氮气至玻璃管冷却。
(1)已知M中铁元素的质量分数为70%,M的化学式为
(2)按图组装好仪器(已省略夹持仪器)并检查装置的气密性,在一定温度下按上述图示装置进行实验。
| 操作步骤 | 实验现象 | 用化学方程式解释原因 |
| 打开K,通入一段时间的氮气,关闭活塞K,加热A中的玻璃管一段时间 | 洗气瓶B中 | |
| A中固体不在分解后,停止加热,打开K,缓慢通入氮气至玻璃管冷却 | 硬质玻璃管中最终可以看到 |

①从实验装置D、E、F、G中,选用两个装置与装置A连接进行实验,依次连接的合理顺序为A →
②能证明生成了非金属氧化物N的现象是
硫酸亚铁加热至高温会分解,生成—种金属氧化物M和两种非金属氧化物。某化学研究小组利用下列装置加热至高温使FeSO4分解。

实验步骤:
将一定量FeSO4固体置于硬质玻璃管中,打开活塞K,通入一段时间N2,关闭活塞K。加热A中的玻璃管一段时间,待A中固体不再分解后,停止加热,打开K,缓慢通入氮气至玻璃管冷却。
(1)已知M中铁元素的质量分数为70%,M的化学式为_____________ 。
(2)按图组装好仪器(已省略夹持仪器)并检查装置的气密性,在一定温度下按上述图示装置进行实验。
(3)某同学欲验证硫酸亚铁分解产物中含有的另一种非金属氧化物N。

①从实验装置D、E、F、G中,选用两个装置与装置A连接进行实验,依次连接的合理顺序为A→______ →______ 。
②能证明生成了非金属氧化物N的现象是________________ 。

实验步骤:
将一定量FeSO4固体置于硬质玻璃管中,打开活塞K,通入一段时间N2,关闭活塞K。加热A中的玻璃管一段时间,待A中固体不再分解后,停止加热,打开K,缓慢通入氮气至玻璃管冷却。
(1)已知M中铁元素的质量分数为70%,M的化学式为
(2)按图组装好仪器(已省略夹持仪器)并检查装置的气密性,在一定温度下按上述图示装置进行实验。
| 操作步骤 | 实验现象 | 用方程式解释原因 |
| 打开K,通入一段时间N2,关闭K。加热A中玻璃管一段时间 | 洗气瓶B中① | ② |
| A中固体不再分解后,停止加热,打开K,缓慢通入N2至玻璃管冷却 | 硬质玻璃管最终可以看到③ | ④ |

①从实验装置D、E、F、G中,选用两个装置与装置A连接进行实验,依次连接的合理顺序为A→
②能证明生成了非金属氧化物N的现象是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


