解答题-工业流程题 较易0.85 引用1 组卷163
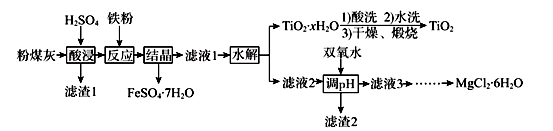
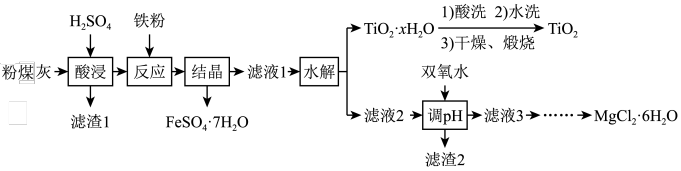
某火电厂收捕到的粉煤灰的主要成分为SiO2、Al2O3、FeO、Fe2O3、MgO、TiO2等。研究小组对其进行综合处理的流程如下:
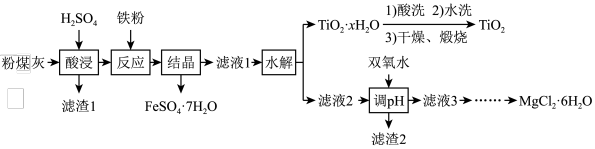
已知:①“酸浸”后钛主要以TiOSO4形式存在,强电解质TiOSO4在溶液中仅能电离SO 和一种阳离子。
和一种阳离子。
②常温下,Ksp[Al(OH)3]=8.0×10−35,Ksp[Fe(OH)3]=4.0×10−38,Ksp[Mg(OH)2]=5.61×10−12。
③滤液1中仍有Fe2+剩余
(1)为了提高粉煤灰浸出速率,在“酸浸”时可采取的措施有___________ (任写一种)。
(2)钛元素发生“水解”反应的离子方程式为___________ 。
(3)加入双氧水的目的是___________ 。滤渣2中的成分分别为Al(OH)3和___________ ,Al(OH)3沉淀完全时(溶液中离子浓度小于10−5mol/L),溶液中的c(OH−)为___________ 。
(4)将MgCl2·6H2O制成无水MgCl2时应注意___________ 。
(5)某同学以石墨为两个电极,电解MgCl2溶液以制取金属镁。你认为他能否获得成功?并用化学方程式解释原因___________ 。

已知:①“酸浸”后钛主要以TiOSO4形式存在,强电解质TiOSO4在溶液中仅能电离SO
②常温下,Ksp[Al(OH)3]=8.0×10−35,Ksp[Fe(OH)3]=4.0×10−38,Ksp[Mg(OH)2]=5.61×10−12。
③滤液1中仍有Fe2+剩余
(1)为了提高粉煤灰浸出速率,在“酸浸”时可采取的措施有
(2)钛元素发生“水解”反应的离子方程式为
(3)加入双氧水的目的是
(4)将MgCl2·6H2O制成无水MgCl2时应注意
(5)某同学以石墨为两个电极,电解MgCl2溶液以制取金属镁。你认为他能否获得成功?并用化学方程式解释原因
22-23高二下·广西梧州·阶段练习
类题推荐
粉煤灰的主要成分为SiO2、Al2O3、FeO、Fe2O3、MgO、TiO2等,研究小组对其进行综合处理的流程如图:

已知:
①“酸浸”后钛主要以TiOSO4形式存在,在溶液中完全电离出SO 和一种可水解的阳离子。
和一种可水解的阳离子。
②当离子浓度小于等于1.0×10-5 mol·L-1时,可认为其已沉淀完全。
③Ksp[Al(OH)3]=1.0×10-34、Ksp[Fe(OH)3]=4.0×10-38。
下列说法错误的是

已知:
①“酸浸”后钛主要以TiOSO4形式存在,在溶液中完全电离出SO
②当离子浓度小于等于1.0×10-5 mol·L-1时,可认为其已沉淀完全。
③Ksp[Al(OH)3]=1.0×10-34、Ksp[Fe(OH)3]=4.0×10-38。
下列说法错误的是
| A.“酸浸”时TiO2发生反应的离子方程式为TiO2+2H+=TiO2++H2O |
| B.“结晶”时应控制适宜温度,温度过高TiO2·xH2O产率降低 |
| C.“调pH”时温度越高,氧化速率越快 |
| D.为使“滤液2”中杂质离子沉淀完全,pH的理论最小值为4.3 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网