填空题 适中0.65 引用1 组卷155
金属钛(Ti)在航空航天、医疗器械等工业领域有着重要用途。目前生产钛的方法之一是将金红石(TiO2)转化为TiCl4,再进一步还原得到钛。回答下列问题:
(1)TiO2转化为TiCl4有直接氯化法和碳氯化法。在1000℃时反应的热化学方程式及其平衡常数如下:
(i)直接氯化:TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g) △H1=+172kJ•mol-1,Kp1=1.0×10-2
(ii)碳氯化:TiO2(s)+2Cl2(g)+2C(s)=TiCl4(g)+2CO(g) △H2=-51kJ•mol-1,Kp2=1.2×1012Pa
①对于直接氯化反应:增大压强,平衡______ 移动(填“向左”“向右”或“不”);温度升高,平衡转化率______ (填“变大”“变小”或“不变”)。
②直接氯化的反应趋势远小于碳氯化,其原因是______ 。
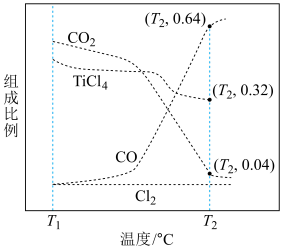
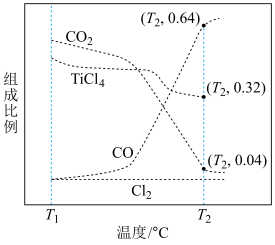
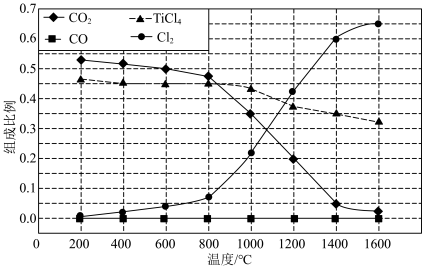
(2)在1.0×105Pa,将TiO2、C、Cl2按物质的量比1∶2.2∶2进行反应。体系中气体平衡组成比例(物质的量分数)随温度变化的理论计算结果如图所示。
①反应 C(s)+
C(s)+ CO2(g)
CO2(g) CO(g)的平衡常数Kp(1400℃)=
CO(g)的平衡常数Kp(1400℃)=______ Pa( ≈8.5)。
≈8.5)。
②图中显示,在200℃平衡时TiO2几乎完全转化为TiCl4,但实际生产中反应温度却远高于此温度,其原因是______ 。
(3)TiO2直接氯化和碳氯化都属于“气—固”反应,工业生产中有利于“气—固”充分接触的措施是______ 。
(1)TiO2转化为TiCl4有直接氯化法和碳氯化法。在1000℃时反应的热化学方程式及其平衡常数如下:
(i)直接氯化:TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g) △H1=+172kJ•mol-1,Kp1=1.0×10-2
(ii)碳氯化:TiO2(s)+2Cl2(g)+2C(s)=TiCl4(g)+2CO(g) △H2=-51kJ•mol-1,Kp2=1.2×1012Pa
①对于直接氯化反应:增大压强,平衡
②直接氯化的反应趋势远小于碳氯化,其原因是
(2)在1.0×105Pa,将TiO2、C、Cl2按物质的量比1∶2.2∶2进行反应。体系中气体平衡组成比例(物质的量分数)随温度变化的理论计算结果如图所示。

①反应
②图中显示,在200℃平衡时TiO2几乎完全转化为TiCl4,但实际生产中反应温度却远高于此温度,其原因是
(3)TiO2直接氯化和碳氯化都属于“气—固”反应,工业生产中有利于“气—固”充分接触的措施是
22-23高二上·河南驻马店·期末
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网