解答题-工业流程题 困难0.15 引用1 组卷573
实验室从某废弃炉渣(含Cu、Ni、Co、Ca、Fe等金属及其氧化物)中回收Cu、Ni、Co,其部分实验过程如下:
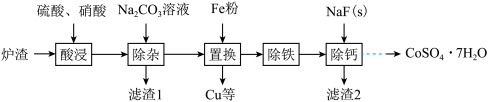
(1)除杂。该步骤所用玻璃仪器有烧杯、___________ 。
(2)除铁。将“置换”后溶液中的 氧化为
氧化为 ,控制pH可形成
,控制pH可形成 沉淀。写出该反应的离子方程式:
沉淀。写出该反应的离子方程式:_____________________ 。
(3)除钙。向“除铁”后的滤液中加入NaF,使 转化为
转化为 沉淀除去。若溶液pH偏低,将会导致
沉淀除去。若溶液pH偏低,将会导致 沉淀不完全,其原因是
沉淀不完全,其原因是____________ 。[ 、
、 ]。
]。
(4)除钙后的溶液经过萃取、反萃取等操作可分离钴和镍.其中萃取原理可表示为
①与萃取剂Cyanex272(磷酸酯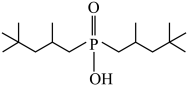 )相比,芳香基磷酸酯更适合高酸度废水中
)相比,芳香基磷酸酯更适合高酸度废水中 的萃取,原因是
的萃取,原因是______ 。
②设计以“除钙”后的混合溶液(含 、
、 、
、 溶液)为原料,制备
溶液)为原料,制备 的实验方案:
的实验方案:__________ (已知 、
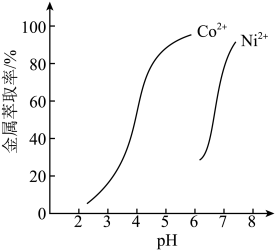
、 的萃取率-pH的关系曲线如图所示。实验中须使用的试剂有:Cyanex272、
的萃取率-pH的关系曲线如图所示。实验中须使用的试剂有:Cyanex272、 溶液、NaOH溶液)。
溶液、NaOH溶液)。

(1)除杂。该步骤所用玻璃仪器有烧杯、
(2)除铁。将“置换”后溶液中的
(3)除钙。向“除铁”后的滤液中加入NaF,使
(4)除钙后的溶液经过萃取、反萃取等操作可分离钴和镍.其中萃取原理可表示为
①与萃取剂Cyanex272(磷酸酯
 )相比,芳香基磷酸酯更适合高酸度废水中
)相比,芳香基磷酸酯更适合高酸度废水中②设计以“除钙”后的混合溶液(含

22-23高三下·江苏·阶段练习
类题推荐  是一种蓝色易溶于水的细粒结晶,主要用于电镀、医药、以及印染工业等。以一种含镍废液(主要成分是
是一种蓝色易溶于水的细粒结晶,主要用于电镀、医药、以及印染工业等。以一种含镍废液(主要成分是 和
和 ,还含有少量
,还含有少量 、
、 、
、 )为原料制取
)为原料制取 的过程如下:
的过程如下:

已知不同金属离子生成氢氧化物沉淀所需的pH如下表。
(1)“氧化”时,主要发生反应的离子方程式为___________ 。
(2)加入NiO能除去Fe、Cu的原因为___________ ,应调节溶液pH的范围为___________ 。
(3)向“除Fe、Cu”后的滤液中加入NaF溶液,使 转化为
转化为 沉淀除去。
沉淀除去。
①若溶液pH偏低,将会导致 沉淀不完全,其原因是
沉淀不完全,其原因是___________ 。
②用NaF除镁而不用 ,与反应
,与反应 有关,该反应的平衡常数为
有关,该反应的平衡常数为___________ (结果保留两位有效数字)。[ ,
, ]
]
(4) 的萃取率随溶液pH变化关系如题图所示。萃取
的萃取率随溶液pH变化关系如题图所示。萃取 时应调节溶液pH的范围为
时应调节溶液pH的范围为___________ 。
(5)通过氧化、除杂(铁、铜、镁)、萃取、反萃取、沉淀等过程,可制备 。已知
。已知 能被有机萃取剂(简称HA)萃取,其萃取原理可表示为
能被有机萃取剂(简称HA)萃取,其萃取原理可表示为 (水层)
(水层) (有机层)
(有机层) (有机层)
(有机层) (水层),则反萃取最好加入的试剂是
(水层),则反萃取最好加入的试剂是___________ 。
A. B.
B. C.
C.
草酸钴用途广泛,可用于指示剂和催化剂制备。一种利用水钴矿[主要成分为Co2O3,含少量Fe2O3、Al2O3、MnO、MgO、CaO等]制取CoC2O4 2H2O实验流程如下:
2H2O实验流程如下:
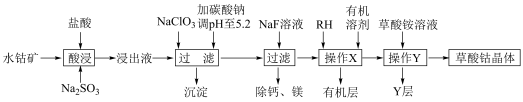
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
(1)写出1种能提高酸浸速率的措施___________ ,“沉淀”的化学式为___________ 。
(2)操作X所用的玻璃仪器的名称为___________ 。
(3)“酸浸”过程中加入Na2SO3的目的是将___________ 还原(填离子符号);NaClO3的作用是将浸出液中的Fe2+氧化,产物中氯元素处于最低化合价,该反应的离子方程式为___________ 。
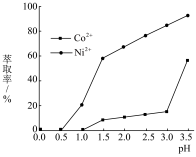
(4)试剂RH对金属离子的萃取率与pH的关系如图所示,加入萃取剂的作用是___________ ;使用萃取剂适宜的pH是___________ 。

A.接近2.0 B.接近3.0 C.接近4.0
(5)“除钙、镁”是将溶液中Ca2+与Mg2+转化为氟化物沉淀。已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10。当加入过量NaF后,所得滤液 =
=___________ 。

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 完全沉淀的pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)写出1种能提高酸浸速率的措施
(2)操作X所用的玻璃仪器的名称为
(3)“酸浸”过程中加入Na2SO3的目的是将
(4)试剂RH对金属离子的萃取率与pH的关系如图所示,加入萃取剂的作用是

A.接近2.0 B.接近3.0 C.接近4.0
(5)“除钙、镁”是将溶液中Ca2+与Mg2+转化为氟化物沉淀。已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10。当加入过量NaF后,所得滤液
实验室以工业钴渣为原料制取CoSO4溶液和ZnSO4·7H2O晶体,其实验流程如下:
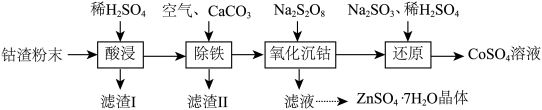
已知:①“酸浸”所得溶液中主要含CoSO4、ZnSO4,另含少量FeSO4、NiSO4。②金属活动性:Ni介于Fe、Cu之间。③下表是相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度1 mol·L-1计算,pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-):
(1)“酸浸”时所加稀硫酸不宜过量太多的原因是________ 。
(2)“除铁”时,向溶液中持续鼓入空气的作用是________ 。
(3)流程中需将滤渣Ⅰ、滤渣Ⅱ的洗涤液与“除铁”后所得滤液合并,目的是________ 。
(4)写出“还原”过程中Na2SO3、稀H2SO4与Co(OH)3反应的离子方程式:________ 。
(5)实验所得CoSO4溶液可用于制备CoCO3,制备时CoSO4饱和溶液与Na2CO3饱和溶液的混合方式为________ 。
(6)请结合如图硫酸锌晶体的溶解度曲线,设计从“氧化沉钴”后的滤液(含ZnSO4、Na2SO4、NiSO4等)中获取ZnSO4·7H2O的实验方案:取适量滤液,____________________________ ,过滤,用少量冰水洗涤,低温干燥得ZnSO4·7H2O晶体。(实验中须使用的试剂有:Zn粉、1.0 mol·L-1 NaOH、1.0 mol·L-1 H2SO4)


已知:①“酸浸”所得溶液中主要含CoSO4、ZnSO4,另含少量FeSO4、NiSO4。②金属活动性:Ni介于Fe、Cu之间。③下表是相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度1 mol·L-1计算,pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-):
| 金属离子 | 开始沉淀的pH | 完全沉淀的pH |
| Co2+ | 7.6 | 9.4 |
| Zn2+ | 5.9 | 8.9 |
(2)“除铁”时,向溶液中持续鼓入空气的作用是
(3)流程中需将滤渣Ⅰ、滤渣Ⅱ的洗涤液与“除铁”后所得滤液合并,目的是
(4)写出“还原”过程中Na2SO3、稀H2SO4与Co(OH)3反应的离子方程式:
(5)实验所得CoSO4溶液可用于制备CoCO3,制备时CoSO4饱和溶液与Na2CO3饱和溶液的混合方式为
(6)请结合如图硫酸锌晶体的溶解度曲线,设计从“氧化沉钴”后的滤液(含ZnSO4、Na2SO4、NiSO4等)中获取ZnSO4·7H2O的实验方案:取适量滤液,


已知不同金属离子生成氢氧化物沉淀所需的pH如下表。
| 开始沉淀的pH | 2.7 | 7.0 | 4.4 | 7.1 | 7.6 | 9.3 |
| 完全沉淀的pH | 3.7 | 9.6 | 6.4 | 9.2 | 9.2 | 10.8 |
(2)加入NiO能除去Fe、Cu的原因为
(3)向“除Fe、Cu”后的滤液中加入NaF溶液,使
①若溶液pH偏低,将会导致
②用NaF除镁而不用
(4)

(5)通过氧化、除杂(铁、铜、镁)、萃取、反萃取、沉淀等过程,可制备
A.
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


