多选题 适中0.65 引用1 组卷358
常温下, 和
和 溶于水及
溶于水及 受热分解的能量变化如图所示。下列说法错误的是
受热分解的能量变化如图所示。下列说法错误的是
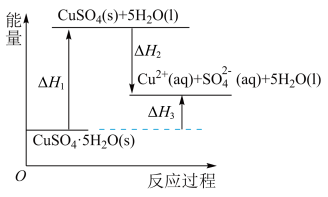

| A. |
| B. |
| C.常温下, |
| D.将 |
22-23高一下·山东潍坊·期中
类题推荐
CO、H2、C2H5OH三种物质燃烧的热化学方程式如下:
①CO(g)+1/2O2(g)=CO2(g) ΔH1=a kJ/mol
②H2(g)+1/2O2(g)=H2O(g) ΔH2=b kJ/mol
③C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g) ΔH3=c kJ/mol
下列说法不正确的是
①CO(g)+1/2O2(g)=CO2(g) ΔH1=a kJ/mol
②H2(g)+1/2O2(g)=H2O(g) ΔH2=b kJ/mol
③C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g) ΔH3=c kJ/mol
下列说法不正确的是
| A.ΔH1<0 |
| B.2CO(g)+4H2(g)=H2O(g)+C2H5OH(l) ΔH=(2a+4b-c) kJ/mol |
| C.CO2与H2合成C2H5OH反应的原子利用率为100% |
| D.2H2O(l)=2H2(g)+O2(g) ΔH=-2b kJ/mol |
下列关于热化学方程式的叙述正确的是
| A.已知HCN(g)=HNC(g) ΔH>0,则HCN更稳定 |
| B.已知2H2(g)+O2(g)=2H2O(g) ΔH=-483.6 kJ·mol-1,则H2的燃烧热为241.8 kJ·mol-1 |
| C.2Na(g)+O2(g)=Na2O2(g) ΔH1;2Na(s)+O2(g)=Na2O2(g) ΔH2,则ΔH1<ΔH2 |
| D.在稀溶液中:H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1,若将0.5 mol·L-1的稀H2SO4与1 mol·L-1的NaOH溶液等体积混合,放出的热量等于57.3 kJ |
反应 中,每生成0.25molN2放出166kJ的热量,该反应的速率表达式为
中,每生成0.25molN2放出166kJ的热量,该反应的速率表达式为 (k、m、n待测),其反应包含两步: ①
(k、m、n待测),其反应包含两步: ① (慢) ②
(慢) ②  (快) T℃时测得有关实验数据如下:
(快) T℃时测得有关实验数据如下:
下列说法正确的是
| 序号 | 速率/( | ||
| I | 0.0060 | 0.0010 | |
| II | 0.0060 | 0.0020 | |
| III | 0.0010 | 0.0060 | |
| IV | 0.0020 | 0.0060 |
| A.整个反应速率由第②步反应决定 |
| B.正反应的活化能一定是①<② |
| C.该反应速率表达式: |
| D.该反应的热化学方程式为 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


