单选题 适中0.65 引用1 组卷337

| A.工作时,电流方向为NiOOH电极→导线→Zn电极→电解质溶液→NiOOH电极 |
| B.工作一段时间后,电解液pH减小 |
| C.负极电极反应式为 |
| D.当电路中转移 |
22-23高一下·山东潍坊·期中
类题推荐
Ni/MH电池是一种以氢氧化氧镍(NiOOH)和储氢合金(MH)为电极,6mol·L-1KOH为电解质溶液的二次电池,其工作原理如图所示,下列说法错误的是
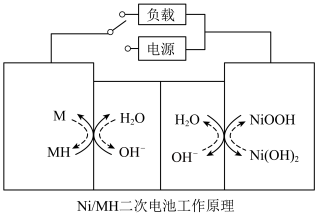

| A.放电时,左侧电极电势低于右侧 |
| B.放电时,右侧电极反应式为: |
| C.充电时,左侧电极附近pH升高 |
| D.充电时,转移1mole-,理论上右侧电极质量减轻1g |
草酸锌可应用于有机合成、电子工业等。工业上制取ZnC2O4的原理如图所示(电解液不参加反应,假设起始时两电极的质量相同),下列说法正确的是
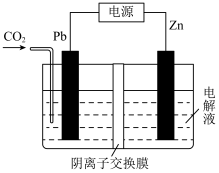
| A.电池工作时,Zn电极上发生还原反应 |
| B.每消耗5.6LCO2,同时转移的电子数为0.25NA |
| C.电池工作时,电路中电子的流动方向为Pb→电解液→Zn→电源→Pb |
| D.每消耗6.5gZn,两电极的质量相差6.5g |
锌—锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:
Zn(s)+2MnO2(s)+H2O(l)= Zn(OH)2(s)+Mn2O3(s),下列说法中错误的是
Zn(s)+2MnO2(s)+H2O(l)= Zn(OH)2(s)+Mn2O3(s),下列说法中错误的是
| A.电池工作时,锌失去电子 ,锌是负极 |
| B.外电路中每通过0.2mol电子,锌的质量理论上减小6.5g |
| C.电池负极的电极反应式为:Zn-2e-+2OH—=Zn(OH)2 |
| D.电池工作时,电子由负极流向正极,溶液中OH—向正极移动,K+、H+向负极移动 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


