单选题 适中0.65 引用1 组卷135
下列离子方程式中,正确的是
| A.氢氧化铁与碘化氢的反应: |
| B.向 |
| C.向 |
| D.工业上用 |
22-23高一下·湖北襄阳·期中
类题推荐
高铁酸盐在水溶液中有四种含铁型体,25℃时,它们的物质的量分数随pH的变化如图所示。下列叙述错误的是
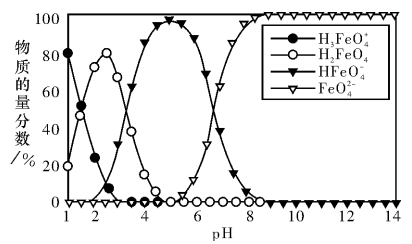

A.已知H3FeO4+的电离平衡常数分别为:K1=2.5×10-2,K2=4.8×10-4,K3=5.0×10-8,当pII=4时,溶液中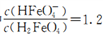 |
| B.为获得尽可能纯净的高铁酸盐,应控制pH≥9 |
| C.向pH=5的高铁酸盐溶液中加入KOH溶液,发生反应的离子方程式为HFeO4ˉ+OHˉ=FeO42-+H2O |
| D.pH=2时,溶液中主要含铁型体浓度的大小关系为c(H2FeO4)>c(H3FeO4+)> c (HFeO4ˉ) |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


