解答题-实验探究题 适中0.65 引用1 组卷319
I.回答下列问题:
(1)技要求写出下列各有机物中官能团的名称。
①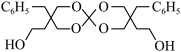 中含氧官能团的名称
中含氧官能团的名称___________ 。
②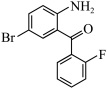 具有的官能团名称是
具有的官能团名称是___________ 。
(2)组成和结构可用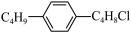 表示的有机物共有(不考虑立体异构)
表示的有机物共有(不考虑立体异构)______ 种。
Ⅱ.三乙氧基甲烷 主要用作医药中间体和感光材料,熔点
主要用作医药中间体和感光材料,熔点 ,沸点
,沸点 ,能溶于乙醇等多数有机溶剂,易燃,遇明火、高热或与氧化剂接触,有引起燃烧爆炸的危险。氯仿(CHCl3)和乙醇钠(
,能溶于乙醇等多数有机溶剂,易燃,遇明火、高热或与氧化剂接触,有引起燃烧爆炸的危险。氯仿(CHCl3)和乙醇钠( ,易溶于乙醇)在
,易溶于乙醇)在 的无水条件下反应可以制取三乙氧基甲烷并得到氯化钠,反应原理:
的无水条件下反应可以制取三乙氧基甲烷并得到氯化钠,反应原理: 。回答下列问题:
。回答下列问题:
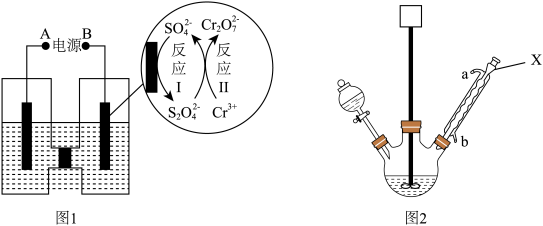
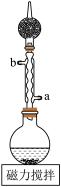
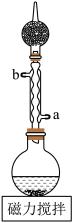
(3)反应装置如图所示,冷凝水应从___________ 端通入(填“a”或“b”)。将3L无水乙醇和490.5g氯仿加入反应器中磁力搅拌均匀,加入的无水乙醇是理论量的多倍,多余乙醇的作用是___________ 。
(4)再将207.0g钠切成小块,从冷凝管口门加入反应器,不搅拌,以保持钠块浮在液面上反应,其目的是___________ 。
(5)为保证反应持续进行,需要控制一定温度,但反应过程中不需要加热,其原因是_______ 。
(6)反应结束后,使用干燥仪器用抽滤法过滤出___________ 固体(填化学式),用___________ (填名称)洗涤该固体,将洗涤液合并入滤液,蒸馏滤液得到纯净的三乙氧基甲烷。
(1)技要求写出下列各有机物中官能团的名称。
①
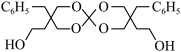 中含氧官能团的名称
中含氧官能团的名称②
 具有的官能团名称是
具有的官能团名称是(2)组成和结构可用
 表示的有机物共有(不考虑立体异构)
表示的有机物共有(不考虑立体异构)Ⅱ.三乙氧基甲烷
(3)反应装置如图所示,冷凝水应从
(4)再将207.0g钠切成小块,从冷凝管口门加入反应器,不搅拌,以保持钠块浮在液面上反应,其目的是
(5)为保证反应持续进行,需要控制一定温度,但反应过程中不需要加热,其原因是
(6)反应结束后,使用干燥仪器用抽滤法过滤出

22-23高二下·辽宁沈阳·阶段练习
类题推荐
三苯甲醇(相对分子质量为260)是重要的化工原料和医药中间体,实验室中可用格氏试剂与苯甲酸乙酯反应制备。实验原理:
反应①: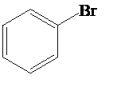 +Mg
+Mg
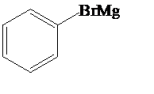 苯基溴化镁(格式试剂)
苯基溴化镁(格式试剂)
反应②:2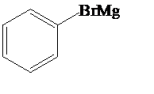 +
+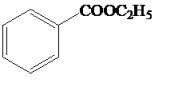

 (三苯甲氧基溴化镁)+C2H5OMg
(三苯甲氧基溴化镁)+C2H5OMg
反应③:

 (三苯甲醇)
(三苯甲醇)
实验步骤:
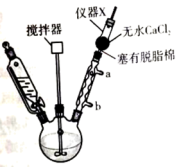
①向三颈烧瓶中加入镁屑和一小粒碘,按图组装实验装置,滴加溴苯、无水乙醚(易燃、易爆、易挥发)的混合液制备格氏试剂(极易水解),反应中保持微沸,直至Mg反应完;
②冷却后,将三颈烧瓶置于冰水浴中,搅拌下加入苯甲酸乙酯13mL(0.09mol)和15mL无水乙醚的混合液,温水浴回流反应0.5h,冷却后加入饱和氯化铵溶液;
③将反应装置改为蒸馏装置,回收乙醚并除去未反应的溴苯和其他副产物,三苯甲醇变为固体析出,抽滤,用石油醚洗涤,干燥得粗产品;
④粗产品经提纯得到纯品三苯甲醇16.0g。
相关物质的物理性质如下:
回答下列问题:
(1)实验装置图中,球形冷凝管的进水口是___________ (填“a”或“b”);仪器X的名称为___________ ,其下支管口塞有少量脱脂棉,目的是___________ ;无水CaCl2的作用是___________ 。
(2)制备格氏试剂时,加入一小粒碘可加快反应速率,推测I2对反应①活化能的影响是___________ (填“升高”“降低”或“不变”)。
(3)步骤③中用石油醚洗涤粗品,能否改用乙醚___________ (填“能”或“不能”)。
(4)粗产品提纯得到纯品的实验方法是___________ (填名称)。
(5)整个实验过程中严禁使用明火,原因是___________ 。
(6)本实验的产率是___________ 。
反应①:
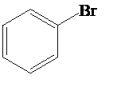 +Mg
+Mg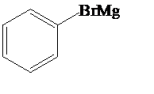 苯基溴化镁(格式试剂)
苯基溴化镁(格式试剂)反应②:2
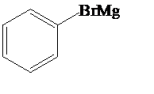 +
+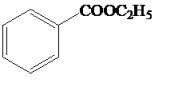
 (三苯甲氧基溴化镁)+C2H5OMg
(三苯甲氧基溴化镁)+C2H5OMg反应③:

 (三苯甲醇)
(三苯甲醇)实验步骤:
①向三颈烧瓶中加入镁屑和一小粒碘,按图组装实验装置,滴加溴苯、无水乙醚(易燃、易爆、易挥发)的混合液制备格氏试剂(极易水解),反应中保持微沸,直至Mg反应完;

②冷却后,将三颈烧瓶置于冰水浴中,搅拌下加入苯甲酸乙酯13mL(0.09mol)和15mL无水乙醚的混合液,温水浴回流反应0.5h,冷却后加入饱和氯化铵溶液;
③将反应装置改为蒸馏装置,回收乙醚并除去未反应的溴苯和其他副产物,三苯甲醇变为固体析出,抽滤,用石油醚洗涤,干燥得粗产品;
④粗产品经提纯得到纯品三苯甲醇16.0g。
相关物质的物理性质如下:
| 物质 | 熔点(℃) | 沸点(℃) | 溶解性 |
| 三苯甲醇 | 164.2 | 380 | 不溶于水,易溶于乙醚 |
| 乙醚 | -116.3 | 34.6 | 微溶于水,易溶于乙醇等 |
| 溴苯 | -30.7 | 156.2 | 不溶于水,易溶于乙醚 |
| 苯甲酸乙酯 | -34.6 | 212.6 | 不溶于水,易溶于乙醚 |
(1)实验装置图中,球形冷凝管的进水口是
(2)制备格氏试剂时,加入一小粒碘可加快反应速率,推测I2对反应①活化能的影响是
(3)步骤③中用石油醚洗涤粗品,能否改用乙醚
(4)粗产品提纯得到纯品的实验方法是
(5)整个实验过程中严禁使用明火,原因是
(6)本实验的产率是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
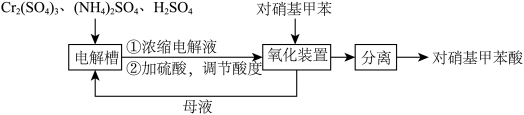
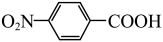 )是一种广泛用于医药、染料、感光材料等的重要精细化工中间体。工业上以对硝基甲苯(
)是一种广泛用于医药、染料、感光材料等的重要精细化工中间体。工业上以对硝基甲苯(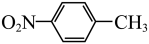 )、Cr(SO)3等物质为主要原料,通过间接电合成法制备对硝基苯甲酸,生产工艺流程如下:
)、Cr(SO)3等物质为主要原料,通过间接电合成法制备对硝基苯甲酸,生产工艺流程如下: