解答题-结构与性质 较易0.85 引用3 组卷507
铁在史前就为人们所用。在人类文明发展过程中,铁所起的作用是其他任何元素都不能比拟的。请回答下列问题:
(1)基态铁原子中,价电子电子云的伸展方向有_______ 种。
(2)五羰基合铁[Fe(CO)5]分解制铁晶体,反应过程中断裂和形成的化学键有_________ ( 填序号);
A.离子键 B.极性键 C.非极性键 D.配位键 E.金属键 F.范德华力
Fe(CO)5中各元素电负性的大小顺序是___________________ 。
(3)绿矾(FeSO4·7H2O)结构如图。

①H2O分别与Fe2+、 的相互作用分别为
的相互作用分别为_______________ 、_____________ 。
②比较 中的键角∠O−S−O
中的键角∠O−S−O________ H2O中的键角∠H−O−H。 (填“<” “>”或“=”)
(4)铁的化合物种类众多,其中FeF3的熔点高于1000°C,而FeBr3的熔点只有200°C,原因是___________ 。
(5)铁的一种配位化合物(普鲁士蓝)中铁氰骨架结构如图(a)所所示,骨架为正六面体,K+位于骨架的正六面体的空穴中,以平衡铁氰骨架的负电荷,则该钾盐的化学式为_____________________ 。

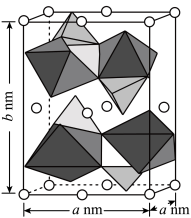
(6)一种锂电池的正极材料磷酸铁锂(LiFePO4) 的晶胞结构如上图(b)所示。其中Li+分别位于顶角、棱心、面心,O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。磷酸铁锂晶体的晶胞参数分别为anm、bnm,则磷酸铁锂晶体的摩尔体积Vm=____________ cm3·mol−1 (已知阿伏加德罗常数为NA,晶体的摩尔体积是指单位物质的量晶体所占的体积)。
(1)基态铁原子中,价电子电子云的伸展方向有
(2)五羰基合铁[Fe(CO)5]分解制铁晶体,反应过程中断裂和形成的化学键有
A.离子键 B.极性键 C.非极性键 D.配位键 E.金属键 F.范德华力
Fe(CO)5中各元素电负性的大小顺序是
(3)绿矾(FeSO4·7H2O)结构如图。

①H2O分别与Fe2+、
②比较
(4)铁的化合物种类众多,其中FeF3的熔点高于1000°C,而FeBr3的熔点只有200°C,原因是
(5)铁的一种配位化合物(普鲁士蓝)中铁氰骨架结构如图(a)所所示,骨架为正六面体,K+位于骨架的正六面体的空穴中,以平衡铁氰骨架的负电荷,则该钾盐的化学式为

(6)一种锂电池的正极材料磷酸铁锂(LiFePO4) 的晶胞结构如上图(b)所示。其中Li+分别位于顶角、棱心、面心,O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。磷酸铁锂晶体的晶胞参数分别为anm、bnm,则磷酸铁锂晶体的摩尔体积Vm=
2023·陕西·模拟预测
类题推荐
完成下列问题
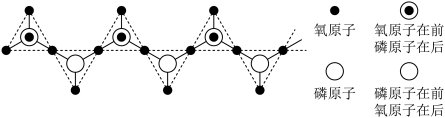
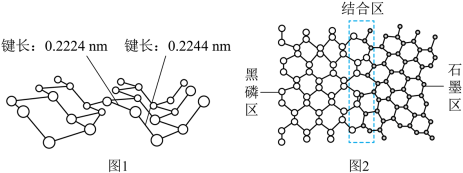
(1)黑磷与石墨类似,也具有层状结构(如图1),为了大幅度提高锂电池的充电速率,科学家研发了黑磷—石墨复合负极材料,其单层结构俯视图如图2所示。
①多个处于激发态1s22s12p23s1的碳原子,在回到基态的过程中,最多可发出___________ 种不同波长的光。
②与碳处于同一周期,第一电离能最大的元素的基态原子吸收能量后可得到多种激发态原子,其中形成的能量最低的激发态原子的电子排布图为___________ 。
③图2中,黑磷区P原子的杂化方式为___________ , 石墨区C原子的杂化方式为___________ 。
④根据图1和图2的信息,下列说法不正确的有___________ (填字母)。
a.黑磷区P—P键的键能完全相同
b.黑磷与石墨都属于混合型晶体
c.复合材料单层中,P原子与C原子之间的作用力属于范德华力
d.由石墨和黑磷制备该复合材料的过程,发生了化学反应
(2)科学家借用足球烯核心,实现高效且选择性可精准定制的离子跨膜运输,如下图所示:
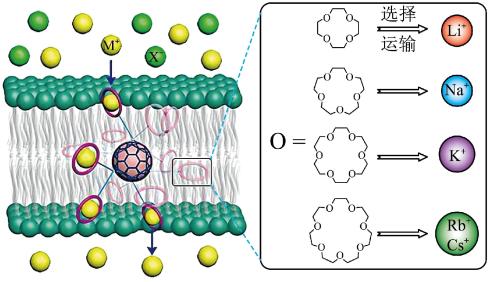
已知:①图中的有机物为“冠醚”,命名规则是“环上原子个数—冠醚氧原子个数”。
②几种冠醚与识别的碱金属离子的有关数据如下表所示:
①运输Li+的冠醚分子中σ键的数目为___________ ,运输Cs+的冠醚名称是___________ ,冠醚与碱金属离子之间存在微弱的配位键,配位原子是___________ 。
②根据上表中数据, 18—冠醚—6不能识别和运输Na+和Cs+的原因是___________ ;观察上图,冠醚不能识别和运输X—的主要原因可能是___________ 。
(3)一种锂电池的正极材料磷酸亚铁锂(LiFePO4)的晶胞结构如图所示。其中Li+分别位于晶胞的顶角、棱心、面心,O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构,该晶体的晶胞参数分别为a nm、b nm,则该晶体的摩尔体积Vm=___________ cm3·mol-1(已知阿伏加德罗常数为NA,晶体的摩尔体积是指单位物质的量晶体所占的体积。)
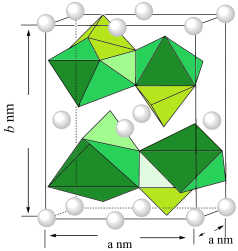
(1)黑磷与石墨类似,也具有层状结构(如图1),为了大幅度提高锂电池的充电速率,科学家研发了黑磷—石墨复合负极材料,其单层结构俯视图如图2所示。

①多个处于激发态1s22s12p23s1的碳原子,在回到基态的过程中,最多可发出
②与碳处于同一周期,第一电离能最大的元素的基态原子吸收能量后可得到多种激发态原子,其中形成的能量最低的激发态原子的电子排布图为
③图2中,黑磷区P原子的杂化方式为
④根据图1和图2的信息,下列说法不正确的有
a.黑磷区P—P键的键能完全相同
b.黑磷与石墨都属于混合型晶体
c.复合材料单层中,P原子与C原子之间的作用力属于范德华力
d.由石墨和黑磷制备该复合材料的过程,发生了化学反应
(2)科学家借用足球烯核心,实现高效且选择性可精准定制的离子跨膜运输,如下图所示:

已知:①图中的有机物为“冠醚”,命名规则是“环上原子个数—冠醚氧原子个数”。
②几种冠醚与识别的碱金属离子的有关数据如下表所示:
| 冠醚 | 冠醚空腔直径/pm | 适合的粒子直径/pm |
| 12—冠醚—4 | 120~ 150 | Li+(152) |
| 15—冠醚—5 | 170~ 220 | Na+ (204) |
| 18—冠醚—6 | 260~ 320 | K+(276) |
| 340~ 430 | Rb+(304) | |
| Cs+(334) |
②根据上表中数据, 18—冠醚—6不能识别和运输Na+和Cs+的原因是
(3)一种锂电池的正极材料磷酸亚铁锂(LiFePO4)的晶胞结构如图所示。其中Li+分别位于晶胞的顶角、棱心、面心,O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构,该晶体的晶胞参数分别为a nm、b nm,则该晶体的摩尔体积Vm=

铁(Fe)、钴(Co)、镍(Ni)是第四周期第VIII族的元素,在化学上称为铁系元素,其化合物在生产生活中应用广泛。
(1)基态Ni原子的核外电子排布式为_______ 。
(2)铁系元素能与CO形成Fe(CO)5、Ni(CO)4等金属羰基化合物。已知室温时Fe(CO)5为浅黄色液体,沸点103oC,则Fe(CO)5中含有的化学键类型包括_______。
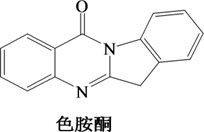
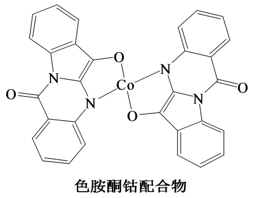
(3)以甲醇为溶剂,Co2+可与色胺酮分子配位结合形成对DNA具有切割作用的色胺酮钴配合物(合成过程如下所示)。色胺酮分子中所含元素(H、C、N、O)第一电离能由大到小的顺序为_______ ,色氨酮分子中N原子的杂化类型为_______ 。X射线衍射分析显示色胺酮钴配合物晶胞中还含有一个CH3OH分子,CH3OH是通过_______ 作用与色胺酮钴配合物相结合。

(4)LiFePO4常用作锂离子电池的正极材料,其阴离子PO 的空间构型为
的空间构型为_______ ,与PO 互为等电子体的微粒有
互为等电子体的微粒有_______ (任写一种)。
(5)Fe、Co、Ni与Ca都位于第四周期且最外层电子数相同,但相应单质的熔点,Fe、Co、Ni明显高于Ca,其原因是_______ 。
(6)ZnS是一种使用广泛的荧光材料。已知立方ZnS的晶胞结构如图所示:
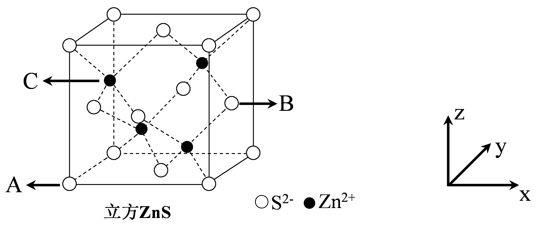
①已知A、B点的原子坐标分别为(0,0,0)和(1, ,
, ),则C点的原子坐标为
),则C点的原子坐标为_______ ;
②立方ZnS的晶胞参数a=541pm,则其晶体密度为_______ g·cm-3.(列出计算表达式,设NA为阿伏加德罗常数的值)
(1)基态Ni原子的核外电子排布式为
(2)铁系元素能与CO形成Fe(CO)5、Ni(CO)4等金属羰基化合物。已知室温时Fe(CO)5为浅黄色液体,沸点103oC,则Fe(CO)5中含有的化学键类型包括_______。
| A.极性共价键 | B.离子键 | C.配位键 | D.金属键 |


(4)LiFePO4常用作锂离子电池的正极材料,其阴离子PO
(5)Fe、Co、Ni与Ca都位于第四周期且最外层电子数相同,但相应单质的熔点,Fe、Co、Ni明显高于Ca,其原因是
(6)ZnS是一种使用广泛的荧光材料。已知立方ZnS的晶胞结构如图所示:

①已知A、B点的原子坐标分别为(0,0,0)和(1,
②立方ZnS的晶胞参数a=541pm,则其晶体密度为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网