单选题 适中0.65 引用4 组卷317
某同学为测定某NaHCO3(含少量NaCl)固体中NaHCO3的含量,设计如下实验。
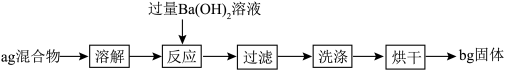
| A.NaHCO3的质量分数为: |
| B.可通过恒重操作确保固体完全烘干 |
| C.反应的离子方程式为:HCO |
| D.确定Ba(OH)2是否过量的操作:取上层清液,继续加Ba(OH)2溶液,看有无沉淀生成 |
2023·上海虹口·二模
类题推荐
常温下,通过下列实验探究NaHCO3溶液的性质。
已知:常温下,碳酸的电离平衡常数:Ka1=4.3×10-7,Ka2=5.1×10-11。下列有关说法正确的是
| 实验 | 实验操作和现象 |
| 1 | 向0.1mol·L-1NaHCO3溶液中加入一定量0.1mol·L-1NaOH溶液,测得溶液的pH为10.0 |
| 2 | 将浓度均为0.1mol·L-1NaHCO3溶液和Ba(OH)2溶液按等体积混合,产生白色沉淀 |
| 3 | 将浓度均为0.1mol·L-1NaHCO3溶液和HCl溶液按体积比2:1混合,产生无色气体 |
| 4 | 将0.1mol·L-1NaHCO3溶液滴入0.1mol·L-1FeSO4溶液,生成沉淀,产生无色气体 |
| A.实验1所得溶液中存在c(HCO |
| B.由实验2可知Ksp(BaCO3)=2.5×10-3 |
| C.实验3所得的溶液中存在c(H+)+c(Na+)=2c(CO |
| D.实验4中反应的离子方程式为Fe2++CO |
某实验小组利用传感器探究Na2CO3和NaHCO3的性质。已知:pH越大,溶液碱性越强。下列分析正确的是
| 实验序号 | 实验操作 | 实验数据或实验现象 |
| 实验1 |  | 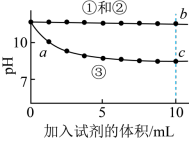 |
| 实验2 | 向碳酸氢钠溶液中加入一定浓度CaCl2溶液 | 产生白色沉淀和无色气泡 |
| A.①与②的实验数据基本相同,说明②中的OH-未参与该反应 |
| B.实验2中发生反应的离子方程式为Ca2++ |
| C.a点反应的离子方程式为:Ca2++2OH-+2 |
| D.Na2CO3和NaHCO3的稀溶液可利用Ba(OH)2溶液鉴别 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


