填空题 适中0.65 引用1 组卷297
I、
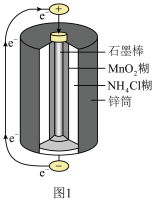
(1)锌锰干电池是最早使用的化学电池,其基本构造如图1所示:电路中每通过0.4mole-,负极质量减少___________________ g;工作时NH 在正极放电产生两种气体,其中一种气体分子是10eˉ的微粒,正极的电极反应式是
在正极放电产生两种气体,其中一种气体分子是10eˉ的微粒,正极的电极反应式是__________ 。
(2)比能量是指消耗单位质量的电极所释放的电量,用来衡量电池的优劣,则Li、Na、Al分别作为电极时比能量由大到小的顺序为__________ 。
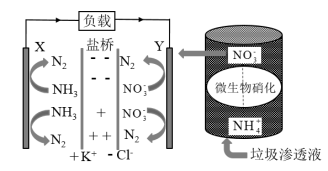
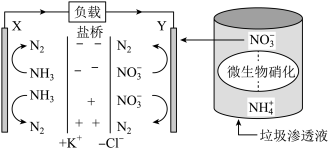
(3)某种利用垃圾渗透液实现发电装置示意图如下,当该装置工作时,Y极发生的电极反应式为____________ 。
II.锂一空气电池的理论能量密度高,是未来提高电动汽车续航里程的关键。
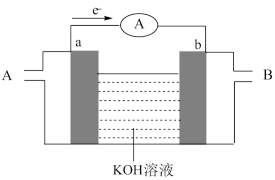
(4)锂一空气电池的反应原理可表示为: 。其放电时的工作原理如图所示:
。其放电时的工作原理如图所示:
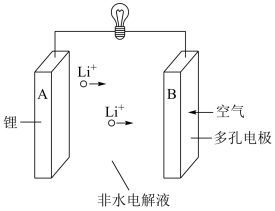
电池工作时,发生氧化反应的是___________ (填“A”或“B”)极。
(5)空气中的CO2、H2O影响电池放电。探究H2O对放电的影响:向非水电解液中加入少量水,放电后检测A、B电极上的固体物质。
A极:LiOH B极:Li2O2、LiOH
①A、B电极产生LiOH的化学方程式分别是__________ 、____________ 。
②H2O降低锂一空气电池放电、充电循环性能。
(6)探究CO2对放电的影响:使电池在三种不同气体(物质的量相等)中放电,测量外电路转移的电子与消耗O2的比值[ ]。
]。
①放电时,实验i中B极的电极反应式为_________________ 。
②下列分析正确的是_________________ 。
a.放电时,i、iii中通过外电路的电子数相等
b.ⅲ中B极所发生的电极反应的产物主要为Li2O2
c.ⅲ中 ,说明CO2未与Li2O2反应
,说明CO2未与Li2O2反应
(1)锌锰干电池是最早使用的化学电池,其基本构造如图1所示:电路中每通过0.4mole-,负极质量减少

(2)比能量是指消耗单位质量的电极所释放的电量,用来衡量电池的优劣,则Li、Na、Al分别作为电极时比能量由大到小的顺序为
(3)某种利用垃圾渗透液实现发电装置示意图如下,当该装置工作时,Y极发生的电极反应式为

II.锂一空气电池的理论能量密度高,是未来提高电动汽车续航里程的关键。
(4)锂一空气电池的反应原理可表示为:

电池工作时,发生氧化反应的是
(5)空气中的CO2、H2O影响电池放电。探究H2O对放电的影响:向非水电解液中加入少量水,放电后检测A、B电极上的固体物质。
A极:LiOH B极:Li2O2、LiOH
①A、B电极产生LiOH的化学方程式分别是
②H2O降低锂一空气电池放电、充电循环性能。
(6)探究CO2对放电的影响:使电池在三种不同气体(物质的量相等)中放电,测量外电路转移的电子与消耗O2的比值[
| 实验 | i | ii | iii |
| 气体 | O2 | CO2 | |
| ≈2 | ≈2 |
②下列分析正确的是
a.放电时,i、iii中通过外电路的电子数相等
b.ⅲ中B极所发生的电极反应的产物主要为Li2O2
c.ⅲ中
22-23高一下·四川内江·阶段练习
类题推荐
锂—空气电池的理论能量密度高,是未来提高电动汽车续航里程的关键。
(1)锂在元素周期表中的位置是___________ ,属于比较活泼的金属。
(2)锂—空气电池的反应原理可表示为: 。其放电时的工作原理如下图所示:
。其放电时的工作原理如下图所示:
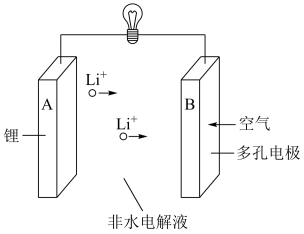
电池工作时,发生氧化反应的是___________ (填“ ”或“
”或“ ”)极。
”)极。
(3)空气中的 、
、 影响电池放电。探究
影响电池放电。探究 对放电的影响:向非水电解液中加入少量水,放电后检测
对放电的影响:向非水电解液中加入少量水,放电后检测 、
、 电极上的固体物质。
电极上的固体物质。
 极:
极:
 极:
极: 、
、
① 、
、 电极产生
电极产生 的化学方程式分别是
的化学方程式分别是___________ 、___________ 。
② 降低锂—空气电池放电、充电循环性能。
降低锂—空气电池放电、充电循环性能。
(4)探究 对放电的影响:使电池在三种不同气体(物质的量相等)中放电,测量外电路转移的电子与消耗
对放电的影响:使电池在三种不同气体(物质的量相等)中放电,测量外电路转移的电子与消耗 的比值[
的比值[ ]。
]。
①放电时,实验i中 极的电极反应式为
极的电极反应式为___________ 。
②下列分析正确的是___________ 。
a. 放电时,i、iii中通过外电路的电子数相等
b. iii中 极所发生的电极反应的产物主要为
极所发生的电极反应的产物主要为
c. iii中 ,说明
,说明 未与
未与 反应
反应
③i、iii中电池放电完毕后充电,iii中产生 的量少于i,推测原因:一是iii中
的量少于i,推测原因:一是iii中 的量比i少,生成
的量比i少,生成 的量较i少;二是
的量较i少;二是___________ 。
(1)锂在元素周期表中的位置是
(2)锂—空气电池的反应原理可表示为:

电池工作时,发生氧化反应的是
(3)空气中的
①
②
(4)探究
| 实验 | i | ii | iii |
| 气体 | |||
②下列分析正确的是
a. 放电时,i、iii中通过外电路的电子数相等
b. iii中
c. iii中
③i、iii中电池放电完毕后充电,iii中产生
电池是一种将化学能直接转化为电能的装置,其出现方便了人们的生活。
(1)关于碱性锌锰电池(图1),下列说法正确的是_______。
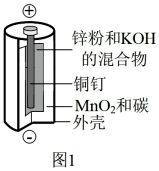
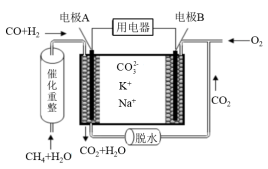
(2)锂-空气电池(图2)的理论能量密度高,是决定未来电动汽车续航里程的关键。锂一空气电池的反应原理可表示为:2Li+O2 Li2O2。
Li2O2。
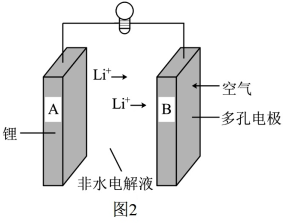
①电池充电时B电极连接外接电源的_______ 极。
②探究H2O对放电的影响;向非水电解液中加入少量水,放电后检测到A、B电极均有LiOH固体产生,则B电极产生LiOH固体的电极反应式为_______ 。
(3)铝离子电池(图3)具有高效耐用、超快充电等优势。已知正极反应物为CnAlCl4。
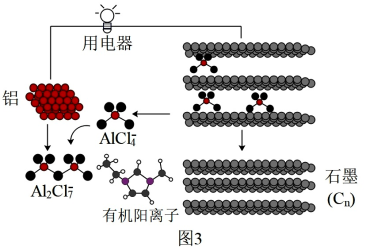
①充电时有机阳离子向_______ 电极移动(填“铝”或“石墨”)。
②放电时每消耗1mol铝,会生成_______ molAl2Cl 。
。
③充电时阳极的电极反应式为_______ 。
(4)若用电解法电解苯酚(C6H5OH)产生CO2,当转移7mol电子时,产生CO2_______ mol。
(1)关于碱性锌锰电池(图1),下列说法正确的是_______。

| A.碱性锌锰电池克服了酸性锌锰电池较易自放电的缺点 |
| B.电池工作时,电子由负极经过内层固体电解质流向铜钉 |
| C.负极的电极反应式为Zn-2e=Zn2+ |
| D.用该电池电解精炼粗铜,负极反应6.5g锌时,阳极一定消耗6.4g固体 |

①电池充电时B电极连接外接电源的
②探究H2O对放电的影响;向非水电解液中加入少量水,放电后检测到A、B电极均有LiOH固体产生,则B电极产生LiOH固体的电极反应式为
(3)铝离子电池(图3)具有高效耐用、超快充电等优势。已知正极反应物为CnAlCl4。

①充电时有机阳离子向
②放电时每消耗1mol铝,会生成
③充电时阳极的电极反应式为
(4)若用电解法电解苯酚(C6H5OH)产生CO2,当转移7mol电子时,产生CO2
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网