解答题-原理综合题 较难0.4 引用1 组卷248
CO2资源化利用和转化、消除硫、氮等引起的污染已成为当今科学研究的热点。
(1)加氢法减碳:制甲醇的总反应可表示为:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH。该反应一般认为通过如下步骤来实现:
Ⅰ.CO2(g)+H2(g)=CO(g)+H2O(g) ΔH1=+41kJ·mol-1
Ⅱ.CO(g)+2H2(g)=CH3OH(g) ΔH2=-90kJ·mol-1
①总反应的ΔH=_______ kJ·mol-1;
②若反应Ⅰ为慢反应,下列示意图中能体现上述反应能量变化的是_______ 填标号)。
A.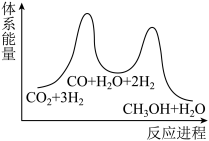 B.
B.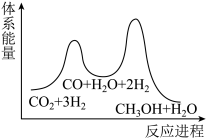
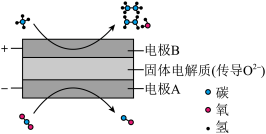
③CH4和CO2都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如下图所示,阴极上的反应式为_______ 。
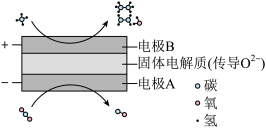
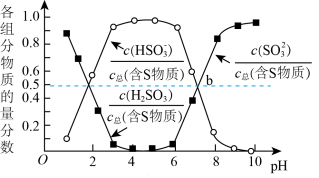
(2)吸收法脱硫:亚硫酸铵溶液可以处理SO2,(NH4)2SO3+SO2+H2O=2NH4HSO3,25℃时溶液pH与各组分物质的量分数变化关系如图所示。b点时溶液pH=7,则
_______ 。
(3)还原法脱氮:用催化剂协同纳米零价铁去除水体中NO 。催化还原过程如图所示。
。催化还原过程如图所示。
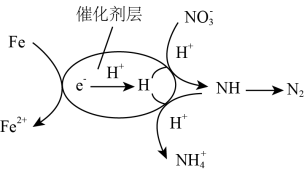
①该反应机理中生成N2的过程可描述为_______ 。
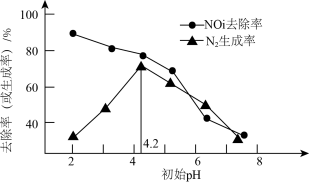
②过程中NO 去除率及N2生成率如图所示,为有效降低水体中氮元素的含量,宜调整水体pH为4.2,当
去除率及N2生成率如图所示,为有效降低水体中氮元素的含量,宜调整水体pH为4.2,当 时,随pH减小,N2生成率逐渐降低的原因是
时,随pH减小,N2生成率逐渐降低的原因是_______ 。
(1)加氢法减碳:制甲醇的总反应可表示为:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH。该反应一般认为通过如下步骤来实现:
Ⅰ.CO2(g)+H2(g)=CO(g)+H2O(g) ΔH1=+41kJ·mol-1
Ⅱ.CO(g)+2H2(g)=CH3OH(g) ΔH2=-90kJ·mol-1
①总反应的ΔH=
②若反应Ⅰ为慢反应,下列示意图中能体现上述反应能量变化的是
A.
 B.
B.
③CH4和CO2都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如下图所示,阴极上的反应式为

(2)吸收法脱硫:亚硫酸铵溶液可以处理SO2,(NH4)2SO3+SO2+H2O=2NH4HSO3,25℃时溶液pH与各组分物质的量分数变化关系如图所示。b点时溶液pH=7,则

(3)还原法脱氮:用催化剂协同纳米零价铁去除水体中NO

①该反应机理中生成N2的过程可描述为
②过程中NO

22-23高二下·江苏·阶段练习
类题推荐
I:已知反应: 。在一定体积的容器内发生上述反应,反应中
。在一定体积的容器内发生上述反应,反应中 的浓度随时间的变化如下表:
的浓度随时间的变化如下表:
(1)该反应的平衡常数表达式是K=______ 。根据表中数据计算1300℃时, 在4分钟内的反应速率=
在4分钟内的反应速率=______  。达到平衡时
。达到平衡时 的转化率=
的转化率=_______ %(结果保留到0.1%)
(2)表中a______ b,c______ 1.23(选填“>”、“<”或“=”)。
Ⅱ:CO2资源化利用和转化、消除硫、氮等引起的污染已成为当今科学研究的热点。
(3)加氢法减碳:制甲醇的总反应可表示为:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH。该反应一般认为通过如下步骤来实现:
I.CO2(g)+H2(g)=CO(g)+H2O(g) ΔH1=+41kJ·mol-1
Ⅱ.CO(g)+2H2(g)=CH3OH(g) ΔH2=-90kJ·mol-1
①总反应的ΔH=___________ kJ·mol-1;
②若反应I为慢反应,下列示意图中能体现上述反应能量变化的是___________ 填标号)。
a. B.
B.
③CH4和CO2都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如下图所示,阴极上的反应式为___________ 。
| 温度 时间(分钟) | 1300℃ | 高于1300℃ |
| 0 | 2mol•L-1 | 2mol•L-1 |
| 2 | amol•L-1 | bmol•L-1 |
| 4 | 1.4mol•L-1 | cmol•L-1 |
| 6 | 1.23mol•L-1 | cmol•L-1 |
| 8 | 1.23mol•L-1 | cmol•L-1 |
(2)表中a
Ⅱ:CO2资源化利用和转化、消除硫、氮等引起的污染已成为当今科学研究的热点。
(3)加氢法减碳:制甲醇的总反应可表示为:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH。该反应一般认为通过如下步骤来实现:
I.CO2(g)+H2(g)=CO(g)+H2O(g) ΔH1=+41kJ·mol-1
Ⅱ.CO(g)+2H2(g)=CH3OH(g) ΔH2=-90kJ·mol-1
①总反应的ΔH=
②若反应I为慢反应,下列示意图中能体现上述反应能量变化的是
a.
 B.
B.
③CH4和CO2都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如下图所示,阴极上的反应式为

有效去除大气中的氮氧化物( )和水体中的氮是环境保护的重要课题。
)和水体中的氮是环境保护的重要课题。
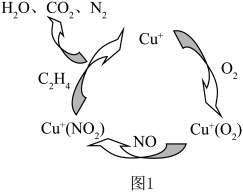
(1)乙烯还原。目前,科学家在研究一种以乙烯作为还原剂的脱硝(NO)原理,其脱硝机理示意图如图1所示。写出该脱硝原理总反应的化学方程式:__ ; 氧化。按一定流速将含NO的废气通过
氧化。按一定流速将含NO的废气通过 溶液,NO可转化成
溶液,NO可转化成 被吸收。请写出NO与
被吸收。请写出NO与 反应的离子方程式
反应的离子方程式__ ;
(3)氢气催化还原。
主反应:
副反应:
①则反应:2NO(g)+N2(g) 2N2O(g)
2N2O(g)  =
=__ kJ•mol-1
②某温度下 的体积分数对
的体积分数对 还原NO反应的影响如图2所示。当
还原NO反应的影响如图2所示。当 的体积分数大于
的体积分数大于 时,
时, 的体积分数呈下降趋势,原因是
的体积分数呈下降趋势,原因是__ ;
将原煤经热解、冷却得到煤焦,NO的脱除主要含吸附和化学还原两个过程,煤焦表面存在的官能团有利于NO的吸附,其数量与煤焦中氢碳质量比的值密切相关。热解温度为500℃、900℃得到的煤焦分别用S-500、S-900表示,相关信息如表:
则相同温度下,S-900对NO的脱除率比S-500的低,可能的原因是__ ;
(5)地下水中的 可用还原法处理,
可用还原法处理, 可被还原为
可被还原为 、NO、
、NO、 等。利用Zn和
等。利用Zn和 溶液反应模拟地下水的脱硝过程、探究脱硝原理及相关因素对脱硝速率的影响。模拟过程的实验装置如图3所示。实验时用0.1mol/L
溶液反应模拟地下水的脱硝过程、探究脱硝原理及相关因素对脱硝速率的影响。模拟过程的实验装置如图3所示。实验时用0.1mol/L 洗涤Zn粒,再用蒸馏水洗涤至接近中性;将
洗涤Zn粒,再用蒸馏水洗涤至接近中性;将 溶液的pH调至2.5。
溶液的pH调至2.5。 的目的是
的目的是__ 。
②向上述 溶液中加入足量洗涤后的Zn粒,写出Zn与
溶液中加入足量洗涤后的Zn粒,写出Zn与 溶液反应生成
溶液反应生成 的离子方程式:
的离子方程式:__ ;
(6)有人研究了用纳米零价铁去除水体中 。控制其他条件不变,用纳米零价铁还原水体中的
。控制其他条件不变,用纳米零价铁还原水体中的 ,测得溶液中
,测得溶液中 、
、 、
、 浓度随时间变化如图4所示。与初始溶液中氮浓度相比,反应过程中溶液中的总氮(
浓度随时间变化如图4所示。与初始溶液中氮浓度相比,反应过程中溶液中的总氮( 、
、 、
、 )浓度减少,其可能原因是
)浓度减少,其可能原因是__ 。
(1)乙烯还原。目前,科学家在研究一种以乙烯作为还原剂的脱硝(NO)原理,其脱硝机理示意图如图1所示。写出该脱硝原理总反应的化学方程式:
(3)氢气催化还原。
主反应:
副反应:
①则反应:2NO(g)+N2(g)
②某温度下
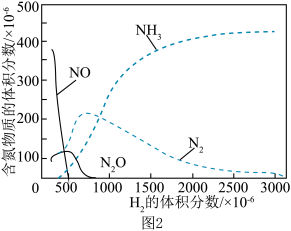
将原煤经热解、冷却得到煤焦,NO的脱除主要含吸附和化学还原两个过程,煤焦表面存在的官能团有利于NO的吸附,其数量与煤焦中氢碳质量比的值密切相关。热解温度为500℃、900℃得到的煤焦分别用S-500、S-900表示,相关信息如表:
煤焦 | 元素分析(%) | |
C | H | |
S-500 | 80.79 | 2.76 |
S-900 | 84.26 | 0.82 |
(5)地下水中的

②向上述
(6)有人研究了用纳米零价铁去除水体中

利用太阳能光解水,制备的H2用于还原CO2合成甲醇,可实现资源的再利用。
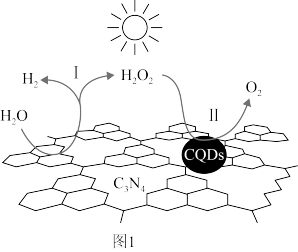
(1)中国科学家研究的复合光催化剂[碳纳米点(CQDs)/氮化碳(C3N4)纳米复合物]可以利用太阳光高效分解水,其原理如图1所示。反应I的化学方程式为_____ 。
(2)H2和CO、CO2在催化剂的作用下合成甲醇的主要反应如下:
第一步:CO2(g)+H2(g) CO(g)+H2O(g) △H1=+41 kJ·mol-1
CO(g)+H2O(g) △H1=+41 kJ·mol-1
第二步:CO(g)+2H2(g) CH3OH(g) △H2=-99 kJ·mol-1
CH3OH(g) △H2=-99 kJ·mol-1
CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=
CH3OH(g)+H2O(g) △H=_____ 。
②第二步反应中的相关化学键的键能(E)数据如表,试计算x=_____ 。(提示:CO中的化学键与N2中的化学键类似)
(3)在水溶液中电解CO2生成甲醇的原理如图2所示。
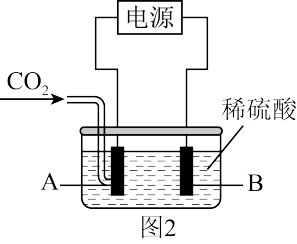
①写出A电极生成甲醇的电极反应式:____ 。
②A极生成1 mol甲醇时,B极生成气体在标准状况下的体积是_____ 。
(4)金刚石和石墨燃烧反应中的能量变化如图3所示。

图3
由图3可知:石墨的燃烧热△H=____ 。
(5)燃煤烟气中的NOx、SO2经处理后可被吸收。若烟气主要成分为NO、SO2,可通过电解法除去,其原理如图4所示。
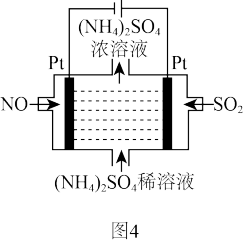
阴极的电极反应式为____ 。电解过程得到的产物为_____ 。
(1)中国科学家研究的复合光催化剂[碳纳米点(CQDs)/氮化碳(C3N4)纳米复合物]可以利用太阳光高效分解水,其原理如图1所示。反应I的化学方程式为

(2)H2和CO、CO2在催化剂的作用下合成甲醇的主要反应如下:
第一步:CO2(g)+H2(g)
第二步:CO(g)+2H2(g)
CO2(g)+3H2(g)
②第二步反应中的相关化学键的键能(E)数据如表,试计算x=
| 化学键 | H-H | C-O | C≡O | H-O | C-H |
| E/kJ·mol-1 | 436 | x | 1076 | 465 | 413 |

①写出A电极生成甲醇的电极反应式:
②A极生成1 mol甲醇时,B极生成气体在标准状况下的体积是
(4)金刚石和石墨燃烧反应中的能量变化如图3所示。

图3
由图3可知:石墨的燃烧热△H=
(5)燃煤烟气中的NOx、SO2经处理后可被吸收。若烟气主要成分为NO、SO2,可通过电解法除去,其原理如图4所示。

阴极的电极反应式为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


