解答题-实验探究题 适中0.65 引用2 组卷306
三聚氯氰是重要的精细化工产品,具有广泛的用途,其生产通常是由氯化氰制备和氯化氰聚合两个过程组成。
I.氯化氰制备
已知:氯化氰为无色液体,熔点-6.5℃,沸点12.5℃。可溶于水、乙醇、乙醚等,遇水缓慢水解为氰酸和盐酸。现用氰化钠和氯气在四氯化碳中反应制备氯化氰,反应式:NaCN+Cl2=NaCl+CNCl。反应装置如图所示,在三口烧瓶上装有温度计、搅拌器、进气管、出气管,据图回答下列问题:
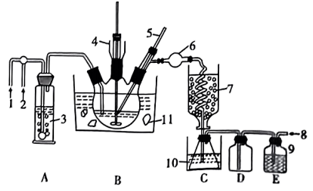
(1)CNCl的结构式为______ ;其中C原子的杂化类型为______ 。
(2)在氯化氰的制备装置中,装置3、装置9中的试剂为______ 。在反应前需要先向装置内通入约3分钟干燥氮气,目的是_____ 。
(3)该制备分为两个阶段。
阶段一:将40g氰化钠粉末及140mL四氯化碳装入烧瓶中,缓慢送入氯气并搅拌使得氯气与NaCN充分反应。此阶段装置7、装置10、装置11作用相同,为______ ;当D中出现______ 现象时,说明阶段一结束。
阶段二:将______ (填“装置7”“装置10”或“装置11”)的温度调整至60℃,将_____ (填“装置7”“装置10”或“装置11”)的温度调整至-40℃并缓慢通入氮气直至阶段二结束。阶段二结束之后产品将被集中在_____ 中(填字母)。
II.氯化氰聚合
(4)氯化氰干燥后,在聚合塔中加热至400℃后便能得到氯化氰三聚物,请画出氯化氰三聚物的结构式:______ 。
I.氯化氰制备
已知:氯化氰为无色液体,熔点-6.5℃,沸点12.5℃。可溶于水、乙醇、乙醚等,遇水缓慢水解为氰酸和盐酸。现用氰化钠和氯气在四氯化碳中反应制备氯化氰,反应式:NaCN+Cl2=NaCl+CNCl。反应装置如图所示,在三口烧瓶上装有温度计、搅拌器、进气管、出气管,据图回答下列问题:

(1)CNCl的结构式为
(2)在氯化氰的制备装置中,装置3、装置9中的试剂为
(3)该制备分为两个阶段。
阶段一:将40g氰化钠粉末及140mL四氯化碳装入烧瓶中,缓慢送入氯气并搅拌使得氯气与NaCN充分反应。此阶段装置7、装置10、装置11作用相同,为
阶段二:将
II.氯化氰聚合
(4)氯化氰干燥后,在聚合塔中加热至400℃后便能得到氯化氰三聚物,请画出氯化氰三聚物的结构式:
22-23高三·重庆渝中·阶段练习
类题推荐
溴乙烷(CH3CH2Br)是种挥发性很强的无色液体,沸点38.4℃,密度为1.46g/cm3,难溶于水,是有机合成的重要原料。实验室制备溴乙烷过程中涉及的反应有:
NaBr+H2SO4 HBr↑+NaHSO4;
HBr↑+NaHSO4;
CH3CH2OH+HBr CH3CH2Br+H2O;
CH3CH2Br+H2O;
CH3CH2OH H2C=CH2↑+H2O;
H2C=CH2↑+H2O;
2CH3CH2OH H2O+CH3CH2OCH2CH3(乙醚)。
H2O+CH3CH2OCH2CH3(乙醚)。
已知乙醚的密度为0.71g/cm3,沸点34.6℃。
实验步骤:
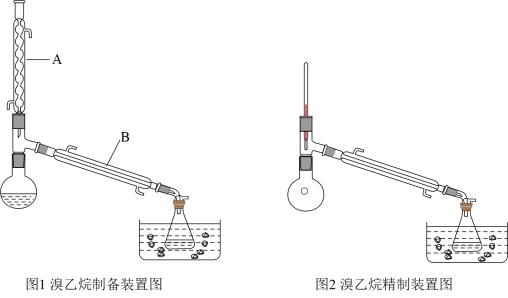
(1)溴乙烷的制备:烧瓶中加入19mL浓硫酸(0.35mol)、10mL乙醇(0.17mol)及9mL水,冷却至室温,再加入溴化钠15.5g(0.15mol)和几粒沸石,如图1(加热及夹持装置略去),锥形瓶内放入饱和亚硫酸氢钠溶液并置于冰水浴中,小火加热烧瓶至反应结束。
(2)溴乙烷的精制:对(1)中馏出液进行分液,在冰水浴条件下将有机层转入干燥的锥形瓶中,在冰水浴条件下逐滴加入2mL浓硫酸除去杂质,再次分液,弃去硫酸层,得到溴乙烷的粗产品。然后将粗产品转入图2烧瓶中,在水浴条件下加热并收集35-40℃馏分,产量为10.0g。
回答下列问题:
(1)根据实验药品的用量,制备溴乙烷时烧瓶的最适宜规格为____ 。
(2)向图1装置中加料,浓硫酸、乙醇、水三种物质加入烧瓶的先后顺序为____ ;反应中有棕黄色气体产生,该反应的化学方程式为____ ;锥形瓶内饱和亚硫酸氢钠溶液的作用是____ (用离子反应方程式表示);溴乙烷的制备实验完成的标志是____ 。
(3)图1中A为上口加有塞子的回流装置,其作用为____ 。
(4)溴乙烷的精制阶段,第一次分液应保留____ (填“上层”或“下层”)液体;整个制备和精制阶段采用冰水浴的原因是____ 。
(5)本实验溴乙烷的产率为____ (小数点后保留2位,产率= ×100%)。
×100%)。
NaBr+H2SO4
CH3CH2OH+HBr
CH3CH2OH
2CH3CH2OH
已知乙醚的密度为0.71g/cm3,沸点34.6℃。

实验步骤:
(1)溴乙烷的制备:烧瓶中加入19mL浓硫酸(0.35mol)、10mL乙醇(0.17mol)及9mL水,冷却至室温,再加入溴化钠15.5g(0.15mol)和几粒沸石,如图1(加热及夹持装置略去),锥形瓶内放入饱和亚硫酸氢钠溶液并置于冰水浴中,小火加热烧瓶至反应结束。
(2)溴乙烷的精制:对(1)中馏出液进行分液,在冰水浴条件下将有机层转入干燥的锥形瓶中,在冰水浴条件下逐滴加入2mL浓硫酸除去杂质,再次分液,弃去硫酸层,得到溴乙烷的粗产品。然后将粗产品转入图2烧瓶中,在水浴条件下加热并收集35-40℃馏分,产量为10.0g。
回答下列问题:
(1)根据实验药品的用量,制备溴乙烷时烧瓶的最适宜规格为
| A.50mL | B.100mL | C.150mL | D.250mL |
(3)图1中A为上口加有塞子的回流装置,其作用为
(4)溴乙烷的精制阶段,第一次分液应保留
(5)本实验溴乙烷的产率为
氯化氰(CNCl)是合成三聚氯氰的原料。氯化氰为无色液体,熔点-6.5℃,沸点12.5℃,遇水缓慢水解为氰酸和盐酸。现用氰化钠和氯气在四氯化碳(沸点为77℃)中反应制备氯化氰,反应式: 。反应装置如图所示。
。反应装置如图所示。
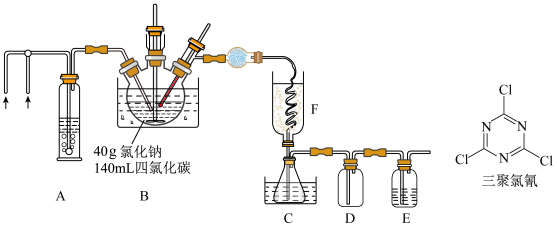
(1)仪器A的名称为___________ ;从实验装置角度分析本实验存在的缺陷___________ 。
(2)下列有关说法正确的是___________。
(3)反应结束后,简述将三颈烧瓶内残留的CNCl转移至装置C中的方法___________ 。
(4)氯化氰干燥后,在聚合塔中加热至400℃后便能得到氯化氰三聚物。测定三聚氯氰的含量的方法为蒸氨法。
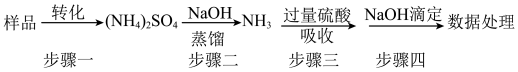
①为完成步骤二、三,选择必须的仪器,并按连接顺序排列(填写代表仪器的字母,不考虑夹持和橡皮管连接):热源→___________ 。
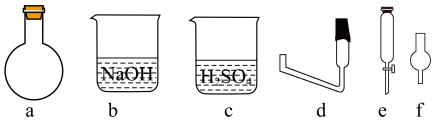
②若取mg样品,经步骤三中 吸收,滴定过程消耗
吸收,滴定过程消耗 溶液,计算样品中三聚氯氰的百分含量
溶液,计算样品中三聚氯氰的百分含量___________ (列出计算式)。

(1)仪器A的名称为
(2)下列有关说法正确的是___________。
| A.装置A中装饱和食盐水,装置E中装浓硫酸 |
| B.反应前需要通一段时间氮气,以排出装置内的氧气 |
| C.反应过程中,需要同时维持装置B、C、F在较低的温度 |
| D.装置D中出现黄绿色气体表明反应结束 |
(4)氯化氰干燥后,在聚合塔中加热至400℃后便能得到氯化氰三聚物。测定三聚氯氰的含量的方法为蒸氨法。

①为完成步骤二、三,选择必须的仪器,并按连接顺序排列(填写代表仪器的字母,不考虑夹持和橡皮管连接):热源→

②若取mg样品,经步骤三中
苯甲酸被广泛应用于合成药物、染料等化学品,某实验小组采用液相氧化法对其进行合成,有关药品性质及具体实验步骤如下:
【实验原理】
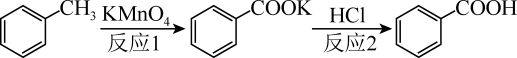
已知: 在弱酸、弱碱及中性条件下的还原产物为
在弱酸、弱碱及中性条件下的还原产物为 。
。
【药品性质】
【实验步骤】
(一)苯甲酸钾的制备
①烧瓶中加入 甲苯(
甲苯( )、
)、 (过量)、
(过量)、 蒸馏水及一小粒沸石,加热,保持回流状态直至__Ⅰ__为止,停止加热;
蒸馏水及一小粒沸石,加热,保持回流状态直至__Ⅰ__为止,停止加热;
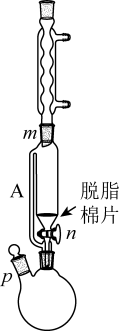
②向上述得到的悬浊液中加入适量的饱和 溶液,充分反应后,由m口加入图装置A中。将活塞n___Ⅱ___,进行过滤;
溶液,充分反应后,由m口加入图装置A中。将活塞n___Ⅱ___,进行过滤;
(二)苯甲酸的制备
③由p口向两颈烧瓶中加入一粒转子及 无水乙醇,m口装上球形冷凝管,加热搅拌回流
无水乙醇,m口装上球形冷凝管,加热搅拌回流 ,冷却后由p口加入
,冷却后由p口加入 浓盐酸,塞紧玻璃塞搅拌
浓盐酸,塞紧玻璃塞搅拌 后,将活塞n_______Ⅲ_______,浓缩两颈烧瓶中溶液至
后,将活塞n_______Ⅲ_______,浓缩两颈烧瓶中溶液至 左右;
左右;
④冷却溶液,开始析出白色片状的苯甲酸晶体,静置 后过滤,用_______Ⅳ_______淋洗晶体,干燥得晶体
后过滤,用_______Ⅳ_______淋洗晶体,干燥得晶体 。
。
请回答下列问题:
(1)能被 氧化为苯甲酸的苯的同系物在结构上应具备的条件是
氧化为苯甲酸的苯的同系物在结构上应具备的条件是_______ (填代号);
a.只有一个侧链
b.侧链不能有支链结构
c.侧链必须含有碳碳双键或碳碳三键等不饱和结构
d.与苯环直接相连的碳原子上连有氢原子
(2)装置A的名称为_______ ,此实验中装置A的侧管需用棉布缠绕,其目的是_______ ;
(3)步骤①中,可判断“反应1”结束的Ⅰ处的实验现象为_______ ;
(4)步骤②中加入饱和 溶液的目的是
溶液的目的是_______ ,请写出该过程的离子方程式_______ 。
(5)步骤②和③中,应对活塞n进行的操作是Ⅱ:_______ (填“关闭”或“打开”,后同),Ⅲ:_______ ;
(6)步骤③中,回流 的实验目的是
的实验目的是_______ ;
(7)步骤④中,IV处应选用的试剂为_______ (填代号);
a.乙醚 b. 乙醇 c.冷水 d.四氯化碳
乙醇 c.冷水 d.四氯化碳
(8)通过提供的数据计算,该实验的产率为_______ 。
【实验原理】

已知:
【药品性质】
| 药品 | 熔点(℃) | 沸点(℃) | 密度( | 溶解性 |
| 甲苯 | 110.6 | 0.872 | 难溶于水,与乙醇、乙醚等互溶 | |
| 苯甲酸 | 122.1 | 249.2 | 1.266 | 易溶于热水、乙醇、乙醚等溶剂,微溶于冷水 |
(一)苯甲酸钾的制备
①烧瓶中加入
②向上述得到的悬浊液中加入适量的饱和
(二)苯甲酸的制备
③由p口向两颈烧瓶中加入一粒转子及
④冷却溶液,开始析出白色片状的苯甲酸晶体,静置

请回答下列问题:
(1)能被
a.只有一个侧链
b.侧链不能有支链结构
c.侧链必须含有碳碳双键或碳碳三键等不饱和结构
d.与苯环直接相连的碳原子上连有氢原子
(2)装置A的名称为
(3)步骤①中,可判断“反应1”结束的Ⅰ处的实验现象为
(4)步骤②中加入饱和
(5)步骤②和③中,应对活塞n进行的操作是Ⅱ:
(6)步骤③中,回流
(7)步骤④中,IV处应选用的试剂为
a.乙醚 b.
(8)通过提供的数据计算,该实验的产率为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


