解答题-工业流程题 较难0.4 引用1 组卷251
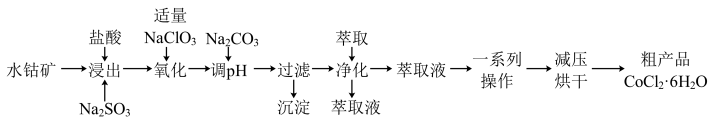
CoCl2·6H2O是一种饲料营养强化剂。一种利用水钴矿(主要成分为Co2O3、Co(OH)3,还含少量Fe2O3、Al2O3、MnO等)制取CoCl2·6H2O的工艺流程如下:
已知:①CoCl2·6H2O熔点为86℃,加热至110~120℃时,易分解。
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:(金属离子浓度为0.01mol/L)
(1)已知氧化性Co3+ >Fe3+,浸出液中含有的阳离子主要有H+、___________ 、Na+、Fe2+、Mn2+、Al3+等。
(2)在“氧化”步骤中,发生的主要离子反应方程式为___________ 。
(3)加Na2CO3调pH可得到两种沉淀,则pH最佳范围是___________ 。
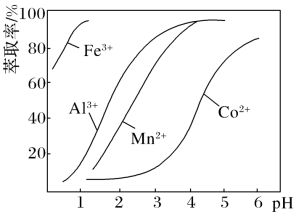
(4)已知萃取剂对金属离子的萃取率与pH的关系如图。控制溶液pH为3.0~3.5,则加入萃取剂的目的是除去___________ 。
(5)制得的CoCl2·6H2O在烘干时需减压烘干的原因是___________ 。为测定粗产品中CoCl2·6H2O含量,称取3.00 g的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量为2.87g,则粗产品中CoCl2·6H2O的质量分数为___________ (结果保留三位有效数字)。
(6)某同学用标准硝酸银溶液滴定未知浓度的CoCl2溶液,下列可作为指示剂的是___________(填选项,忽略亚钴离子的颜色干扰)。已知几种物质在20℃时的颜色及Ksp值如下表:

已知:①CoCl2·6H2O熔点为86℃,加热至110~120℃时,易分解。
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:(金属离子浓度为0.01mol/L)
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(2)在“氧化”步骤中,发生的主要离子反应方程式为
(3)加Na2CO3调pH可得到两种沉淀,则pH最佳范围是
(4)已知萃取剂对金属离子的萃取率与pH的关系如图。控制溶液pH为3.0~3.5,则加入萃取剂的目的是除去

(5)制得的CoCl2·6H2O在烘干时需减压烘干的原因是
(6)某同学用标准硝酸银溶液滴定未知浓度的CoCl2溶液,下列可作为指示剂的是___________(填选项,忽略亚钴离子的颜色干扰)。已知几种物质在20℃时的颜色及Ksp值如下表:
| 化学式 | AgCl | AgSCN | Ag2S | Ag2CrO4 |
| 颜色 | 白色 | 浅黄色 | 黑色 | 红色 |
| Ksp | 2.0×10-10 | 1.0×10-12 | 2.0 ×10-48 | 2.0×10-12 |
| A.KCl | B.KSCN | C.K2CrO4 | D.K2S |
2022·宁夏中卫·二模
类题推荐  是一种饲料营养强化剂。一种利用水钴矿
是一种饲料营养强化剂。一种利用水钴矿 主要成分为
主要成分为 、
、 ,还含少量
,还含少量 、
、 、MnO等
、MnO等 制取
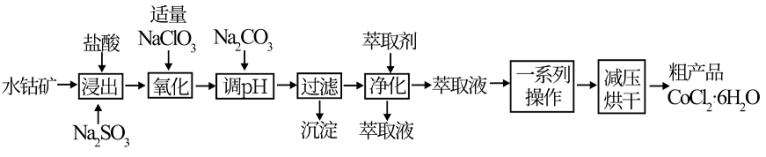
制取 的工艺流程如下:
的工艺流程如下:
已知:①部分阳离子以氢氧化物形式沉淀时溶液的pH见下表: 金属离子浓度为
金属离子浓度为 )
)
② 熔点为
熔点为 ,加热至
,加热至 时,失去结晶水生成无水氯化钴。
时,失去结晶水生成无水氯化钴。
(1)已知氧化性 ,浸出液中含有的阳离子主要有
,浸出液中含有的阳离子主要有 、
、_______ 、 、
、 、
、 等。
等。
(2)在“氧化”步骤中,发生的主要离子反应方程式为_______ 。
(3)加 调pH的最佳范围是
调pH的最佳范围是_______ ,过滤所得到的两种沉淀的化学式为_______ 。
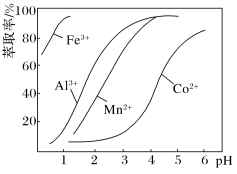
(4)萃取剂对金属离子的萃取率与pH的关系如图。控制溶液pH为 ,则加入萃取剂的目的是
,则加入萃取剂的目的是_______ 。
(5)“一系列操作”包含三个基本实验操作,它们是_______ 、_______ 和过滤。制得的 在烘干时需减压烘干的原因是
在烘干时需减压烘干的原因是_______ 。为测定粗产品中 含量,称取
含量,称取 的粗产品溶于水,加入足量
的粗产品溶于水,加入足量 溶液,过滤、洗涤,将沉淀烘干后称其质量为
溶液,过滤、洗涤,将沉淀烘干后称其质量为 ,则粗产品中
,则粗产品中 的质量分数为
的质量分数为_______  结果保留三位有效数字
结果保留三位有效数字 。经过检测,发现粗产品中含有NaCl杂质,则
。经过检测,发现粗产品中含有NaCl杂质,则 的质量分数可能比实际值
的质量分数可能比实际值_______  填“偏大”或“偏小”
填“偏大”或“偏小” 。
。
CoCl2·6H2O是一种饲料营养强化剂。一种利用水钴矿(主要成分为Co2O3、Co(OH)3,还含少量Fe2O3、Al2O3、MnO等)制取CoCl2·6H2O的工艺流程如下:
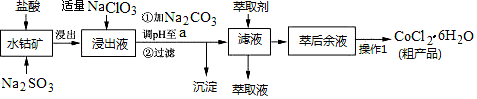
已知:①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:(金属离子浓度为:0.01mol/L)
③CoCl2·6H2O熔点为86℃,加热至110~120℃时,失去结晶水生成无水氯化钴。
(1)写出浸出过程中Co2O3发生反应的离子方程式______________ 。
(2)写出NaClO3发生反应的主要离子方程式______________ ;若不慎向“浸出液”中加过量NaClO3时,可能会生成有毒气体,写出生成该有毒气体的离子方程式_____________ 。
(3)“加Na2CO3调pH至a”,过滤所得到的两种沉淀的化学式为___________ 。
(4)制得的CoCl2·6H2O在烘干时需减压烘干的原因是__________________ 。
(5)萃取剂对金属离子的萃取率与pH的关系如图。向“滤液”中加入萃取剂的目的是_________ ;其使用的最佳pH范围是________________ 。
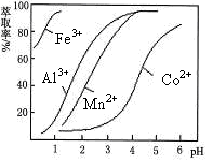
A.2.0~2.5 B.3.0~3.5 C.4.0~4.5 D.5.0~5.5
(6)为测定粗产品中CoCl2·6H2O含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量。通过计算发现粗产品中CoCl2·6H2O的质量分数大于100%,其原因可能是________________ 。(答一条即可)

已知:①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:(金属离子浓度为:0.01mol/L)
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
③CoCl2·6H2O熔点为86℃,加热至110~120℃时,失去结晶水生成无水氯化钴。
(1)写出浸出过程中Co2O3发生反应的离子方程式
(2)写出NaClO3发生反应的主要离子方程式
(3)“加Na2CO3调pH至a”,过滤所得到的两种沉淀的化学式为
(4)制得的CoCl2·6H2O在烘干时需减压烘干的原因是
(5)萃取剂对金属离子的萃取率与pH的关系如图。向“滤液”中加入萃取剂的目的是

A.2.0~2.5 B.3.0~3.5 C.4.0~4.5 D.5.0~5.5
(6)为测定粗产品中CoCl2·6H2O含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量。通过计算发现粗产品中CoCl2·6H2O的质量分数大于100%,其原因可能是
CoCl2· 6H2O是一种饲料营养强化剂。一种利用水钴矿(主要成分为Co2O3、 Co(OH)3,还含少量Fe2O3、Al2O3、MnO等)制取CoCl2· 6H2O的工艺流程如下:
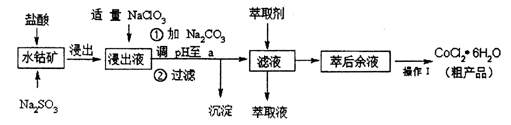
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表(金属离子浓度为0.01 mol/L):
③CoCl2· 6H2O熔点为86℃,加热至110~120℃时,失去结晶水生成无水氯化钴。
(1)写出浸出过程中主要发生的离子反应方程式:______________ 。
(2)若不慎向“浸出液”中加过量NaClO3时,可能会生成的有害气体是_______ (填化学式)。
(3)萃取剂对金属离子的萃取率与pH的关系如图,向“滤液”中加入萃取剂的目的是_______ ,其使用的最佳pH范围是 ________ (选填下列字母)。
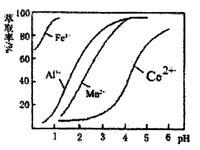
A. 2.0~2.5 B. 3.0~3.5 C. 4.0~4.5 D. 5.0~5.5
(4) “操作1”是________ 。制得的CoCl2· 6H2O需减压烘干的原因是__________ 。
(5)为测定粗产品中CoCl2· 6H2O的含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量。通过计算发现粗产品中CoCl2· 6H2O的质量分数大于100%,其原因可能是___________________ 。(答一条即可)

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表(金属离子浓度为0.01 mol/L):
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co (OH) 2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)写出浸出过程中主要发生的离子反应方程式:
(2)若不慎向“浸出液”中加过量NaClO3时,可能会生成的有害气体是
(3)萃取剂对金属离子的萃取率与pH的关系如图,向“滤液”中加入萃取剂的目的是

A. 2.0~2.5 B. 3.0~3.5 C. 4.0~4.5 D. 5.0~5.5
(4) “操作1”是
(5)为测定粗产品中CoCl2· 6H2O的含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量。通过计算发现粗产品中CoCl2· 6H2O的质量分数大于100%,其原因可能是

已知:①部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | |||||
| 开始沉淀 | |||||
| 完全沉淀 |
(1)已知氧化性
(2)在“氧化”步骤中,发生的主要离子反应方程式为
(3)加
(4)萃取剂对金属离子的萃取率与pH的关系如图。控制溶液pH为

(5)“一系列操作”包含三个基本实验操作,它们是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


