解答题-工业流程题 适中0.65 引用2 组卷243
工业上,处理低品位黄铜矿[二硫化亚铁铜(CuFeS2)含量较低]常采用生物堆浸法。堆浸所得的溶液可用于制备绿矾(FeSO4∙7H2O)和胆矾(CuSO4∙5H2O)。相关流程如下图。
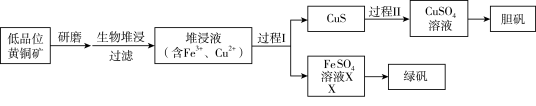
已知:①溶液中的c(H+)越大,pH越小,酸性越强。
②生物堆浸使用的氧化亚铁硫杆菌(T.f细菌)在pH1.0~6.0范围内可保持活性。
③溶液中pH很小时,金属通常以离子形式存在,随着pH增大,有些离子会形成氢氧化物沉淀(即使pH<7也可沉淀),不同离子形成沉淀时的pH如下表所示。
(1)生物堆浸过程的反应在T。f细菌的作用下进行,主要包括两个阶段,第一阶段是在T。f细菌作用下,将黄铜矿溶解,第二阶段为Fe2+继续被氧化转变成Fe3+。
①补全第一阶段反应的离子方程式(反应物已配平):_______ 。CuFeS2+4H++O2 =_______。
=_______。
②写出第二阶段反应的离子方程式:_______ 。
(2)结合已知推断:生物堆浸过程中,应控制溶液的pH在_______ 范围内。
(3)已知:CuS是一种难溶于水的黑色固体。过程II中,用H2O2和稀硫酸处理后,CuS完全溶解 ,用离子方程式表示H2O2的作用是_______ 。
(4)绿矾的纯度可通过其与KMnO4反应测定。取mg绿矾晶体,加适量稀硫酸溶解,与物质的量浓度为cmol/L的KMnO4溶液恰好反应时,消耗KMnO4溶液的体积为VmL。绿矾晶体质量分数的计算式为_______ 。(已知:FeSO4·7H2O摩尔质量为278g/mol)

已知:①溶液中的c(H+)越大,pH越小,酸性越强。
②生物堆浸使用的氧化亚铁硫杆菌(T.f细菌)在pH1.0~6.0范围内可保持活性。
③溶液中pH很小时,金属通常以离子形式存在,随着pH增大,有些离子会形成氢氧化物沉淀(即使pH<7也可沉淀),不同离子形成沉淀时的pH如下表所示。
| Fe3+ | Cu2+ | Fe2+ | |
| 开始沉淀时的pH | 1.5 | 4.2 | 6.3 |
| 完全沉淀时的pH | 2.8 | 6.7 | 8.3 |
①补全第一阶段反应的离子方程式(反应物已配平):
②写出第二阶段反应的离子方程式:
(2)结合已知推断:生物堆浸过程中,应控制溶液的pH在
(3)已知:CuS是一种难溶于水的黑色固体。过程II中,用H2O2和稀硫酸处理后,CuS
(4)绿矾的纯度可通过其与KMnO4反应测定。取mg绿矾晶体,加适量稀硫酸溶解,与物质的量浓度为cmol/L的KMnO4溶液恰好反应时,消耗KMnO4溶液的体积为VmL。绿矾晶体质量分数的计算式为
22-23高一下·北京海淀·开学考试
类题推荐
工业上,处理低品位黄铜矿[二硫化亚铁铜 含量较低]常采用生物堆浸法。堆浸所得的溶液可用于制备绿矾
含量较低]常采用生物堆浸法。堆浸所得的溶液可用于制备绿矾 和胆矾
和胆矾 。相关流程如下图。
。相关流程如下图。
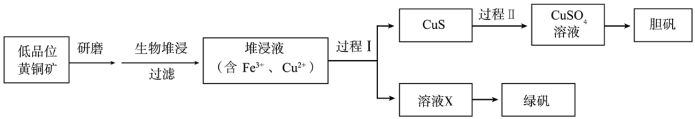
已知:①生物堆浸使用的氧化亚铁硫杆菌(T。f细菌)在pH 1.0~6.0范围内可保持活性。
②金属离子沉淀的pH如下表。
(1)生物堆浸前,需先将矿石进行研磨,目的是___________ 。
(2)生物堆浸过程的反应在T。f细菌的作用下进行,主要包括两个阶段,第一阶段的反应为:

第二阶段反应为 继续被氧化转变成
继续被氧化转变成 ,反应的离子方程式为
,反应的离子方程式为___________ 。
(3)结合已知推断:生物堆浸过程中,应控制溶液的pH在___________ 范围内。
(4)过程Ⅰ中,加入 固体还原堆浸液中的
固体还原堆浸液中的 ,得到溶液X。为判断堆浸液中
,得到溶液X。为判断堆浸液中 是否被还原完全,可取少量溶液X,向其中加入
是否被还原完全,可取少量溶液X,向其中加入___________ 试剂(填试剂的化学式),观察溶液颜色变化。
(5)过程Ⅱ中,用 和稀硫酸处理后,CuS
和稀硫酸处理后,CuS完全溶解 ,用离子方程式表示 的作用是
的作用是___________ 。
(6)绿矾的纯度可通过 滴定法测定。取m g绿矾晶体,加适量稀硫酸溶解。用物质的量浓度为c mol/L的
滴定法测定。取m g绿矾晶体,加适量稀硫酸溶解。用物质的量浓度为c mol/L的 溶液滴定。至恰好完全反应时,消耗
溶液滴定。至恰好完全反应时,消耗 溶液的体积为V mL。绿矾晶体质量分数的计算式为
溶液的体积为V mL。绿矾晶体质量分数的计算式为___________ 。(已知: 摩尔质量为278g/mol)
摩尔质量为278g/mol)
(7)用 晶体配制
晶体配制 溶液,放置一天后发现产生黄色固体。实验测定
溶液,放置一天后发现产生黄色固体。实验测定 溶液放置过程中溶液的pH和黄色固体的量的变化,结果如下:
溶液放置过程中溶液的pH和黄色固体的量的变化,结果如下:
分析黄色固体中除 、
、 还可能含有
还可能含有___________ 离子。

已知:①生物堆浸使用的氧化亚铁硫杆菌(T。f细菌)在pH 1.0~6.0范围内可保持活性。
②金属离子沉淀的pH如下表。
| 开始沉淀时的pH | 1.5 | 4.2 | 6.3 |
| 完全沉淀时的pH | 2.8 | 6.7 | 8.3 |
(2)生物堆浸过程的反应在T。f细菌的作用下进行,主要包括两个阶段,第一阶段的反应为:
第二阶段反应为
(3)结合已知推断:生物堆浸过程中,应控制溶液的pH在
(4)过程Ⅰ中,加入
(5)过程Ⅱ中,用
(6)绿矾的纯度可通过
(7)用
| 1小时 | 6小时 | 24小时 | |
| 溶液的pH | 2.39 | 2.35 | 1.40 |
| 黄色固体的量 | 几乎没有 | 少量 | 大量 |
工业上,处理低品位黄铜矿[二疏化亚铁铜(CuFS2)]常采用生物堆浸法。堆浸所得的溶液可用于制备绿矾(FeSO4·7H2O)和胆矾(CuSO4·5H2O)。相关流程如下图。
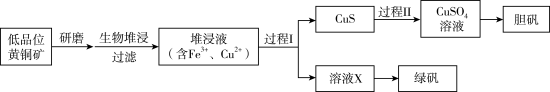
已知:①生物堆浸使用的氧化亚铁硫杆菌(T.f细菌)在pH1.0~6.0范围内可保持活性。
②金属离子沉淀的pH如下表。
(1)生物堆浸前,需先将矿石进行研磨,目的是________ 。
(2)生物堆浸过程的反应在T.f细菌的作用下进行,主要包括两个阶段,第一阶段的反应为: 。第二阶段反应为Fe2+继续被氧化转变成Fe3+,反应的离子方程式为
。第二阶段反应为Fe2+继续被氧化转变成Fe3+,反应的离子方程式为___________ 。
(3)结合已知推断:生物堆浸过程中,应控制溶液的pH在_____ 范围内。
(4)过程I中,加入Na2S2O3固体还原堆浸液中的Fe3+,得到溶液X。为判断堆浸液中Fe3+是否被还原完全,可取少量溶液X,向其中加入________ 试剂(填试剂的化学式),观察溶液颜色变化。
(5)过程Ⅱ中,用H2O2和稀硫酸处理后,CuS完全溶解,用离子方程式表示H2O2的作用是________ 。
(6)绿矾的纯度可通过KMnO4滴定法测定。取少量绿矾晶体,加适量稀硫酸溶解,配成100mL溶液。取20mL溶液,用物质的量浓度为cmo1/L的KMnO4溶液滴定,滴定终点的判定方法是_________ 。至恰好完全反应时,消耗KMnO4溶液的体积为VmL。则绿矾晶体物质的量为________ 。

已知:①生物堆浸使用的氧化亚铁硫杆菌(T.f细菌)在pH1.0~6.0范围内可保持活性。
②金属离子沉淀的pH如下表。
| Fe3+ | Cu2+ | Fe2+ | |
| 开始沉淀时的pH | 1.5 | 4.2 | 6.3 |
| 完全沉淀时的pH | 2.8 | 6.7 | 8.3 |
(2)生物堆浸过程的反应在T.f细菌的作用下进行,主要包括两个阶段,第一阶段的反应为:
(3)结合已知推断:生物堆浸过程中,应控制溶液的pH在
(4)过程I中,加入Na2S2O3固体还原堆浸液中的Fe3+,得到溶液X。为判断堆浸液中Fe3+是否被还原完全,可取少量溶液X,向其中加入
(5)过程Ⅱ中,用H2O2和稀硫酸处理后,CuS完全溶解,用离子方程式表示H2O2的作用是
(6)绿矾的纯度可通过KMnO4滴定法测定。取少量绿矾晶体,加适量稀硫酸溶解,配成100mL溶液。取20mL溶液,用物质的量浓度为cmo1/L的KMnO4溶液滴定,滴定终点的判定方法是
工业上,处理低品位黄铜矿[二硫化亚铁铜( )]常采用生物堆浸法。堆浸所得的溶液可用于制备绿矾(
)]常采用生物堆浸法。堆浸所得的溶液可用于制备绿矾( )和胆矾(
)和胆矾( )。相关流程如下图。
)。相关流程如下图。 1.0~6.0范围内可保持活性。
1.0~6.0范围内可保持活性。
②金属离子沉淀的pH如下表。
(1)Cu2+价电子轨道表示式为___________ ,生物堆浸前,需先将矿石进行研磨,目的是___________ 。
(2)生物堆浸过程的反应在T。f细菌的作用下进行,主要包括两个阶段,第一阶段的反应为: 。第二阶段反应为
。第二阶段反应为 继续被氧化转变成
继续被氧化转变成 ,反应的离子方程式为
,反应的离子方程式为___________ 。
(3)结合已知推断:生物堆浸过程中,应控制溶液的 在
在___________ 范围内。
(4)过程Ⅰ中,加入 固体还原堆浸液中的
固体还原堆浸液中的 ,得到溶液X。为判断堆浸液中
,得到溶液X。为判断堆浸液中 是否被还原完全,可取少量溶液X,向其中加入
是否被还原完全,可取少量溶液X,向其中加入___________ ,说明Fe3+已被完全还原。
(5)过程Ⅱ中,用 和稀硫酸处理后,
和稀硫酸处理后,
完全溶解 ,用离子方程式表示 的作用是
的作用是___________ 。
(6)绿矾的纯度可通过 滴定法测定。取
滴定法测定。取 绿矾晶体,加适量稀硫酸溶解。用物质的量浓度为cmol/L的
绿矾晶体,加适量稀硫酸溶解。用物质的量浓度为cmol/L的 溶液滴定,滴定终点的判定方法是
溶液滴定,滴定终点的判定方法是___________ 。至恰好完全反应时,消耗 溶液的体积为
溶液的体积为 。绿矾晶体质量分数的计算式为
。绿矾晶体质量分数的计算式为___________ 。
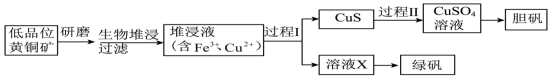
②金属离子沉淀的pH如下表。
| Fe3+ | Cu2+ | Fe2+ | |
| 开始沉淀时的pH | 1.5 | 4.2 | 6.3 |
| 完全沉淀时的pH | 2.8 | 6.7 | 8.3 |
(2)生物堆浸过程的反应在T。f细菌的作用下进行,主要包括两个阶段,第一阶段的反应为:
(3)结合已知推断:生物堆浸过程中,应控制溶液的
(4)过程Ⅰ中,加入
(5)过程Ⅱ中,用
(6)绿矾的纯度可通过
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


