解答题-实验探究题 适中0.65 引用2 组卷538
乙二酸俗称草酸( ),是一种二元弱酸,易溶于水,具有还原性。25℃时,
),是一种二元弱酸,易溶于水,具有还原性。25℃时, 的电离平衡常数
的电离平衡常数 ,
, 。
。
Ⅰ.学习小组甲用酸性 标准溶液滴定未知浓度的草酸溶液。
标准溶液滴定未知浓度的草酸溶液。
(1) 中C元素的化合价是
中C元素的化合价是___________ ,写出 的电离方程式
的电离方程式___________ 。
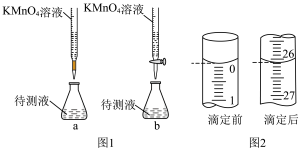
(2)某学生的滴定方式(夹持部分略去)如图1所示,合理的是___________ (填“a”或“b”),由图2可知消耗 溶液体积为
溶液体积为___________ mL,若滴定终点时俯视滴定管刻度读数,则由此测得的草酸溶液的物质的量浓度会___________ (填“偏大”“偏小”或“不变”)。
Ⅱ.学习小组乙查阅文献获得以下信息:
①三水三草酸合铁酸钾[ ]为翠绿色晶体,光照易分解,
]为翠绿色晶体,光照易分解, 是一种稳定的配离子,能类似于
是一种稳定的配离子,能类似于 中的
中的 在溶液中稳定存在。
在溶液中稳定存在。 和
和 存在如下平衡:
存在如下平衡:
ⅰ.

ⅱ.

②相同条件下,草酸根(C2O )的还原性强于
)的还原性强于
③ 为黄色固体,微溶于水,可溶于强酸
为黄色固体,微溶于水,可溶于强酸
【实验】探究Fe3+和草酸根在溶液中的反应。
(3)取实验中少量晶体洗净,配成溶液,滴加KSCN溶液,不变红,原因是___________ (结合ⅰ、ⅱ平衡,用必要的化学用语和数据解释原因),继续加入硫酸,溶液变红,说明加入硫酸, 与
与 结合使ⅱ平衡
结合使ⅱ平衡___________ 移动(填“正向”或“逆向”)。经检验发现上述实验中 和
和 未发生氧化还原反应。
未发生氧化还原反应。
(4)取实验中少量的翠绿色溶液于试管中光照一段时间,产生黄色沉淀和气泡,反应的离子方程式为 ,用单线桥法表示该反应中的电子转移情况。
,用单线桥法表示该反应中的电子转移情况。__________
(5)写出一种利用盐类水解原理在生产或生活中应用的实例___________ 。
Ⅰ.学习小组甲用酸性
(1)
(2)某学生的滴定方式(夹持部分略去)如图1所示,合理的是

Ⅱ.学习小组乙查阅文献获得以下信息:
①三水三草酸合铁酸钾[
ⅰ.
ⅱ.
②相同条件下,草酸根(C2O
③
【实验】探究Fe3+和草酸根在溶液中的反应。
| 操作 | 现象 |
| 在避光处,向10mL 0.5 | 得到翠绿色溶液和翠绿色晶体 |
(4)取实验中少量的翠绿色溶液于试管中光照一段时间,产生黄色沉淀和气泡,反应的离子方程式为
(5)写出一种利用盐类水解原理在生产或生活中应用的实例
2023·广东梅州·模拟预测
类题推荐
某化学兴趣小组为了探究在相同条件下,草酸根( )的还原性是否强于
)的还原性是否强于 ,进行了如下三个实验。
,进行了如下三个实验。
【实验1】通过 和
和 在溶液中的反应比较
在溶液中的反应比较 和
和 的还原性强弱。实验操作与现象如下:
的还原性强弱。实验操作与现象如下:
在避光处,向 溶液中缓慢加入
溶液中缓慢加入 溶液至过量,搅拌,充分反应后,冰水浴冷却,过滤后得到翠绿色溶液和翠绿色晶体,并留存翠绿色溶液a待用。
溶液至过量,搅拌,充分反应后,冰水浴冷却,过滤后得到翠绿色溶液和翠绿色晶体,并留存翠绿色溶液a待用。
已知:Ⅰ.草酸 ( )为二元弱酸。
)为二元弱酸。
Ⅱ.三水三草酸合铁酸钾[ ]为翠绿色晶体,光照易分解。其水溶液中存在:
]为翠绿色晶体,光照易分解。其水溶液中存在:
 请回答:
请回答:
(1)实验室配制 溶液时若不加盐酸一起进行配制,常常得到红褐色的溶液,请用离子方程式说明原因
溶液时若不加盐酸一起进行配制,常常得到红褐色的溶液,请用离子方程式说明原因_______ 。
(2)取实验1中少量晶体洗净,配成溶液,滴加KSCN溶液,不变红。继续加入硫酸,溶液变红,说明晶体中含有+3价的铁元素。加硫酸后溶液变红的原因是_______ 。
(3)经检验,翠绿色晶体为 。为了确认实验1中是否发生了氧化还原反应,取少量翠绿色溶液a,向其中滴加
。为了确认实验1中是否发生了氧化还原反应,取少量翠绿色溶液a,向其中滴加_______ (填序号)未见明显现象。
A.少量KSCN溶液 B.少量 溶液 C.少量HCl溶液
溶液 C.少量HCl溶液
该小组据此判断氧化还原没有发生。请简述未发生氧化还原反应的原因_______ 。
【实验2】通过比较 与
与 、
、 反应的难易,判断二者还原性的强弱。实验操作与现象如下:
反应的难易,判断二者还原性的强弱。实验操作与现象如下:
①向 溶液中加入
溶液中加入 溶液,过滤,立即产生黄色沉淀;
溶液,过滤,立即产生黄色沉淀;
②洗涤①中的黄色沉淀(已知: 为黄色固体,微溶于水,可溶于强酸),向其中加入过量的
为黄色固体,微溶于水,可溶于强酸),向其中加入过量的 溶液,振荡,静置,反应剧烈放热,产生大量的红褐色沉淀和无色气体;
溶液,振荡,静置,反应剧烈放热,产生大量的红褐色沉淀和无色气体;
③待充分反应后,向其中加入稀硫酸,调节pH约为4,得到翠绿色溶液。请回答:
(4)证明 被氧化的实验现象是
被氧化的实验现象是_______ 。
(5)以上现象能否说明 没有被氧化。请判断并说明理由:
没有被氧化。请判断并说明理由:_______ 。
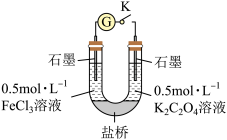
【实验3】利用电化学装置进行实验,其装置如图:

(6)用 溶液、
溶液、 溶液和其他试剂,设计图的装置进行实验比较
溶液和其他试剂,设计图的装置进行实验比较 和
和 的还原性强弱,一段时间的实验后,该小组依据实验所观察到的现象做出了
的还原性强弱,一段时间的实验后,该小组依据实验所观察到的现象做出了 比
比 还原性强的实验结论。则下列实验现象描述能支持这一结论的有:_______。(填序号)
还原性强的实验结论。则下列实验现象描述能支持这一结论的有:_______。(填序号)
【实验1】通过
在避光处,向
已知:Ⅰ.草酸 (
Ⅱ.三水三草酸合铁酸钾[
(1)实验室配制
(2)取实验1中少量晶体洗净,配成溶液,滴加KSCN溶液,不变红。继续加入硫酸,溶液变红,说明晶体中含有+3价的铁元素。加硫酸后溶液变红的原因是
(3)经检验,翠绿色晶体为
A.少量KSCN溶液 B.少量
该小组据此判断氧化还原没有发生。请简述未发生氧化还原反应的原因
【实验2】通过比较
①向
②洗涤①中的黄色沉淀(已知:
③待充分反应后,向其中加入稀硫酸,调节pH约为4,得到翠绿色溶液。请回答:
(4)证明
(5)以上现象能否说明
【实验3】利用电化学装置进行实验,其装置如图:

(6)用
| A.电流表指针发生偏转 |
| B.取左侧烧杯内溶液滴加氢氧化钠溶液,出现红褐色沉淀 |
| C.取左侧烧杯内溶液滴加 |
| D.右侧烧杯的电极附近有无色气泡生成,经实验,该气体能使澄清石灰水变浑浊。 |
盐酸和草酸是生活中常见的酸,回答下列问题:
Ⅰ.某学生用0.2000mol/L的标准NaOH溶液滴定未知浓度的盐酸,操作如下:
a.用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上;
b.固定好滴定管并使滴定管尖嘴处充满液体;
c.调节液面至“0”或“0”刻度线以下,并记下读数;
d.移取20.00L待测液注入洁净的存有少量蒸馏水的锥形瓶中,并加入3滴酚酞溶液;
e.用标准液滴定至终点,记下滴定管液面读数。
(1)以上步骤中有错误的是___________ (填字母)。
(2)该同学将中和滴定原理应用到葡萄酒中抗氧化剂残留量(以游离 计算)的测定中:
计算)的测定中:
准确量取100.00L葡萄酒样品,加酸蒸馏出抗氧化剂成分,取馏分于锥形瓶中,滴加少量淀粉溶液,用0.0100mo/L标准 溶液滴定至终点,重复操作三次,平均消耗标准溶液22.50mL。(已知滴定过程中所发生的反应是
溶液滴定至终点,重复操作三次,平均消耗标准溶液22.50mL。(已知滴定过程中所发生的反应是 )
)
①滴定前需排放装有标准溶液的滴定管尖嘴处的气泡,其正确的图示为___________ (填字母)。
A. B.
B. 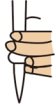 C.
C. 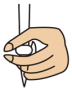 D.
D.
②判断达到滴定终点的依据是___________ ;所测100.00mL葡萄酒样品中抗氧化剂的残留量为___________ mg/L。
Ⅱ.已知常温下的电离平衡常数 ,某化学小组研究草酸
,某化学小组研究草酸 及其盐的性质。
及其盐的性质。
(3) 中
中 的杂化类型是
的杂化类型是___________ 。
(4)常温下, 溶液中各离子浓度由大到小的顺序为
溶液中各离子浓度由大到小的顺序为___________ 。
(5)下列 溶液中离子浓度的关系不正确的是
溶液中离子浓度的关系不正确的是___________ (填字母)。
A.
B.
C.
(6)探究 和
和 在溶液中的反应。
在溶液中的反应。
【资料】i.三水三草酸合铁酸钾 为翠绿色晶体,光照易分解,其水溶液中存在:
为翠绿色晶体,光照易分解,其水溶液中存在: 。
。
ii.
 。
。
进行如下实验:
经检验,上述实验中 和
和 未发生氧化还原反应。
未发生氧化还原反应。
取实验中少量晶体洗净,配成溶液波,滴加 溶液,不变红,原因是
溶液,不变红,原因是___________ (结合资料,用必要的化学用语和数据解释原因),继续加入硫酸,溶液变红,说明加入硫酸, 与
与 结合使反应
结合使反应 平衡
平衡___________ (填“正向”或“逆向”)移动。
(7)设计实验证明草酸的酸性比碳酸强:___________ 。
Ⅰ.某学生用0.2000mol/L的标准NaOH溶液滴定未知浓度的盐酸,操作如下:
a.用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上;
b.固定好滴定管并使滴定管尖嘴处充满液体;
c.调节液面至“0”或“0”刻度线以下,并记下读数;
d.移取20.00L待测液注入洁净的存有少量蒸馏水的锥形瓶中,并加入3滴酚酞溶液;
e.用标准液滴定至终点,记下滴定管液面读数。
(1)以上步骤中有错误的是
(2)该同学将中和滴定原理应用到葡萄酒中抗氧化剂残留量(以游离
准确量取100.00L葡萄酒样品,加酸蒸馏出抗氧化剂成分,取馏分于锥形瓶中,滴加少量淀粉溶液,用0.0100mo/L标准
①滴定前需排放装有标准溶液的滴定管尖嘴处的气泡,其正确的图示为
A.
 B.
B.  C.
C.  D.
D.
②判断达到滴定终点的依据是
Ⅱ.已知常温下的电离平衡常数
(3)
(4)常温下,
(5)下列
A.
B.
C.
(6)探究
【资料】i.三水三草酸合铁酸钾
ii.
进行如下实验:
| 操作 | 现象 |
| 在避光处,向 | 得到翠绿色溶液和翠绿色晶体 |
取实验中少量晶体洗净,配成溶液波,滴加
(7)设计实验证明草酸的酸性比碳酸强:
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网