解答题-工业流程题 较难0.4 引用2 组卷698
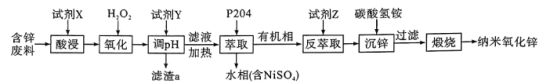
纳米氧化锌是一种多功能性新型无机材料,化工上可以利用废弃的锌镍电池废料(主要含:Zn、Ni和少量的Fe、Al)制备纳米氧化锌,其生产流程如图所示:
已知:Ksp[Zn(OH)2]=1.6×10-16;Ksp[Ni(OH)2]=2.8×10-15;Ksp[Fe(OH)3]=2.7×10-39;Ksp[Al(OH)3 =4.6×10-33
回答下列问题:
(1)H2SO4属于高沸点的酸,不仅是因为H2SO4分子属于极性分子,另外一个主要原是___________ 。
(2)为检验“氧化”操作后的溶液中是否含有Fe2+,某同学取适量待检溶液,滴加酸性高锰酸钾溶液该方法是否合理:___________ (填“是”或“否”),理由是___________ (以离子方程式表示)。
(3)“沉铁铝”操作中加热不仅能够加快反应速率,另外一个主要目的是___________ 取“沉铁铝”操作所得的沉淀物置于1.0L水中室温下充分溶解,其中沉淀物中若含有5.6gFe(OH)3最终所得溶液中c(Fe3+)=___________ mol/L。
(4)假定萃取达到平衡时,样品在水和萃取剂中的总浓度比为1:80,若在50mL的水溶液样品中用10mL萃取剂P204萃取,则萃取后溶液中残留的样品浓度为原溶液的___________ 倍。
(5)化工生产中,分离Zn2+离子用萃取法而不通过调节溶液pH形成沉淀的方法,原因是___________ 。
(6)“沉锌”过程中若NH4HCO3用量过大,易生成碱式碳酸锌[2Zn(OH)2·ZnCO3·2H2O]沉淀,该反应的离子方程式为___________ 。

已知:Ksp[Zn(OH)2]=1.6×10-16;Ksp[Ni(OH)2]=2.8×10-15;Ksp[Fe(OH)3]=2.7×10-39;Ksp[Al(OH)3 =4.6×10-33
回答下列问题:
(1)H2SO4属于高沸点的酸,不仅是因为H2SO4分子属于极性分子,另外一个主要原是
(2)为检验“氧化”操作后的溶液中是否含有Fe2+,某同学取适量待检溶液,滴加酸性高锰酸钾溶液该方法是否合理:
(3)“沉铁铝”操作中加热不仅能够加快反应速率,另外一个主要目的是
(4)假定萃取达到平衡时,样品在水和萃取剂中的总浓度比为1:80,若在50mL的水溶液样品中用10mL萃取剂P204萃取,则萃取后溶液中残留的样品浓度为原溶液的
(5)化工生产中,分离Zn2+离子用萃取法而不通过调节溶液pH形成沉淀的方法,原因是
(6)“沉锌”过程中若NH4HCO3用量过大,易生成碱式碳酸锌[2Zn(OH)2·ZnCO3·2H2O]沉淀,该反应的离子方程式为
2023·安徽宿州·一模
类题推荐
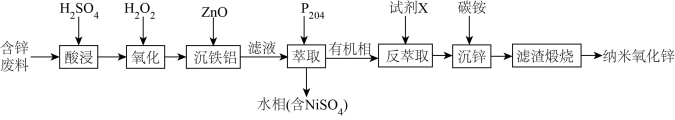
纳米氧化锌是一种多功能性新型无机材料,化工上可以利用废弃的锌镍电池废料(主要含Zn、Ni和少量的Fe、Al)制备纳米氧化锌,其生产流程如图所示:

已知: ;
; ;
; ;
; 。回答下列问题:
。回答下列问题:
(1)调pH加入的X可能是___________。
(2)为检验“氧化”操作后的溶液中是否含有 ,某同学取适量待检溶液,滴加酸性高锰酸钾溶液。该方法是否合理:
,某同学取适量待检溶液,滴加酸性高锰酸钾溶液。该方法是否合理:___________ (填“是”或“否”),理由是___________ (以离子方程式表示)。
(3)假定萃取达到平衡时,样品在水和萃取剂中的总浓度比为 ,若在
,若在 的水溶液样品中用
的水溶液样品中用 磷酸酯萃取剂(P204)萃取,则萃取后溶液中残留的样品浓度为原溶液的
磷酸酯萃取剂(P204)萃取,则萃取后溶液中残留的样品浓度为原溶液的___________ %(保留两位有效数字)。
(4)化工生产中,分离 离子用萃取法而不通过调节溶液pH形成沉淀的方法,原因是
离子用萃取法而不通过调节溶液pH形成沉淀的方法,原因是___________ 。
(5)“沉锌”得到碱式碳酸锌,化学式为 。
。
①“沉锌”的离子方程式为___________ 。
②碱式碳酸锌加热升温过程中固体的质量变化如图所示。350℃时,剩余固体中已不含碳元素,此时剩余固体的成分及物质的量之比是___________ 。


已知:
(1)调pH加入的X可能是___________。
| A. | B. | C. | D. |
(3)假定萃取达到平衡时,样品在水和萃取剂中的总浓度比为
(4)化工生产中,分离
(5)“沉锌”得到碱式碳酸锌,化学式为
①“沉锌”的离子方程式为
②碱式碳酸锌加热升温过程中固体的质量变化如图所示。350℃时,剩余固体中已不含碳元素,此时剩余固体的成分及物质的量之比是

镍及其化合物在工业上有广泛用途,以某地红土镍矿(主要成分NiO、MgO、Al2O3、SiO2和铁的氧化物为原料,采用酸溶法制取硫酸镍和MgSO4●7H2O,工业流程如图所示。
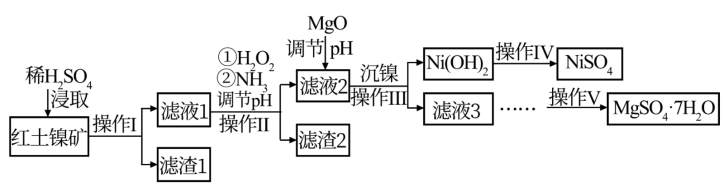
已知:①常温下,NiSO4易溶于水,Ni(OH)2和NiOOH不溶于水,已知Ksp[Ni(OH)2]=1.0×10-15。
②在上述流程中,某些金属离子开始沉淀和沉淀完全时的pH如下:
回答下列问题:
(1)“浸取”时需将矿样研磨的目的是___________ ,“滤渣1”的成分___________ (填化学式)。
(2)滤液1中加入H2O2的作用___________ (用反应离子方程式表示)。
(3)操作II为达到实验目的,由表中的数据判断通入NH3调节溶液pH的范围是___________
(4)“滤液1”中是否存在Fe3+,可用___________ (填试剂名称) 检验,检验存在Fe3+的实验方法是___________ 。
(5)“沉镍”中pH调为8.5,则滤液中Ni2+的浓度为___________ mol·L-1
(6)操作V是___________ 、过滤、洗涤。
(7)NiSO4在碱性溶液中用NaClO氧化,可制得碱性镍镉电池电极材料NiOOH,该反应的离子方程式___________ 。

已知:①常温下,NiSO4易溶于水,Ni(OH)2和NiOOH不溶于水,已知Ksp[Ni(OH)2]=1.0×10-15。
②在上述流程中,某些金属离子开始沉淀和沉淀完全时的pH如下:
| 沉淀物 | Ni(OH)2 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀时的pH | 7.1 | 7.6 | 2.7 | 3.4 | 9.2 |
| 沉淀完全(c=1x10-5)时的pH | 9.0 | 9.6 | 3.2 | 4.7 | 11.1 |
回答下列问题:
(1)“浸取”时需将矿样研磨的目的是
(2)滤液1中加入H2O2的作用
(3)操作II为达到实验目的,由表中的数据判断通入NH3调节溶液pH的范围是
(4)“滤液1”中是否存在Fe3+,可用
(5)“沉镍”中pH调为8.5,则滤液中Ni2+的浓度为
(6)操作V是
(7)NiSO4在碱性溶液中用NaClO氧化,可制得碱性镍镉电池电极材料NiOOH,该反应的离子方程式
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网