解答题-实验探究题 适中0.65 引用1 组卷134
天然气中常混有 ,现用如下方法测定天然气中
,现用如下方法测定天然气中 的含量。反应中涉及的方程式有:
的含量。反应中涉及的方程式有:
①
②
③
(1)反应①中, 体现
体现_______ (选填“酸性”“氧化性”或“还原性”)。
采用以下方法测定 的含量。
的含量。
步骤I:将1L天然气中的 溶于水并进行反应①,配制成500mL溶液。
溶于水并进行反应①,配制成500mL溶液。
步骤II:加入0.001mol的I2(过量)使ZnS完全转化为ZnI2,加入淀粉溶液作为指示剂,用0.1mol·L-1的 滴定过量的I2,做几组平行实验,平均消耗15.00mL。
滴定过量的I2,做几组平行实验,平均消耗15.00mL。
(2)①滴定达到终点的现象为:溶液由_______ 色变_______ 色,且半分钟不恢复原色。
②根据条件计算天然气中H2S的含量为_______ mg·L-1。
③若在步骤I收集H2S的过程中,有少量硫化氢进入 溶液中,则测得H2S的含量
溶液中,则测得H2S的含量_______ (选填“偏高”“偏低”或“无影响”)。
(3)假设在反应②中,碘单质全部转化为易溶于水的ZnI2,如何检验体系中的I-_______ 。
(4)利用硫碘循环处理H2S的方法如图所示:
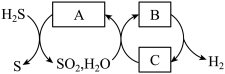
写出上述流程中A、B、C的化学式。
A:_______ ;B:_______ ;C:_______ 。
①
②
③
(1)反应①中,
采用以下方法测定
步骤I:将1L天然气中的

步骤II:加入0.001mol的I2(过量)使ZnS完全转化为ZnI2,加入淀粉溶液作为指示剂,用0.1mol·L-1的
(2)①滴定达到终点的现象为:溶液由
②根据条件计算天然气中H2S的含量为
③若在步骤I收集H2S的过程中,有少量硫化氢进入
(3)假设在反应②中,碘单质全部转化为易溶于水的ZnI2,如何检验体系中的I-
(4)利用硫碘循环处理H2S的方法如图所示:

写出上述流程中A、B、C的化学式。
A:
2022高二·上海·学业考试
类题推荐
某小组在实验室中探究Cl2与Na2S样品(Na2S杂质不参与化学反应,且能溶于水)的反应。回答下列问题:
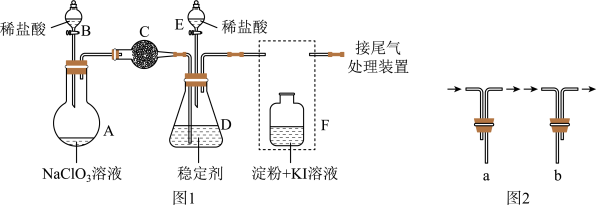
I. Cl2的制备

①装置A中发生反应的离子方程式为_______ 。
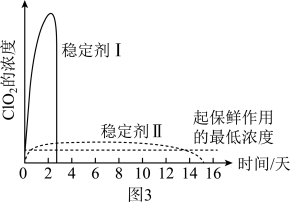
②欲收集干燥的Cl2,则图中装置的连接顺序为a→_______ (按照气流方向,填小写字母)
II.Cl2与Na2S的反应
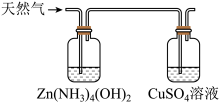
将上述收集到的Cl2通入下图所示装置中,充分反应,得到黄色浑浊溶液。
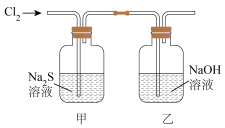
一段时间后,将甲中浑浊溶液过滤,取滤液进行下列实验,探究甲中反应的产物。
③根据以上探究结果,请写出Cl2与Na2S反应的离子方程式:_______ 。
III. Na2S中S2-的含量可以用“碘量法”测得。称量a g Na2S样品,置于碘量瓶中,接着移取50 mL 0.100 mol/L的I2-KI溶液于其中,往碘量瓶中加入乙酸溶液,密闭,置黑暗处反应5min,有单质S析出。以淀粉溶液为指示剂,过量的I2用0.10mol/L的Na2S2O3溶液滴定,反应式为I2+2 =2I-+
=2I-+ 。测定时消耗Na2S2O3溶液的体积为V mL。终点颜色变化为
。测定时消耗Na2S2O3溶液的体积为V mL。终点颜色变化为_______ ,样品中S2-的含量为_______ (写出表达式)。
I. Cl2的制备

①装置A中发生反应的离子方程式为
②欲收集干燥的Cl2,则图中装置的连接顺序为a→
II.Cl2与Na2S的反应
将上述收集到的Cl2通入下图所示装置中,充分反应,得到黄色浑浊溶液。

一段时间后,将甲中浑浊溶液过滤,取滤液进行下列实验,探究甲中反应的产物。
操作步骤 | 实验现象 | 结论 |
| 取少量滤液于试管A中,加入Ba(OH)2溶液,振荡 | ① | 有硫酸根离子生成 |
| 另取少量滤液于试管B中,滴加品红溶液和盐酸 | 品红溶液不褪色 | ②无 |
III. Na2S中S2-的含量可以用“碘量法”测得。称量a g Na2S样品,置于碘量瓶中,接着移取50 mL 0.100 mol/L的I2-KI溶液于其中,往碘量瓶中加入乙酸溶液,密闭,置黑暗处反应5min,有单质S析出。以淀粉溶液为指示剂,过量的I2用0.10mol/L的Na2S2O3溶液滴定,反应式为I2+2
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网