解答题-实验探究题 适中0.65 引用1 组卷163
化学为人类日常生活提供了很多便利,氯及其化合物在人类的生活中占有重要地位。回答下列问题:
Ⅰ.如图是氯元素的“价类二维图”。
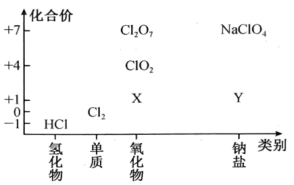
(1)X的化学式为______ ;Cl2O7为______ (填“酸性”“碱性”或“两性”)氧化物。
(2)巴西奥运会期间,由于工作人员将以Y为有效成分的消毒液与双氧水混用,导致游泳池藻类快速生长,其反应的化学方程式为______ 。
(3)下列物质常用于杀菌消毒,其中消毒原理与HClO相同的是______ (填字母)。
Ⅱ.某实验小组用如图装置制备Cl2,并验证Cl2的部分性质。
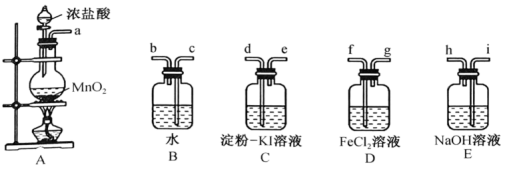
(4)盛放浓盐酸的仪器名称为_____ ,写出制备氯气的化学方程式:_____ 。
(5)根据装置C中淀粉-KI溶液变蓝可验证非金属性:Cl_____ (填“>”“<”或“=”)I。
(6)装置D中的实验现象为_____ ,说明Cl2具有氧化性;实验中未被反应的Cl2用装置E吸收,g应连接_____ (填“h”或“i”)口。
(7)该实验小组利用上述装置B中的新制氯水进行如图实验。
探究丙中的褪色原因,该实验小组同学提出两种假设:a.铁离子被氧化;b.SCN-被氧化。
①取两支试管分别加入褪色后的溶液,滴加0.1mol∙L-1的FeCl3溶液和KSCN溶液各1滴,观察到_____ 现象,得出结论:假设b成立。
②进一步预测SCN-可能被转化为 ,通过实验验证了该预测,写出实验操作及现象:
,通过实验验证了该预测,写出实验操作及现象:______ 。
Ⅰ.如图是氯元素的“价类二维图”。

(1)X的化学式为
(2)巴西奥运会期间,由于工作人员将以Y为有效成分的消毒液与双氧水混用,导致游泳池藻类快速生长,其反应的化学方程式为
(3)下列物质常用于杀菌消毒,其中消毒原理与HClO相同的是
| A.O3 | B.酒精 | C.熟石灰 | D.KMnO4 |
Ⅱ.某实验小组用如图装置制备Cl2,并验证Cl2的部分性质。

(4)盛放浓盐酸的仪器名称为
(5)根据装置C中淀粉-KI溶液变蓝可验证非金属性:Cl
(6)装置D中的实验现象为
(7)该实验小组利用上述装置B中的新制氯水进行如图实验。
| 操作 | 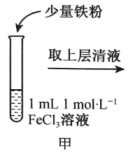 | 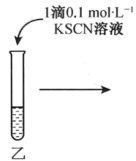 | 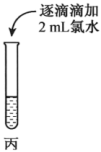 |
| 现象 | 溶液由棕黄色变为浅绿色 | 无明显现象 | 溶液变为红色,而后红色褪去 |
①取两支试管分别加入褪色后的溶液,滴加0.1mol∙L-1的FeCl3溶液和KSCN溶液各1滴,观察到
②进一步预测SCN-可能被转化为
22-23高一下·河南·阶段练习
类题推荐
某小组同学分别探究FeCl2溶液、FeCl3溶液的性质。
I.探究FeCl2溶液的性质。
(1)从物质类别角度判断FeCl2属于___________ ,因此可以与某些碱反应。
(2)预测FeCl2具有氧化性,因此可以与Zn反应,此时Zn体现___________ 性。
(3)预测FeCl2具有还原性,预测依据是___________ ,因此可以与酸性KMnO4溶液反应。
(4)进行如下实验操作:
①i中的现象是___________ ,用化学方程式表示产生该现象的原因:___________ 、___________ 。
②ii中反应的离子方程式是___________ 。
③iii中的现象是___________ 。
(5)某同学认为iii中现象并不能证明Fe2+具有还原性,他的理由有二:①将酸性高锰酸钾稀释也可能产生该现象、②___________ , 为证实该反应中Fe2+确实被氧化,需要在反应后的溶液中加入试剂___________ ,观察到现象___________ 。
II.探究FeCl3溶液的性质。
小组同学进行如下实验操作并观察到对应现象:
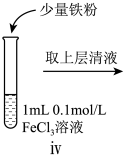
(6)iv中反应的离子方程式是___________ 。
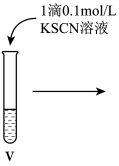
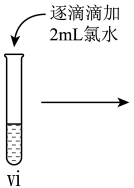
(7)vi 中滴加氯水过程中,氯水反应的离子方程式是___________ 。
III.小组同学探究vi中褪色原因,提出两种假设: a.铁离子被转化,b. SCN被转化。
(8)分别向褪色后的溶液中滴加0.1 mol/L FeCl3溶液和KSCN溶液各1滴,观察到___________ 现象,得出结论:假设b成立。
(9)进一步预测SCN-可能被转化为SO ,通过实验验证了该预测,写出实验操作及现象
,通过实验验证了该预测,写出实验操作及现象___________ 。
I.探究FeCl2溶液的性质。
(1)从物质类别角度判断FeCl2属于
(2)预测FeCl2具有氧化性,因此可以与Zn反应,此时Zn体现
(3)预测FeCl2具有还原性,预测依据是
(4)进行如下实验操作:
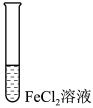 | 序号 | 操作 |
| i | 滴加NaOH溶液 | |
| ii | 加入少量锌粉 | |
| iii | 滴加酸性KMnO4溶液 |
②ii中反应的离子方程式是
③iii中的现象是
(5)某同学认为iii中现象并不能证明Fe2+具有还原性,他的理由有二:①将酸性高锰酸钾稀释也可能产生该现象、②
II.探究FeCl3溶液的性质。
小组同学进行如下实验操作并观察到对应现象:
| 操作 | 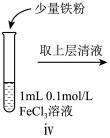 |  | 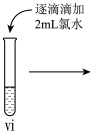 |
| 现象 | 溶液由棕黄色变为浅绿色 | 无明显现象 | 溶液变为红色, 而后红色褪去 |
(7)vi 中滴加氯水过程中,氯水反应的离子方程式是
III.小组同学探究vi中褪色原因,提出两种假设: a.铁离子被转化,b. SCN被转化。
(8)分别向褪色后的溶液中滴加0.1 mol/L FeCl3溶液和KSCN溶液各1滴,观察到
(9)进一步预测SCN-可能被转化为SO
某小组同学分别探究FeCl2溶液、FeCl3溶液的性质。
I.探究FeCl2溶液的性质。
(1)预测FeCl2具有还原性,预测依据是_______ ,因此可以与酸性KMnO4溶液反应。
(2)进行如下实验操作:
①i中的现象是_______ 。
②i中反应的化学方程式是_______ 。
③iii中的现象是_______ 。
(3)某同学认为iii中现象并不能证明Fe2+具有还原性,他的理由有二:①将酸性高锰酸钾稀释也可能产生该现象;②_______ 。
II.探究FeCl3溶液的性质。
小组同学进行如下实验操作并观察到对应现象:
(4)vi中滴加氯水过程中,氯水反应的离子方程式是_______ 。
III.小组同学探究vi中褪色原因,提出两种假设:a.铁离子被氧化,b.SCN-被氧化。
(5)分别向褪色后的溶液中滴加0.1 mol·L-1 FeCl3溶液和KSCN溶液各1滴,观察到_______ 现象,得出结论:假设b成立。
(6)进一步预测SCN-可能被转化为SO ,通过实验验证了该预测,写出实验操作及现象
,通过实验验证了该预测,写出实验操作及现象_______ 。
I.探究FeCl2溶液的性质。
(1)预测FeCl2具有还原性,预测依据是
(2)进行如下实验操作:
| 序号 | 操作 |
| i | 滴加NaOH溶液 | |
| ii | 加入少量锌粉 | |
| iii | 滴加酸性KMnO4溶液 |
②i中反应的化学方程式是
③iii中的现象是
(3)某同学认为iii中现象并不能证明Fe2+具有还原性,他的理由有二:①将酸性高锰酸钾稀释也可能产生该现象;②
II.探究FeCl3溶液的性质。
小组同学进行如下实验操作并观察到对应现象:
| 操作 |
|
|
|
| 现象 | 溶液由棕黄色变为浅绿色 | 无明显现象 | 溶液变为红色,而后红色褪去 |
III.小组同学探究vi中褪色原因,提出两种假设:a.铁离子被氧化,b.SCN-被氧化。
(5)分别向褪色后的溶液中滴加0.1 mol·L-1 FeCl3溶液和KSCN溶液各1滴,观察到
(6)进一步预测SCN-可能被转化为SO
某小组同学分别探究FeCl2溶液、FeCl3溶液的性质。
Ⅰ.探究FeCl2溶液的性质。
(1)从化合价的角度预测,FeCl2可能具有的性质___________ 。
(2)向FeCl2溶液中滴加酸性KMnO4溶液,可观察到的现象是___________ ,某同学认为上述现象并不能证明Fe2+具有还原性,他的理由___________ 。
Ⅱ.探究FeCl3溶液的性质
小组同学进行如下实验操作并观察到对应现象:
(3)iv中反应的离子方程式是___________
(4)vi 中滴加氯水过程中,氯水反应的离子方程式是___________ 。
Ⅲ.小组同学探究vi中褪色原因,提出两种假设: a.铁离子被转化,b.SCN-被转化
(5)分别向褪色后的溶液中滴加0.1 mol/L FeCl3溶液和KSCN溶液各1滴,观察到___________ 现象,得出结论:假设b成立。
(6)进一步预测SCN-可能被转化为SO ,通过实验验证了该预测,写出实验操作及现象
,通过实验验证了该预测,写出实验操作及现象___________
Ⅰ.探究FeCl2溶液的性质。
(1)从化合价的角度预测,FeCl2可能具有的性质
(2)向FeCl2溶液中滴加酸性KMnO4溶液,可观察到的现象是
Ⅱ.探究FeCl3溶液的性质
小组同学进行如下实验操作并观察到对应现象:
| 操作 | 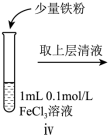 | 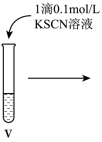 | 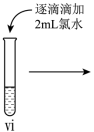 |
| 现象 | 溶液由棕黄色变为浅绿色 | 无明显现象 | 溶液变为红色,而后红色褪去 |
(4)vi 中滴加氯水过程中,氯水反应的离子方程式是
Ⅲ.小组同学探究vi中褪色原因,提出两种假设: a.铁离子被转化,b.SCN-被转化
(5)分别向褪色后的溶液中滴加0.1 mol/L FeCl3溶液和KSCN溶液各1滴,观察到
(6)进一步预测SCN-可能被转化为SO
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网