解答题-工业流程题 适中0.65 引用4 组卷866
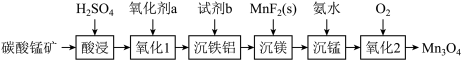
四氧化三锰是电子工业生产锰锌铁氧体软磁材料的重要原料。以碳酸锰矿(主要成分为MnCO3,还含有少量FeCO3、Al2O3、MgO和SiO2等杂质)为原料制备高品位四氧化三锰的一种工艺流程如下:
②Ksp(MgF2)=7.4×10-1l;Ksp(MnF2)=5.6×10-3
回答下列问题:
(1)提高“酸浸”效果的方法有___________ 、___________ (任写两种)。
(2)“氧化1”步骤中,氧化剂a可选用MnO2,发生反应的离子方程式为___________ ,为了检验氧化是否完全可选用的试剂是___________ (写化学式)。
(3)“沉铁铝”步骤中,调节pH的范围为___________ 。
(4)“沉镁”步骤中,沉淀转化反应的平衡常数K值等于___________ 。
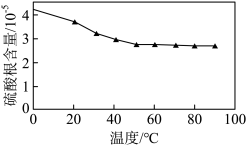
(5)“沉锰”步骤中,杂质含量直接影响四氧化三锰的品位,实验测得温度对四氧化三锰中硫酸根含量的影响如图所示。实际生产中综合考虑选择50°C为宜,不选择更高温度的原因是___________ 。___________ 。
| 金属离子 | Al3+ | Fe3+ | Fe2+ | Mg2+ | Mn2+ |
| 开始沉淀 | 4.1 | 2.2 | 7.5 | 9.6 | 8.8 |
| 完全沉淀 | 5.4 | 3.2 | 9.5 | / | / |
回答下列问题:
(1)提高“酸浸”效果的方法有
(2)“氧化1”步骤中,氧化剂a可选用MnO2,发生反应的离子方程式为
(3)“沉铁铝”步骤中,调节pH的范围为
(4)“沉镁”步骤中,沉淀转化反应的平衡常数K值等于
(5)“沉锰”步骤中,杂质含量直接影响四氧化三锰的品位,实验测得温度对四氧化三锰中硫酸根含量的影响如图所示。实际生产中综合考虑选择50°C为宜,不选择更高温度的原因是
2023·四川泸州·二模
类题推荐
硫酸锰是一种重要的化工中间体。一种以高硫锰矿(主要成分为含锰化合物及FeS)为原料制备硫酸锰的工艺流程如下:

已知:①“混合焙烧”后烧渣含MnSO4、Fe2O3及少量FeO、Al2O3、MgO。
②金属离子在水溶液中沉淀的pH范围如下表所示(25℃):
③离子浓度≤10-5mol·L-1时,离子沉淀完全。
请回答:
(1)为提高原料利用率“混合焙烧”时常采取的措施_______ 。
(2)氧化步骤发生反应的离子方程式为_______ ,若省略“氧化”步骤,造成的影响是_______ 。
(3)“中和除杂”时,应控制溶液的pH范围是_______ 。
(4)“氟化除杂”后,溶液中c(F-)浓度为0.05mol/L。则溶液中c(Mg2+)和c(Ca2+)的比值=_______ (已知:Ksp(MgF2)=6.4×10-10;Ksp(CaF2)=3.6×10-12)
(5)“碳化结晶”生成MnCO3沉淀时发生反应的离子方程式为_______ ,“碳化结晶”需选择合适的温度,温度不宜过高也不能过低的原因是_______ 。

已知:①“混合焙烧”后烧渣含MnSO4、Fe2O3及少量FeO、Al2O3、MgO。
②金属离子在水溶液中沉淀的pH范围如下表所示(25℃):
| 物质 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Al(OH)3 |
| 开始沉淀 | 1.9 | 7.6 | 7.3 | 3.0 |
| 完全沉淀 | 3.2 | 9.6 | 9.3 | 5.2 |
③离子浓度≤10-5mol·L-1时,离子沉淀完全。
请回答:
(1)为提高原料利用率“混合焙烧”时常采取的措施
(2)氧化步骤发生反应的离子方程式为
(3)“中和除杂”时,应控制溶液的pH范围是
(4)“氟化除杂”后,溶液中c(F-)浓度为0.05mol/L。则溶液中c(Mg2+)和c(Ca2+)的比值=
(5)“碳化结晶”生成MnCO3沉淀时发生反应的离子方程式为
硫酸锰是一种重要的化工中问体。一种以高硫锰矿(主要成分为含锰化合物及FeS)为原料制备硫酸锰的工艺流程如下:

已知:①“混合焙烧”后烧渣含MnSO4、Fe2O3及少量FeO、Al2O3、 MgO。
②金属离子在水溶液中沉淀的pH范围如下表所示(25°C):
③离子浓度 10-5mol·L-1时,离子沉淀完全。
10-5mol·L-1时,离子沉淀完全。
请回答:
(1)“混合焙烧”主要目的是_______
(2)若试剂a为MnO2,则氧化步骤发生反应的离子方程式为_______ ,若省略“氧化”步骤,造成的影响是_______ 。
(3)“中和除杂”时,应控制溶液的pH范围是_______ 。
(4)“氟化除杂”后,溶液中c(F- )浓度为0.05mol/L。则溶液中c(Mg2+)和c (Ca2+)的比值=_______ (已知: Ksp(MgF2)= 6.4×10-10; Ksp(CaF2)=3.6×10-12)
(5)“碳化结晶”时选择NH4HCO3, NH4HCO3溶液中各离子浓度大小顺序为_______ ,(已知CH3COONH4溶液呈中性)“碳化结晶”时发生反应的离子方程式为_______ ,“碳化结晶”时不选择Na2CO3溶液的原因是_______ 。

已知:①“混合焙烧”后烧渣含MnSO4、Fe2O3及少量FeO、Al2O3、 MgO。
②金属离子在水溶液中沉淀的pH范围如下表所示(25°C):
| 物质 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Al(OH)3 |
| 开始沉淀 | 1.9 | 7.6 | 7.3 | 3.0 |
| 完全沉淀 | 3.2 | 9.6 | 9.3 | 5.2 |
请回答:
(1)“混合焙烧”主要目的是
(2)若试剂a为MnO2,则氧化步骤发生反应的离子方程式为
(3)“中和除杂”时,应控制溶液的pH范围是
(4)“氟化除杂”后,溶液中c(F- )浓度为0.05mol/L。则溶液中c(Mg2+)和c (Ca2+)的比值=
(5)“碳化结晶”时选择NH4HCO3, NH4HCO3溶液中各离子浓度大小顺序为
硫酸锰是一种重要的化工中间体。一种以高硫锰矿(主要成分为含锰化合物及FeS)与氧化锰矿(主要成分为MnO2等锰的氧化物)为原料制备硫酸锰的工艺流程如下:

已知:①“混合焙烧”后烧渣含MnSO4、Fe2O3 及少量FeO、Al2O3、 MgO。
②金属离子在水溶液中沉淀的pH范围如下表所示(25℃):
③离子浓度≤10-5mol·L-1时,离子沉淀完全。
(1)“混合焙烧”的主要目的是_______
(2)MgO的沸点比Al2O3低的原因:_______ 。
(3)若试剂a为MnO2,则氧化步骤发生反应的离子方程式为_______ ,若省略“氧化”步骤,造成的影响是_______ 。
(4)“中和除杂”时,应控制溶液的pH范围是_______ 。
(5)“氟化除杂”后,溶液中c(F-)浓度为0.05mol·L-1.则溶液中c(Mg2+)和c(Ca2+)的比值=______ (已知: Ksp(MgF2)=6.4 ×10-10; Ksp(CaF2)=3.6×10-12)
(6)“碳化结晶”时发生反应的离子方程式为_______ ,选择NH4HCO3而不选择Na2CO3溶液的原因是_______ 。

已知:①“混合焙烧”后烧渣含MnSO4、Fe2O3 及少量FeO、Al2O3、 MgO。
②金属离子在水溶液中沉淀的pH范围如下表所示(25℃):
| 物质 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Al(OH)3 |
| 开始沉淀的pH | 1.9 | 7.6 | 7.3 | 3.0 |
| 完全沉淀的pH | 3.2 | 9.6 | 9.3 | 5.2 |
(1)“混合焙烧”的主要目的是
(2)MgO的沸点比Al2O3低的原因:
(3)若试剂a为MnO2,则氧化步骤发生反应的离子方程式为
(4)“中和除杂”时,应控制溶液的pH范围是
(5)“氟化除杂”后,溶液中c(F-)浓度为0.05mol·L-1.则溶液中c(Mg2+)和c(Ca2+)的比值=
(6)“碳化结晶”时发生反应的离子方程式为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


