解答题-原理综合题 适中0.65 引用1 组卷47
Ⅰ.工业合成氨与制备硝酸一般可连续生产,回答下列问题:
(1)工业生产时,制取氢气的一个反应为:CO+H2O(g) CO2+H2。T℃时,往1L密闭容器中充入0.2molCO和0.3mol水蒸气。反应建立平衡后,体系中c(H2)=0.12mol·L-1。该温度下此反应的平衡常数K=
CO2+H2。T℃时,往1L密闭容器中充入0.2molCO和0.3mol水蒸气。反应建立平衡后,体系中c(H2)=0.12mol·L-1。该温度下此反应的平衡常数K=___________ (填计算结果)。
(2)硝酸厂的尾气直接排放将污染空气,目前科学家探索利用燃料气体中的甲烷等将氮氧化物还原为氮气和水,其反应机理为:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g),ΔH=-574kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g),ΔH=-1160kJ·mol-1
则甲烷直接将NO2还原为N2的热化学方程式为:___________ 。
Ⅱ.甲醇是一种重要的有机化工原料,可用于制取甲醚。一定温度下,在三个体积为1.0L的恒容密闭容器中发生反应:2CH3OH(g) CH3OCH3(g)+H2O(g)。
CH3OCH3(g)+H2O(g)。
(3)容器I中的反应达到平衡时所需的时间___________ (填“大于”“小于”或等于)容器II中的。
(4)a=___________
(5)下列说法中能说明该反应达到平衡状态的是___________。(填字母)
(6)已知下面两个反应(m、n均大于0):
反应①:CO(g)+2H2(g) CH3OH(g) ΔH=-mkJ·mol-1
CH3OH(g) ΔH=-mkJ·mol-1
反应②:2CO(g)+4H2(g) CH3OCH3(g)+H2O(g) ΔH=-nkJ·mol-1
CH3OCH3(g)+H2O(g) ΔH=-nkJ·mol-1
则下列m与n的关系中,正确的是___________(填字母)。
(1)工业生产时,制取氢气的一个反应为:CO+H2O(g)
(2)硝酸厂的尾气直接排放将污染空气,目前科学家探索利用燃料气体中的甲烷等将氮氧化物还原为氮气和水,其反应机理为:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g),ΔH=-574kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g),ΔH=-1160kJ·mol-1
则甲烷直接将NO2还原为N2的热化学方程式为:
Ⅱ.甲醇是一种重要的有机化工原料,可用于制取甲醚。一定温度下,在三个体积为1.0L的恒容密闭容器中发生反应:2CH3OH(g)
| 容器编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
| CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
| I | 387 | 0.20 | 0.080 | 0.080 |
| II | 387 | 0.40 | a | b |
| III | 207 | 0.20 | 0.090 | 0.090 |
(4)a=
(5)下列说法中能说明该反应达到平衡状态的是___________。(填字母)
| A.容器中压强不变 |
| B.混合气体中c(CH3OCH3)不变 |
| C.混合气体的密度不变 |
| D.单位时间内生成1molCH3OCH3同时消耗2molCH3OH |
反应①:CO(g)+2H2(g)
反应②:2CO(g)+4H2(g)
则下列m与n的关系中,正确的是___________(填字母)。
| A.n>2m | B.m>2n | C.2m>n | D.m>3n |
22-23高二上·宁夏吴忠·期中
类题推荐
甲醇是一种重要的有机化工原料,可用于制取甲醚。一定温度下,在三个体积为1.0L的恒容密闭容器中发生反应:2CH3OH(g)⇌CH3OCH3(g)+H2O(g)。
(1)容器I中的反应达到平衡时所需的时间_____ (填“大于”“小于”或等于)容器III中的。
(2)a=___________
(3)下列说法中能说明该反应达到平衡状态的是___________。(填字母)
(4)已知下面两个反应(m、n均大于0):
反应①:CO(g)+2H2(g)⇌CH3OH(g) ΔH=-mkJ·mol-1
反应②:2CO(g)+4H2(g)⇌CH3OCH3(g)+H2O(g) ΔH=-nkJ·mol-1
则下列m与n的关系中,正确的是___________(填字母)。
| 容器 编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
| CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
| I | 387 | 0.20 | 0.080 | 0.080 |
| II | 387 | 0.40 | a | b |
| III | 207 | 0.20 | 0.090 | 0.090 |
(1)容器I中的反应达到平衡时所需的时间
(2)a=
(3)下列说法中能说明该反应达到平衡状态的是___________。(填字母)
| A.容器中压强不变 |
| B.混合气体中c(CH3OCH3)不变 |
| C.混合气体的密度不变 |
| D.单位时间内生成1mol CH3OCH3同时消耗2mol CH3OH |
反应①:CO(g)+2H2(g)⇌CH3OH(g) ΔH=-mkJ·mol-1
反应②:2CO(g)+4H2(g)⇌CH3OCH3(g)+H2O(g) ΔH=-nkJ·mol-1
则下列m与n的关系中,正确的是___________(填字母)。
| A.n﹥2m | B.m﹥2n | C.2m﹥n | D.m﹥3n |
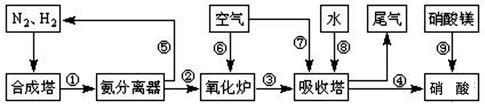
工业合成氨与制备硝酸一般可连续生产,流程如图所示:
(1)工业生产时,制取氢气的一个反应为:CO+H2O(g)⇌CO2+H2。T℃时,往1L密闭容器中充入0.2mol CO和0.3mol水蒸气。反应建立平衡后,体系中c(H2)=0.12mol·L-1.该温度下此反应的平衡常数K=______ (填计算结果)。
(2)合成塔中发生反应N2(g)+3H2(g)⇌2NH3(g);△H<0。下表为不同温度下该反应的平衡常数。由此可推知,表中T1______ 573K(填“>”、“<”或“=”)。
(3)N2和H2以铁作催化剂从145℃就开始反应,不同温度下NH3的产率如图所示。
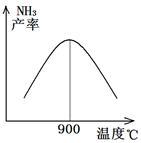
温度高于900℃时,NH3产率下降的原因是______ 。
(4)硝酸厂的尾气直接排放将污染空气,目前科学家探索利用燃料气体中的甲烷等将氮氧化物还原为氮气和水,其反应机理为:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g); △H=-574kJ·mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g); △H=-1160kJ·mol-1
则甲烷直接将NO2还原为N2的热化学方程式为:______
(5)氨气在纯氧中燃烧,生成一种单质和水。科学家利用此原理,设计成氨气-氧气燃料电池,则通入氨气的电极碱性条件下发生反应的电极反应式为______ 。

(1)工业生产时,制取氢气的一个反应为:CO+H2O(g)⇌CO2+H2。T℃时,往1L密闭容器中充入0.2mol CO和0.3mol水蒸气。反应建立平衡后,体系中c(H2)=0.12mol·L-1.该温度下此反应的平衡常数K=
(2)合成塔中发生反应N2(g)+3H2(g)⇌2NH3(g);△H<0。下表为不同温度下该反应的平衡常数。由此可推知,表中T1
| T/℃ | T1 | 300 | T2 |
| K | 1.00×107 | 2.45×105 | 1.88×103 |
(3)N2和H2以铁作催化剂从145℃就开始反应,不同温度下NH3的产率如图所示。

温度高于900℃时,NH3产率下降的原因是
(4)硝酸厂的尾气直接排放将污染空气,目前科学家探索利用燃料气体中的甲烷等将氮氧化物还原为氮气和水,其反应机理为:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g); △H=-574kJ·mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g); △H=-1160kJ·mol-1
则甲烷直接将NO2还原为N2的热化学方程式为:
(5)氨气在纯氧中燃烧,生成一种单质和水。科学家利用此原理,设计成氨气-氧气燃料电池,则通入氨气的电极碱性条件下发生反应的电极反应式为
工业合成氨与制备硝酸一般可连续生产,流程如图所示:

(1)工业生产时,制取氢气的一个反应为:CO+H2O(g) CO2+H2
CO2+H2
T℃时,往1L密闭容器中充入0.2mol CO和0.3mol水蒸气。反应建立平衡后,体系中c(H2)=0.12mol/L。
温度下此反应的平衡常数K=_____ (填计算结果)。
(2)合成塔中发生反应N2(g)+3H2(g) 2NH3(g);△H<0。下表为不同温度下该反应的平衡常数。由此可推知,表中T1
2NH3(g);△H<0。下表为不同温度下该反应的平衡常数。由此可推知,表中T1____ 300K(填“>”、“<”或“=”)。
(3)N2和H2以铁作催化剂从145℃就开始反应,不同温度下NH3的产率如图所示。温度高于900℃时,NH3产率下降的原因是___________ 。
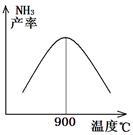
(4)硝酸厂的尾气直接排放将污染空气,目前科学家探索利用燃料气体中的甲烷等将氮氧化物还原为氮气和水,其反应机理为:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g); △H=-574kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g); △H=-1160kJ·mol-1
则甲烷直接将NO2还原为N2的热化学方程式为:_________________ 。
(5)氨气在纯氧中燃烧,生成一种单质和水。科学家利用此原理,设计成氨气-氧气燃料电池,则在碱性条件下通入氨气发生的电极反应式为______________ 。

(1)工业生产时,制取氢气的一个反应为:CO+H2O(g)
 CO2+H2
CO2+H2T℃时,往1L密闭容器中充入0.2mol CO和0.3mol水蒸气。反应建立平衡后,体系中c(H2)=0.12mol/L。
温度下此反应的平衡常数K=
(2)合成塔中发生反应N2(g)+3H2(g)
 2NH3(g);△H<0。下表为不同温度下该反应的平衡常数。由此可推知,表中T1
2NH3(g);△H<0。下表为不同温度下该反应的平衡常数。由此可推知,表中T1| T/℃ | T1 | 300 | T2 |
| K | 1.00×107 | 2.45×105 | 1.88×103 |

(4)硝酸厂的尾气直接排放将污染空气,目前科学家探索利用燃料气体中的甲烷等将氮氧化物还原为氮气和水,其反应机理为:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g); △H=-574kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g); △H=-1160kJ·mol-1
则甲烷直接将NO2还原为N2的热化学方程式为:
(5)氨气在纯氧中燃烧,生成一种单质和水。科学家利用此原理,设计成氨气-氧气燃料电池,则在碱性条件下通入氨气发生的电极反应式为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


