解答题-原理综合题 适中0.65 引用1 组卷660
完成下列小题
(1)选择合适的催化剂,一定条件下可直接光催化分解 ,发生反应:
,发生反应: ,该反应的
,该反应的
___________ 0(填“>”或“<”),在低温下,该反应___________ 自发进行(填“能”或“不能”)。
(2)写出氯碱工业原理的离子反应方程式:___________ 。
(3)亚硫酸 溶液存在电离平衡:
溶液存在电离平衡: ,
,
①已知25℃时, 的
的 溶液中,
溶液中, 的电离度为
的电离度为 ,
, 的一级电离平衡常数
的一级电离平衡常数
___________ (用含 的计算式表示,
的计算式表示, 第二步电离忽略不计,忽略水的电离)。
第二步电离忽略不计,忽略水的电离)。
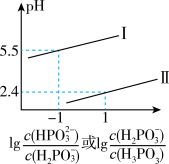
②常温下,将NaOH溶液滴加到亚硝酸 溶液中,混合溶液的pH与离子浓度变化的关系如图所示,则表示
溶液中,混合溶液的pH与离子浓度变化的关系如图所示,则表示 的是曲线
的是曲线___________ (填“Ⅰ”或“Ⅱ”),亚磷酸 的
的
___________ 。
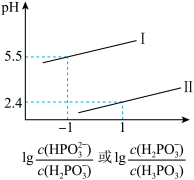
③请结合相关的平衡常数判断 稀溶液显
稀溶液显___________ 性(填“酸”、“中”或“碱”),其溶液中离子浓度由大到小的顺序是___________ 。
(4)25℃时,HF的电离常数 ;
; 的电离常数为
的电离常数为 ,
, ,
, 。足量NaF溶液和
。足量NaF溶液和 溶液反应的离子方程式为:
溶液反应的离子方程式为:___________ 。
(1)选择合适的催化剂,一定条件下可直接光催化分解
(2)写出氯碱工业原理的离子反应方程式:
(3)亚硫酸
①已知25℃时,
②常温下,将NaOH溶液滴加到亚硝酸

③请结合相关的平衡常数判断
(4)25℃时,HF的电离常数
22-23高二上·辽宁鞍山·期末
类题推荐
根据水溶液中的离子平衡有关知识回答下列问题:
(1)纯水在100℃时, ,该温度下
,该温度下 的NaOH溶液中,由水电离出的
的NaOH溶液中,由水电离出的
_______  。
。
(2)常温下,将 的稀盐酸与
的稀盐酸与 的NaOH溶液混合,所得溶液的pH为1,则
的NaOH溶液混合,所得溶液的pH为1,则
_______ (溶液体积变化忽略不计)。
(3)电离平衡常数是衡量弱电解质电离程度强弱的物理量。已知:
①25℃时,等浓度的a:NaCN溶液、b: 溶液和c:
溶液和c: 溶液,三种溶液的pH由大到小的顺序为
溶液,三种溶液的pH由大到小的顺序为_______ 。(大小用a、b、c表示)
②向NaCN溶液中通入少量的 ,发生反应的化学方程式为
,发生反应的化学方程式为_______ 。
(4)常温下,用0.1000 mol∙L−1的NaOH溶液滴定20.00mL0.1000 mol∙L−1的 溶液,滴定过程中,溶液的pH与消耗NaOH溶液的体积的关系如图所示:
溶液,滴定过程中,溶液的pH与消耗NaOH溶液的体积的关系如图所示:

①该滴定过程应该选择_______ (填“酚酞”或“甲基橙”)作指示剂。
②a_______ 20mL(填“>”“<”或“=”)。
③C点溶液中离子浓度由大到小的顺序为_______ 。
(1)纯水在100℃时,
(2)常温下,将
(3)电离平衡常数是衡量弱电解质电离程度强弱的物理量。已知:
| 化学式 | 电离常数(25℃) |
| HCN | |
②向NaCN溶液中通入少量的
(4)常温下,用0.1000 mol∙L−1的NaOH溶液滴定20.00mL0.1000 mol∙L−1的

①该滴定过程应该选择
②a
③C点溶液中离子浓度由大到小的顺序为
Ⅰ.25℃时,部分弱酸的电离平衡常数如表所示:
回答下列问题:
(1)同浓度的 、
、 、
、 结合
结合 的能力由强到弱的顺序为
的能力由强到弱的顺序为________ (填离子符号)。
(2)亚磷酸( )为二元酸,具有较强的还原性,
)为二元酸,具有较强的还原性, 是
是_____ (填“酸式盐”“碱式盐”或“正盐”)。
(3)根据上述电离常数及物质的特性判断下列化学反应方程式错误的是______ (填序号)。
①次氯酸与 溶液的反应:
溶液的反应:
②少量 通入NaClO溶液中:
通入NaClO溶液中:
③碳酸钠滴入足量醋酸溶液中:
Ⅱ.某二元酸(化学式用 表示)的水溶液中存在的离子有:
表示)的水溶液中存在的离子有: 、
、 、
、 、
、 、
、 ,存在的分子有
,存在的分子有 。根据题意回答下列问题:
。根据题意回答下列问题:
(4)写出酸 的两步电离方程式:
的两步电离方程式:________ ;_______ 。
(5)若M溶液由10mL2mol/LNaHA溶液与10mL2mol/LNaOH溶液混合而得,则溶液M的pH___ 7(填“>”、“<”或“=”),溶液中离子浓度由大到小顺序为_________ 。
(6)在 的
的 溶液中,下列微粒浓度关系式正确的是______。
溶液中,下列微粒浓度关系式正确的是______。
(7)常温下,已知 溶液的pH=2,则当
溶液的pH=2,则当 溶液中
溶液中 为
为 时,
时, 溶液的物质的量浓度应
溶液的物质的量浓度应____ 0.1mol/L(填“>”或“<”或“=”);理由是_______ 。
| 化学式 | HClO | ||||
| 电离平衡常数(25℃) |
(1)同浓度的
(2)亚磷酸(
(3)根据上述电离常数及物质的特性判断下列化学反应方程式错误的是
①次氯酸与
②少量
③碳酸钠滴入足量醋酸溶液中:
Ⅱ.某二元酸(化学式用
(4)写出酸
(5)若M溶液由10mL2mol/LNaHA溶液与10mL2mol/LNaOH溶液混合而得,则溶液M的pH
(6)在
| A. |
| B. |
| C. |
| D. |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网