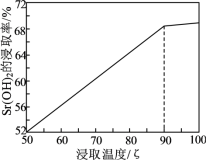解答题-工业流程题 较难0.4 引用1 组卷178
锶(Sr)是第五周期IIA族元素。自然界中的锶存在于天青石中,天青石的主要成分为SrSO4和少量CaSO4、BaSO4。以天青石为原料制备高纯SrCO3需要两个步骤。
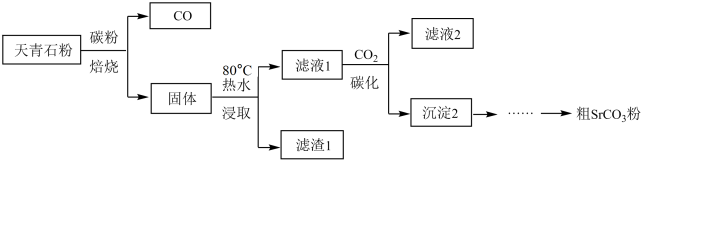
[步骤一]从天青石到粗SrCO3:
已知:i. Ca、Sr、Ba硫化物( MS)和硫氢化物[ M( HS)2]均易溶于水,
ii.20℃时,Sr(OH)2、Ba(OH)2、Ca(OH)2的溶解度(单位为g)分别为1.77、3. 89、0.173;80℃时,Sr(OH)2、 Ba(OH)2、Ca(OH)2的溶解度(单位为g)分别为20. 2、101.4、0.094。
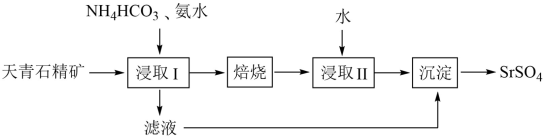
(1)焙烧过程中SrSO4转化为SrS的化学方程式是___________ 。
(2)浸取时发生反应:2MS+2H2O M( HS)2+M(OH)2(M=Ca、Sr、Ba)。使用热水有利于提高平衡转化率,原因是
M( HS)2+M(OH)2(M=Ca、Sr、Ba)。使用热水有利于提高平衡转化率,原因是___________ 。
(3)滤渣1的主要成分是___________ (写化学式)。
[步骤二]粗SrCO3转化为高纯SrCO3:
(4)粗SrCO3中的杂质是BaCO3.有同学提出在实验室可以将粗SrCO3产物溶于酸,再加入Na2SO4溶液实现Sr和Ba的分离。设Ba2+完全沉淀时c(Ba2+)= 10-5mol·L-1,则溶液中c(Sr2+)一定不大于___________ 。该方案___________ (填“合理”或者“不合理”)。[Ksp( BaSO4)= 1.1×10-10,Ksp(SrSO4)= 3.3×10-7]
(5)实际的工业除杂和转化流程如下图所示:

已知:i.溶液中存在 +H2O
+H2O 2
2 +2H+,
+2H+, 具有强氧化性。
具有强氧化性。
ii. Cr( OH)3的性质类似Al( OH)3,Ksp[ Cr(OH)3]=1×10-31。
①若酸溶过程中H+过量太多,则除钡过程中Ba2+去除率会下降,请从化学平衡移动角度解释原因___________ 。
②还原过程中草酸(H2C2O4)发生反应的离子方程式为___________ 。
③为除铬,向溶液D中加入NH3·H2O调节pH为7~8。此过程不调节pH为13的原因是___________ 。
[步骤一]从天青石到粗SrCO3:

已知:i. Ca、Sr、Ba硫化物( MS)和硫氢化物[ M( HS)2]均易溶于水,
ii.20℃时,Sr(OH)2、Ba(OH)2、Ca(OH)2的溶解度(单位为g)分别为1.77、3. 89、0.173;80℃时,Sr(OH)2、 Ba(OH)2、Ca(OH)2的溶解度(单位为g)分别为20. 2、101.4、0.094。
(1)焙烧过程中SrSO4转化为SrS的化学方程式是
(2)浸取时发生反应:2MS+2H2O
(3)滤渣1的主要成分是
[步骤二]粗SrCO3转化为高纯SrCO3:
(4)粗SrCO3中的杂质是BaCO3.有同学提出在实验室可以将粗SrCO3产物溶于酸,再加入Na2SO4溶液实现Sr和Ba的分离。设Ba2+完全沉淀时c(Ba2+)= 10-5mol·L-1,则溶液中c(Sr2+)一定不大于
(5)实际的工业除杂和转化流程如下图所示:

已知:i.溶液中存在
ii. Cr( OH)3的性质类似Al( OH)3,Ksp[ Cr(OH)3]=1×10-31。
①若酸溶过程中H+过量太多,则除钡过程中Ba2+去除率会下降,请从化学平衡移动角度解释原因
②还原过程中草酸(H2C2O4)发生反应的离子方程式为
③为除铬,向溶液D中加入NH3·H2O调节pH为7~8。此过程不调节pH为13的原因是
2023·新疆·一模
类题推荐
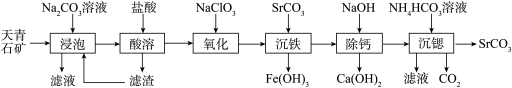
碳酸锶纯品是重要的无机化工产品。一种利用含锶矿渣(主要成分为SrSO4,还含有少量CaCO3和FeO)生产高纯碳酸锶的流程如图:
已知:①Ksp(SrSO4)=3.2×10-7,Ksp(SrCO3)=1.6×10-10
②Sr(OH)2、Ca(OH)2在不同温度下的溶解度表(g/100mLH2O)
③“除钙”时,控制溶液温度95℃~100℃,向滤液中加入NaOH溶液,调节pH≥12,趁热过滤得Ca(OH)2沉淀。
(1)浸泡后所得滤液中c(CO )=2.0×10-3mol•L-1,则c(SO
)=2.0×10-3mol•L-1,则c(SO )=
)=_____ 。
(2)“氧化”反应的离子反应方程式为_____ 。
(3)“沉铁”反应的离子反应方程式为_____ 。
(4)“沉锶”也可以使用Na2CO3溶液,但使用Na2CO3溶液可能会生成杂质。使用Na2CO3溶液可能会生成杂质及原因是_____ 。

已知:①Ksp(SrSO4)=3.2×10-7,Ksp(SrCO3)=1.6×10-10
②Sr(OH)2、Ca(OH)2在不同温度下的溶解度表(g/100mLH2O)
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 90 | 100 |
| Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 | 0.07 |
| Sr(OH)2 | 0.91 | 1.77 | 3.95 | 8.42 | 20.20 | 44.50 | 91.20 |
(1)浸泡后所得滤液中c(CO
(2)“氧化”反应的离子反应方程式为
(3)“沉铁”反应的离子反应方程式为
(4)“沉锶”也可以使用Na2CO3溶液,但使用Na2CO3溶液可能会生成杂质。使用Na2CO3溶液可能会生成杂质及原因是
碳酸锶是重要的化工基础原料,由工业级硝酸锶(含有Ba2+、Ca2+、Mg2+等杂质)制备分析纯碳酸锶的工艺流程如下:
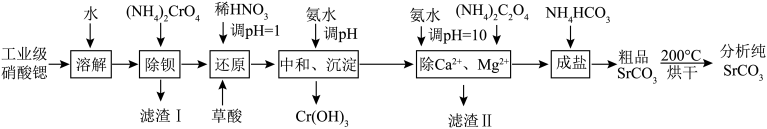
已知:①BaCrO4不溶于水,在水溶液中Cr2O72-与Ba2+不能结合。
②常温下,各物质的溶积常数如下表所示:
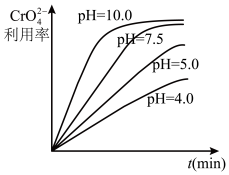
(1)“除钡”过程中CrO42-在不同pH时的利用率随时间变化曲线如下图所示,根据图像分析“除钡”过程中需要调节pH=7.5的原因_______________________________ 。
(2)“还原”过程中,应先调节pH=1.0,再加入草酸,加入草酸时发生反应的离子方程式为_____________________________ 。
(3)“滤渣Ⅱ”的主要成分为________________ 。
(4)“除Ca2+、Mg2+”后得到的滤液中除含有Sr(NO3)2外还含有过量的NH3·H2O,则“成盐”过程中发生反应的离子方程式为__________________________ 。
(5)“粗品SrCO3”烘干过程中除去的主要杂质为_____________________ 。
(6)在“中和、沉淀”步骤中,假定开始Cr3+,Zn3+浓度为0.1mol/L,调节至pH为_______ 时,铬开始沉淀;继续加碱调节至pH为_____ 时,铬刚好完全沉淀(离子浓度小于1×10-6mol/L时,即可认为该离子沉淀完全)。

已知:①BaCrO4不溶于水,在水溶液中Cr2O72-与Ba2+不能结合。
②常温下,各物质的溶积常数如下表所示:
| 化合物 | Ca(OH)2 | CaC2O4 | Mg(OH)2 | MgC2O4 | Cr(OH)3 |
| Ksp近似值 | 5.0×10-6 | 2.2×10-9 | 5.6×10-12 | 4.8×10-6 | 10-30 |
(1)“除钡”过程中CrO42-在不同pH时的利用率随时间变化曲线如下图所示,根据图像分析“除钡”过程中需要调节pH=7.5的原因

(2)“还原”过程中,应先调节pH=1.0,再加入草酸,加入草酸时发生反应的离子方程式为
(3)“滤渣Ⅱ”的主要成分为
(4)“除Ca2+、Mg2+”后得到的滤液中除含有Sr(NO3)2外还含有过量的NH3·H2O,则“成盐”过程中发生反应的离子方程式为
(5)“粗品SrCO3”烘干过程中除去的主要杂质为
(6)在“中和、沉淀”步骤中,假定开始Cr3+,Zn3+浓度为0.1mol/L,调节至pH为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网