解答题-工业流程题 较难0.4 引用4 组卷889
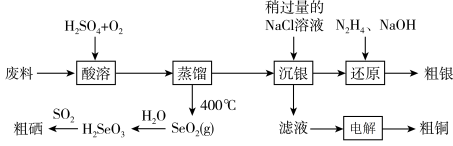
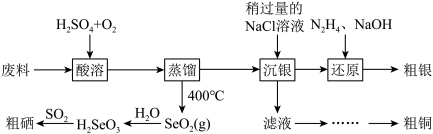
工业上以硒化银半导体废料(含 、Cu)为原料提取硒、铜、银,进而制备一种新型太阳能电池的材料。
、Cu)为原料提取硒、铜、银,进而制备一种新型太阳能电池的材料。
已知:25℃。 ,
, 。
。
请回答下列问题:
(1)“酸溶”时,为提高废料中硒元素的浸出率可采取的措施是___________ (任写一种),写出废料中 转化为
转化为 的化学反应方程式
的化学反应方程式___________ 。
(2)制得的粗铜可通过电解法精炼,电解质溶液可以选择___________(填字母序号)。
(3)上述流程中,通入 发生氧化还原反应获得“粗硒”,该过程中氧化剂和还原剂的物质的量之比为
发生氧化还原反应获得“粗硒”,该过程中氧化剂和还原剂的物质的量之比为___________ 。
(4)“沉银”时,从平衡移动角度解释,加入稍过量 溶液的原因
溶液的原因___________ ,计算 转化成
转化成 的平衡常数
的平衡常数
___________ 。
(5)“还原”时,写出 与液态
与液态 、
、 溶液反应制取粗银的离子方程式
溶液反应制取粗银的离子方程式___________ 。

已知:25℃。
请回答下列问题:
(1)“酸溶”时,为提高废料中硒元素的浸出率可采取的措施是
(2)制得的粗铜可通过电解法精炼,电解质溶液可以选择___________(填字母序号)。
| A.稀 | B. | C. | D. |
(4)“沉银”时,从平衡移动角度解释,加入稍过量
(5)“还原”时,写出
2023·福建漳州·三模
类题推荐
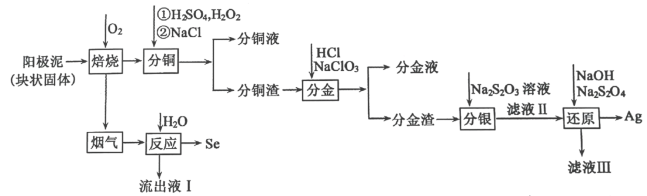
电解精炼铜的阳极泥中含有大量的贵重金属和硒、碲等非金属元素。实验室从电解精炼铜的阳极泥中提取金、银、硒的流程如下:
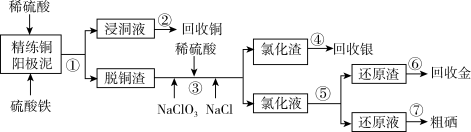
已知:单质金在酸性环境下与NaClO3、NaCl反应生成NaAuCl4;NaAuCl4可被Fe2+、SO2还原为单质金;硒的化合物不能被Fe2+还原,而能被SO2还原。
请回答下列问题:
(1)步骤①所得“浸铜液”中铜元素的存在形态为______ (用化学式表示);加入稀硫酸的目的是____________________ 。
(2)写出步骤③中金元素进入“氯化液”的离子反应方程式___________ ;银元素进入“氯化渣”中,则其存在的形态为_______ (用化学式表示)。
(3)步骤⑤需在氯化液中加入适当的试剂,可选择的试剂为______ (填代号)。
若“氯化液”中c(AuCl )为0.01mol·L-1,则处理500mL该“氯化液”需消耗该物质的质量为
)为0.01mol·L-1,则处理500mL该“氯化液”需消耗该物质的质量为_______ g。
(4)步骤②可以通过电解的方法得到单质铜,则电解时阴极的电极反应式为__________ ;在步骤③中,硒元素被氧化成亚硒酸,则步骤⑦制粗硒的化学反应方程式_____________ 。

已知:单质金在酸性环境下与NaClO3、NaCl反应生成NaAuCl4;NaAuCl4可被Fe2+、SO2还原为单质金;硒的化合物不能被Fe2+还原,而能被SO2还原。
请回答下列问题:
(1)步骤①所得“浸铜液”中铜元素的存在形态为
(2)写出步骤③中金元素进入“氯化液”的离子反应方程式
(3)步骤⑤需在氯化液中加入适当的试剂,可选择的试剂为
| A.FeSO4·7H2O | B.FeCl3 | C.SO2 | D.Na2SO3 |
(4)步骤②可以通过电解的方法得到单质铜,则电解时阴极的电极反应式为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网