单选题 适中0.65 引用11 组卷1661
下图是用钌 基催化剂催化
基催化剂催化 和
和 的反应示意图,当反应生成
的反应示意图,当反应生成 液态
液态 时放出
时放出 的热量。下列说法错误的是
的热量。下列说法错误的是
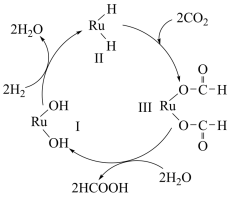

| A.反应历程中存在极性键、非极性键的断裂与形成 |
| B.图示中物质I为该反应的催化剂,物质II、III为中间产物 |
| C.使用催化剂可以降低反应的活化能,但无法改变反应的焓变 |
| D.由题意知: |
2023·广东汕头·一模
类题推荐
下列说法正确的是
| A.小苏打溶液中溶质的电离:NaHCO3 |
| B.钢铁发生吸氧腐蚀时的正极反应:O2+2H2O+4e-=4OH- |
| C.甲烷燃烧热的热化学方程式:CH4(g)+2O2(g)=CO2(g)+2H2O(g)ΔH=-801.3kJ·mol-1 |
| D.将盐酸与氨水的稀溶液混合后,生成1molH2O(l),会放出QkJ的能量,对应的热化学方程式为:H+(ag)+OH-(aq)=H2O(l)ΔH=-QkJ·mol-1 |
下列依据热化学方程式得出的结论正确的是
| A.若将等质量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| B.已知C(石墨,s)=C(金刚石,s)△H>0,则金刚石比石墨稳定 |
| C.已知2C(s)+2O2(g)=2CO2(g);△H1,2C(s)+O2(g)=2CO(g);△H2,则△H1>△H2 |
| D.在101kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式可表 示为 2H2(g)+O2(g)=2H2O(l) △H=﹣571.6 kJ•mol﹣1 |
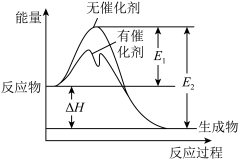
2SO2(g)+O2(g) 2SO3(g)反应过程中的能量变化如图所示(图中E1表示无催化剂时正反应的活化能,E2表示无催化剂时逆反应的活化能)。下列有关叙述正确的是
2SO3(g)反应过程中的能量变化如图所示(图中E1表示无催化剂时正反应的活化能,E2表示无催化剂时逆反应的活化能)。下列有关叙述正确的是
 2SO3(g)反应过程中的能量变化如图所示(图中E1表示无催化剂时正反应的活化能,E2表示无催化剂时逆反应的活化能)。下列有关叙述正确的是
2SO3(g)反应过程中的能量变化如图所示(图中E1表示无催化剂时正反应的活化能,E2表示无催化剂时逆反应的活化能)。下列有关叙述正确的是
| A.该反应的正反应为吸热反应,升高温度可提高活化分子的总数 |
B.0℃、101 kPa下,将1 mol SO2(g)和0.5 mol O2(g)置于密闭容器中充分反应生成SO3(g)放热a kJ,其热化学方程式为2SO2(g)+O2(g) 2SO3(g) ΔH=-2a kJ·mol-l 2SO3(g) ΔH=-2a kJ·mol-l |
| C.该反应中,反应物的总键能小于生成物的总键能 |
| D.ΔH=E1-E2,使用催化剂改变活化能,也改变反应热 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


