解答题-工业流程题 适中0.65 引用1 组卷207
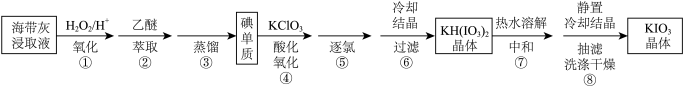
KIO3是常见的食盐加碘剂,实验室制备KIO3晶体的流程如图:
已知:①碘易溶于乙醚,乙醚难溶于水;
②KIO3在水中的溶解度:20℃为8.1g,80℃为21.8g;KIO3难溶于乙醇。
(1)步骤①“氧化”的离子方程式为_____ 。
(2)步骤④中,每1mol碘单质被氧化,转移_____ mol电子。
(3)步骤⑦“中和”的化学方程式为_____ 。步骤⑧中“洗涤”时,最好选用_____ 作为洗涤剂。
(4)以NaIO3为原料制备 的方法是:先向NaIO3溶液中加入过量的NaHSO3,生成碘化物;再向混合溶液中加入NaIO3溶液,反应得到I2,请写出上述制备I2的总反应的离子方程式:
的方法是:先向NaIO3溶液中加入过量的NaHSO3,生成碘化物;再向混合溶液中加入NaIO3溶液,反应得到I2,请写出上述制备I2的总反应的离子方程式:_____ 。
(5)KI溶液和CuSO4溶液混合可生成CuI沉淀和I2,若生成1molI2,消耗的KI至少为_____ mol。I2在KI溶液中可发生反应I2+I- I
I ,KI3易溶于水。实验室中使用过量的KI与CuSO4溶液反应后,过滤,滤液经水蒸气蒸馏可制得高纯碘。反应中加入过量KI的原因是
,KI3易溶于水。实验室中使用过量的KI与CuSO4溶液反应后,过滤,滤液经水蒸气蒸馏可制得高纯碘。反应中加入过量KI的原因是_____ 。

已知:①碘易溶于乙醚,乙醚难溶于水;
②KIO3在水中的溶解度:20℃为8.1g,80℃为21.8g;KIO3难溶于乙醇。
(1)步骤①“氧化”的离子方程式为
(2)步骤④中,每1mol碘单质被氧化,转移
(3)步骤⑦“中和”的化学方程式为
(4)以NaIO3为原料制备
(5)KI溶液和CuSO4溶液混合可生成CuI沉淀和I2,若生成1molI2,消耗的KI至少为
22-23高一·上海宝山·阶段练习
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网