解答题-原理综合题 适中0.65 引用2 组卷187
资源化利用CO2,不仅可以减少温室气体的排放,还可以获得燃料或重要的化工产品。回答下列问题。
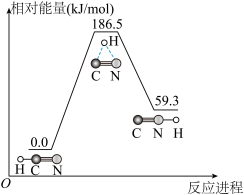
(1)理论研究表明,在101 kPa和298 K下,HCN(g) HNC(g)异构化反应过程的能量变化如图所示:计算可得HCN(g)
HNC(g)异构化反应过程的能量变化如图所示:计算可得HCN(g) HNC(g) ΔH=
HNC(g) ΔH=_______ kJ/mol。HCN与HNC稳定性较强的是_______ 。
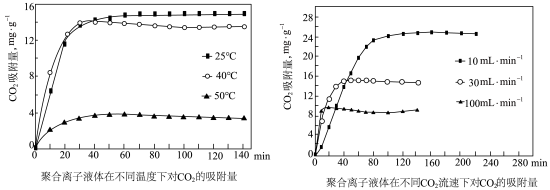
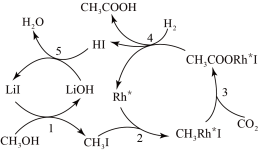
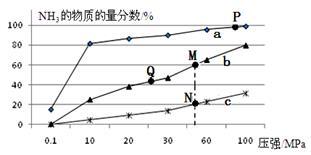
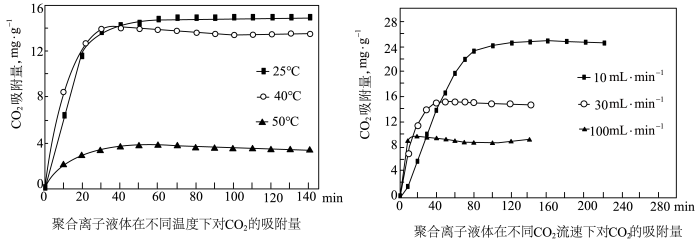
(2)聚合离子液体是目前广泛研究的CO2吸附剂。结合下图 分析聚合离子液体吸附CO2的有利条件是_______ 。
(3)生产尿素:
工业上以CO2、NH3为原料生产尿素[CO(NH2)2],该反应分为二步进行:
第一步:2NH3(g)+CO2(g)⇌ H2NCOONH4(s) △H = - 159.5 kJ·mol-1
第二步:H2NCOONH4(s)⇌CO(NH2)2(s)+ H2O(g) △H = +116.5 kJ·mol-1
①写出上述合成尿素的热化学方程式_______ 。
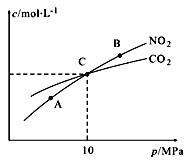
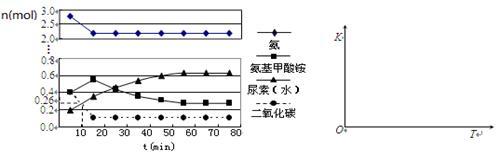
②某实验小组模拟工业上合成尿素,在一定体积的密闭容器中投入4mol NH3和1mol CO2,实验测得反应中各组分物质的量随时间的变化如下图所示:
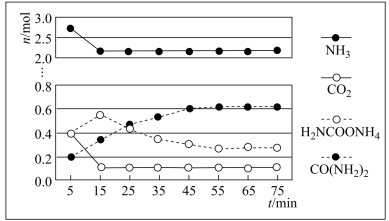
已知总反应的快慢由慢的一步反应决定,则合成尿素总反应的快慢由第_______ 步反应决定,总反应进行到_______ min时到达平衡。
(4)合成乙酸:
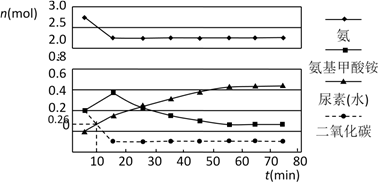
中国科学家首次以CH3OH、CO2和H2为原料高效合 成乙酸,其反应路径如下图所示:
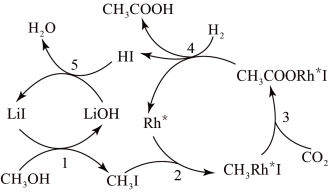
①原料中的CH3OH可通过电解法由CO2制取,用稀硫酸作电解质溶液,写出生成CH3OH的电极反应式_______ 。
②根据图示 ,写出总反应的化学方程式_______ 。
(1)理论研究表明,在101 kPa和298 K下,HCN(g)

(2)聚合离子液体是目前广泛研究的CO2吸附剂。

(3)生产尿素:
工业上以CO2、NH3为原料生产尿素[CO(NH2)2],该反应分为二步进行:
第一步:2NH3(g)+CO2(g)⇌ H2NCOONH4(s) △H = - 159.5 kJ·mol-1
第二步:H2NCOONH4(s)⇌CO(NH2)2(s)+ H2O(g) △H = +116.5 kJ·mol-1
①写出上述合成尿素的热化学方程式
②某实验小组模拟工业上合成尿素,在一定体积的密闭容器中投入4mol NH3和1mol CO2,实验测得反应中各组分物质的量随时间的变化如下图所示:

已知总反应的快慢由慢的一步反应决定,则合成尿素总反应的快慢由第
(4)合成乙酸:
中国科学家首次以CH3OH、CO2和H2为原料高效合 成乙酸,其反应路径如下图所示:

①原料中的CH3OH可通过电解法由CO2制取,用稀硫酸作电解质溶液,写出生成CH3OH的电极反应式
②
22-23高二上·福建福州·期末
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网