解答题-工业流程题 适中0.65 引用1 组卷77
镍是一种常用的催化剂。以红土镍矿(主要含有 、
、 、
、 、
、 等)为原料,制取纳米镍粉,同时获得净水剂黄钠铁矾
等)为原料,制取纳米镍粉,同时获得净水剂黄钠铁矾 的工艺流程如下:
的工艺流程如下:
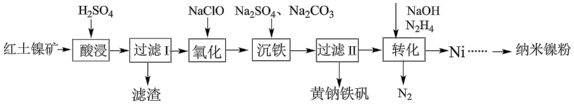
回答下列问题:
(1)黄钠铁矾 中,铁的化合价为
中,铁的化合价为_______ 价;黄钠铁矾能净水的原因是_______ 。
(2)过滤操作时要遵循“一贴、二低、三靠”的原则,其中“二低”指的是滤纸边缘略低于漏斗口、_______ 。
(3)“沉铁”过程加入 的目的是
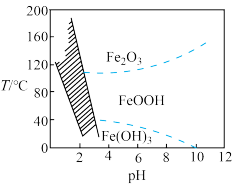
的目的是_______ ,控制不同的条件可以得到不同的沉淀,所得沉淀与温度、 的关系如图所示(图中阴影部分表示的是黄钠铁矾稳定存在区域)。若反应在120℃时进行,加入的
的关系如图所示(图中阴影部分表示的是黄钠铁矾稳定存在区域)。若反应在120℃时进行,加入的 偏多,则所得黄钠铁矾中混有的杂质是
偏多,则所得黄钠铁矾中混有的杂质是_______ (填化学式)。
(4)“转化”过程,向“过滤II”所得滤液(富含 )中加入
)中加入 ,控制溶液中
,控制溶液中 的浓度,可得到不同晶态物质(
的浓度,可得到不同晶态物质( 、
、 或二者的混合物)。当生成
或二者的混合物)。当生成 和
和 的物质的量之比为
的物质的量之比为 时,该反应的离子方程式为
时,该反应的离子方程式为_______ ;在其他条件不变的情况下,随 浓度增大,产物中
浓度增大,产物中 的含量增加,原因是
的含量增加,原因是_______ 。
(5)化学镀镍是金属表面镀镍的常用方法,以 为镀液,次亚磷酸钠
为镀液,次亚磷酸钠 为还原剂,在90℃的酸性溶液中发生反应,
为还原剂,在90℃的酸性溶液中发生反应, 被氧化为亚磷酸
被氧化为亚磷酸 。写出化学镀镍反应的离子方程式:
。写出化学镀镍反应的离子方程式:_______ 。

回答下列问题:
(1)黄钠铁矾
(2)过滤操作时要遵循“一贴、二低、三靠”的原则,其中“二低”指的是滤纸边缘略低于漏斗口、
(3)“沉铁”过程加入

(4)“转化”过程,向“过滤II”所得滤液(富含
(5)化学镀镍是金属表面镀镍的常用方法,以
22-23高二上·云南楚雄·期末
类题推荐
镍是化工产业的重要原料。以红土镍矿(主要含有Fe2O3、FeO、NiO、SiO2等)为原料,制取纳米镍粉,同时获得净水剂黄钠铁矾[NaFe3(SO4)2(OH)6]的工艺流程如下:
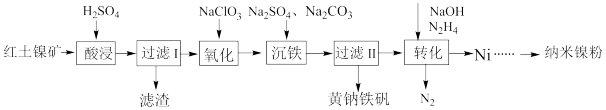
溶液中Ni2+离子开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)“酸浸”时需要加热,其原因是______ 。
(2)“氧化”过程发生反应的离子方程式是______ 。
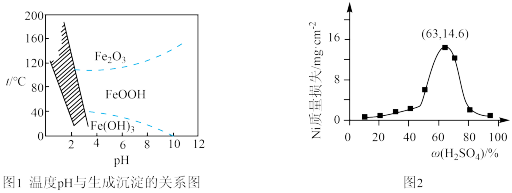
(3)“沉铁”过程,控制不同的条件可以得到不同的沉淀,所得沉淀与温度、pH的关系如图所示(图1中阴影部分表示的是黄钠铁矾稳定存在区域)。若反应在80℃时进行,加碳酸钠偏多,则所得黄钠铁矾中混有的杂质是______ ;检验沉铁步骤中反应是否完全的方法是______ 。
(4)利用上述表格数据,计算Ni(OH)2的Ksp=______ (列出计算式)。
(5)“转化”过程,向“过滤II”所得滤液(富含Ni2+)中加入N2H4,控制溶液中NaOH的浓度,可得到不同晶态物质(NiSO4·Ni、Ni或二者的混合物)。写出生成Ni的离子方程式______ 。
(6)95℃时,将Ni片浸在不同质量分数的硫酸中,经4小时腐蚀后的质量损失情况如图2所示,当ω(H2SO4)大于63%时,Ni被腐蚀的速率逐渐降低的可能原因为______ 。

溶液中Ni2+离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 | Ni2+ |
| 开始沉淀时(c=0.01mol·L-1)的pH | 7.2 |
| 沉淀完全时(c=1.0×10-5mol·L-1)的pH | 8.7 |
(1)“酸浸”时需要加热,其原因是
(2)“氧化”过程发生反应的离子方程式是
(3)“沉铁”过程,控制不同的条件可以得到不同的沉淀,所得沉淀与温度、pH的关系如图所示(图1中阴影部分表示的是黄钠铁矾稳定存在区域)。若反应在80℃时进行,加碳酸钠偏多,则所得黄钠铁矾中混有的杂质是

(4)利用上述表格数据,计算Ni(OH)2的Ksp=
(5)“转化”过程,向“过滤II”所得滤液(富含Ni2+)中加入N2H4,控制溶液中NaOH的浓度,可得到不同晶态物质(NiSO4·Ni、Ni或二者的混合物)。写出生成Ni的离子方程式
(6)95℃时,将Ni片浸在不同质量分数的硫酸中,经4小时腐蚀后的质量损失情况如图2所示,当ω(H2SO4)大于63%时,Ni被腐蚀的速率逐渐降低的可能原因为
黄钠铁矾[NaFe3 (SO4)2(OH)6]是一种高效净水剂,Ni(OH)2可作为合成镍钴锰三元电极材料的原料,工业上可用红土镍矿(主要成分为NiO、FeO、Fe2O3、MgO和SiO2)制备黄钠铁矾和Ni (OH)2,工艺流程如图所示。
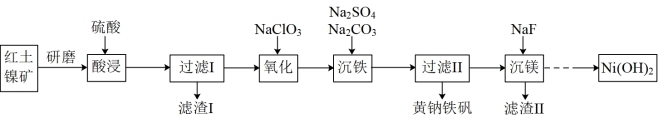
已知:①次亚磷酸钠(NaH2PO2)具有还原性;
②亚磷酸(H3PO3)是二元弱酸。
回答下列问题:
(1)下列说法正确的是_______ (填标号)。
(2)“氧化”过程中发生反应的离子方程式为:_______ ;为 了证明加入的NaClO3已足量,可取“氧化”后的溶液,向其中加入_______ 来检验(填标号)。
a. KSCN 溶液 b. K3[Fe(CN)6]溶液 C.酸性KMnO4溶液
(3)“沉铁” 过程,控制不同的条件可以得到不同的沉淀,所得沉淀与温度、pH的关系如图所示(图中阴影部分表示的是黄钠铁矾稳定存在区域),若控制pH=2.5,沉铁的最佳温度范围为_______ ;若反应在低于40℃时进行,加碳酸钠偏多,则所得黄钠铁矾中混有的杂质是_______ 。
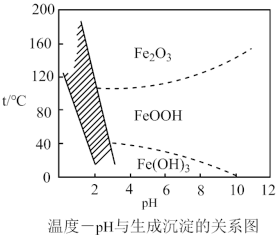
(4)①“沉镁”是生成MgF2沉淀除去Mg2+。若溶液酸度过高,则Mg2+沉淀不完全,原因是_______ 。
②若“沉镁”后溶液的pH=8.0,则此时Ni2+浓度约为_______ mol·L-1 (已知:100.4≈2.5,
Ksp[Ni(OH)2]=10-14.6)。
(5)化学镀镍是金属表面镀镍的常用方法。以NiSO4和NaH2PO2为原料,在90℃的酸性溶液中镀镍,同时生成H3PO3。写出化学镀镍反应的离子方程式_______ 。

已知:①次亚磷酸钠(NaH2PO2)具有还原性;
②亚磷酸(H3PO3)是二元弱酸。
回答下列问题:
(1)下列说法正确的是_______ (填标号)。
| A.研磨粉碎的目的是增大反应速率 |
| B.用浓硫酸可提高“酸浸”时的浸取率 |
| C.过滤时用到的玻璃仪器主要有漏斗、烧杯、玻璃棒 |
| D.“滤渣I”的主要成分为H2SiO3 |
a. KSCN 溶液 b. K3[Fe(CN)6]溶液 C.酸性KMnO4溶液
(3)“沉铁” 过程,控制不同的条件可以得到不同的沉淀,所得沉淀与温度、pH的关系如图所示(图中阴影部分表示的是黄钠铁矾稳定存在区域),若控制pH=2.5,沉铁的最佳温度范围为

(4)①“沉镁”是生成MgF2沉淀除去Mg2+。若溶液酸度过高,则Mg2+沉淀不完全,原因是
②若“沉镁”后溶液的pH=8.0,则此时Ni2+浓度约为
Ksp[Ni(OH)2]=10-14.6)。
(5)化学镀镍是金属表面镀镍的常用方法。以NiSO4和NaH2PO2为原料,在90℃的酸性溶液中镀镍,同时生成H3PO3。写出化学镀镍反应的离子方程式
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网