解答题-原理综合题 适中0.65 引用2 组卷94
已知:① (g,环丙烷)
(g,环丙烷) (g,丙烷)
(g,丙烷) kJ·mol
kJ·mol 。
。
②丙烷(g)、环丙烷(g)的燃烧热 分别为-2220 kJ·mol
分别为-2220 kJ·mol 、-2092 kJ·mol
、-2092 kJ·mol 。
。
③ 、
、 的键能分别为498 kJ·mol
的键能分别为498 kJ·mol 、463 kJ·mol
、463 kJ·mol 。
。
回答下列问题:
(1)写出表示 燃烧热的热化学方程式:
燃烧热的热化学方程式:_______ 。
(2)

_______ kJ·mol 。
。
(3)热值指单位质量可燃物完全燃烧时放出的热量(单位:kJ·g )。环丙烷、丙烷、氢气三种气体完全燃烧生成液态水、二氧化碳,其热值最大的是
)。环丙烷、丙烷、氢气三种气体完全燃烧生成液态水、二氧化碳,其热值最大的是_______ (填名称)。
(4)上述反应①的能量变化如图所示。
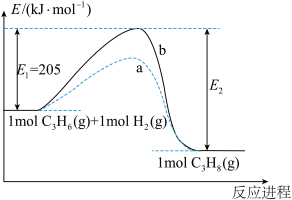
曲线a或b代表镍催化剂对反应的影响,其中表示加入镍催化剂的曲线是_______ (填“a”或“b”)。
_______ 。
(5)一定量的丙烷和环丙烷的混合气体完全燃烧生成液态水和二氧化碳时放出的热量为Q kJ,将产物经浓硫酸干燥,再通过足量的过氧化钠粉末,固体净增8.4 g。由此可知,Q的范围为_______ 。
②丙烷(g)、环丙烷(g)的燃烧热
③
回答下列问题:
(1)写出表示
(2)
(3)热值指单位质量可燃物完全燃烧时放出的热量(单位:kJ·g
(4)上述反应①的能量变化如图所示。

曲线a或b代表镍催化剂对反应的影响,其中表示加入镍催化剂的曲线是
(5)一定量的丙烷和环丙烷的混合气体完全燃烧生成液态水和二氧化碳时放出的热量为Q kJ,将产物经浓硫酸干燥,再通过足量的过氧化钠粉末,固体净增8.4 g。由此可知,Q的范围为
22-23高二上·海南·期末
类题推荐
回答下列问题。
(1)足量 在
在 中完全燃烧生成
中完全燃烧生成 液态水,放出
液态水,放出 的热量,
的热量, 的燃烧热ΔH=
的燃烧热ΔH=___________ 。
(2)N2H4可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和H2O。已知:
①N2(g)+2O2(g)=N2O4(l) ΔH=-19.5kJ·mol-1
②N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH=-534.2kJ·mol-1
写出液体燃料N2H4与液态N2O4反应的热化学方程式:___________ 。
(3)在230℃和催化剂存在的条件下,将CO2与H2转化为CH3OH(g)和H2O(g)。如图为生产1 mol CH3OH(g)的能量变化示意图:

下表为破坏1 mol不同共价键所需的能量(kJ)。试计算:
CO2与H2转化为1 mol CH3OH(g)和H2O(g)的反应为___________ 反应(填吸热或放热),其ΔH=___________ 。
(4)已知下列两个热化学方程式:
 ,
,
 则
则 丙烷燃烧生成
丙烷燃烧生成 和气态水时释放的热量为
和气态水时释放的热量为___________ 
(5)已知:2H2(g)+O2(g)=2H2O(l) ∆H=-571.6kJ/mol,CO(g)+1/2O2(g)=CO2(g) ∆H=-283.0kJ/mol。某 和
和 的混合气体完全燃烧时放出
的混合气体完全燃烧时放出 热量,同时生成
热量,同时生成 液态水,则原混合气体中
液态水,则原混合气体中 和
和 的物质的量之比为
的物质的量之比为___________ 。
(1)足量
(2)N2H4可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和H2O。已知:
①N2(g)+2O2(g)=N2O4(l) ΔH=-19.5kJ·mol-1
②N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH=-534.2kJ·mol-1
写出液体燃料N2H4与液态N2O4反应的热化学方程式:
(3)在230℃和催化剂存在的条件下,将CO2与H2转化为CH3OH(g)和H2O(g)。如图为生产1 mol CH3OH(g)的能量变化示意图:

下表为破坏1 mol不同共价键所需的能量(kJ)。试计算:
| C-H | C-O | C=O | H-H | H-O |
| 413.4 | 351 | 745 | 436 | 462.8 |
(4)已知下列两个热化学方程式:
(5)已知:2H2(g)+O2(g)=2H2O(l) ∆H=-571.6kJ/mol,CO(g)+1/2O2(g)=CO2(g) ∆H=-283.0kJ/mol。某
C、CO、CH4和CH3OH(l)均是常用的燃料。回答下列问题:
(1)金刚石、石墨是C的两种同素异形体。已知:
①C(s,石墨)+O2(g)=CO2(g) ΔH1=-393.5 kJ·mol- 1
②C(s,金刚石)+O2(g)=CO2(g) △H2= -395.0 kJ·mol- 1
则稳定性:金刚石___________ (填“>”“=”或“<”)石墨。
(2)燃烧a g CH4生成二氧化碳气体和液态水,放出热量44.5 kJ。经测定,生成的CO2与足量澄清石灰水反应得到5 g沉淀,则CH4(g) + 2O2(g)=CO2(g) + 2H2O(l) △H1=___________ kJ·mol- 1,其中a=___________ 。
(3)已知完全燃烧1 mol C、CO、CH3OH(l)(有水生成时水为液态),放出的热量依次为393.5 kJ、283.0 kJ和726.5 kJ。
①写出表示CH3OH燃烧热的热化学方程式:___________ 。
②结合(2)数据,相同质量的上述4种物质完全燃烧,放出热量最多的是___________ (填化学式)。
(4)工业上可通过CO和H2化合制备CH3OH,该反应的热化学方程式为CO(g) +2H2(g)=CH3OH(g) △H = -116 kJ·mol- 1。断裂1mol某些化学键所吸收的能量数据如表:
则CO中形成1molC O键所放出的能量是
O键所放出的能量是___________ kJ。
(5)用CO2与H2也可生产CH3OH。已知:H2的燃烧热为285.8 kJ·mol- 1,CH3OH(g) =CH3OH(l) △H = - 37.3 kJ·mol- 1 ,利用(2)、(3)、(4)中的有关数据,可得CO2(g)+3H2(g)=CH3OH(l)+ H2O(1)的△H=___________ kJ·mol- 1。
(1)金刚石、石墨是C的两种同素异形体。已知:
①C(s,石墨)+O2(g)=CO2(g) ΔH1=-393.5 kJ·mol- 1
②C(s,金刚石)+O2(g)=CO2(g) △H2= -395.0 kJ·mol- 1
则稳定性:金刚石
(2)燃烧a g CH4生成二氧化碳气体和液态水,放出热量44.5 kJ。经测定,生成的CO2与足量澄清石灰水反应得到5 g沉淀,则CH4(g) + 2O2(g)=CO2(g) + 2H2O(l) △H1=
(3)已知完全燃烧1 mol C、CO、CH3OH(l)(有水生成时水为液态),放出的热量依次为393.5 kJ、283.0 kJ和726.5 kJ。
①写出表示CH3OH燃烧热的热化学方程式:
②结合(2)数据,相同质量的上述4种物质完全燃烧,放出热量最多的是
(4)工业上可通过CO和H2化合制备CH3OH,该反应的热化学方程式为CO(g) +2H2(g)=CH3OH(g) △H = -116 kJ·mol- 1。断裂1mol某些化学键所吸收的能量数据如表:
| 化学键 | C- H | H-H | C- O | H- O |
| 能量/kJ | 413 | 436 | 358 | 463 |
(5)用CO2与H2也可生产CH3OH。已知:H2的燃烧热为285.8 kJ·mol- 1,CH3OH(g) =CH3OH(l) △H = - 37.3 kJ·mol- 1 ,利用(2)、(3)、(4)中的有关数据,可得CO2(g)+3H2(g)=CH3OH(l)+ H2O(1)的△H=
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网