解答题-原理综合题 较难0.4 引用1 组卷102
利用 与天然气反应制取
与天然气反应制取 的原理是
的原理是 。在
。在 密闭容器中通入
密闭容器中通入 的
的 与
与 的
的 ,在三种不同条件下反应,测得
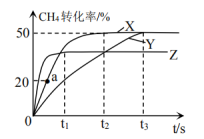
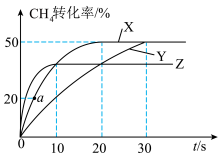
,在三种不同条件下反应,测得 的转化率与时间的关系如图所示。
的转化率与时间的关系如图所示。
(1)已知: ;
;
 。则反应
。则反应 的
的
_______  。
。
(2)下列现象说明反应已经达到平衡状态的是_______(填字母序号)
(3)由曲线Y到曲线X改变的条件可能是_______ ;由曲线X到曲线Z采取的措施可能是_______ 。
(4)曲线X对应实验条件下,从起始至达到平衡时,用 表示的反应速率
表示的反应速率
_______  ;曲线Y对应温度下该反应的平衡常数
;曲线Y对应温度下该反应的平衡常数
_______ 。
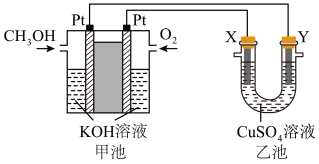
(5)以甲烷为燃料的新型电池得到广泛的研究应用,如图是目前研究较多的一类固体氧化物燃料电池工作原理示意图。
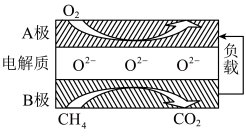
B极上的电极反应式为_______ 。若用该燃料电池作电源,用石墨作电极电解硫酸铜溶液,当阳极收集到 (标准状况)气体时,消耗甲烷的体积为
(标准状况)气体时,消耗甲烷的体积为_______ L(标准状况下)。

(1)已知:
(2)下列现象说明反应已经达到平衡状态的是_______(填字母序号)
| A. | B. |
| C.容器内气体密度保持不变 | D.混合气体的平均相对分子质量不变 |
(4)曲线X对应实验条件下,从起始至达到平衡时,用
(5)以甲烷为燃料的新型电池得到广泛的研究应用,如图是目前研究较多的一类固体氧化物燃料电池工作原理示意图。

B极上的电极反应式为
22-23高二下·安徽·开学考试
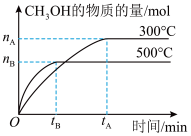
类题推荐  是一种重要的化工原料,被广泛应用在工农业生产中。请运用所学知识解决下列问题:
是一种重要的化工原料,被广泛应用在工农业生产中。请运用所学知识解决下列问题:
已知反应:


 工业制取炭黑的方法之一是将甲烷隔绝空气加热到
工业制取炭黑的方法之一是将甲烷隔绝空气加热到 进行裂解。该反应的热化学方程式为
进行裂解。该反应的热化学方程式为______ 。
 容积固定为1L的密闭容器内充入
容积固定为1L的密闭容器内充入 和
和 ,保持
,保持 发生反应
发生反应 ,用压力计监测反应过程中容器内压强的变化如下表:
,用压力计监测反应过程中容器内压强的变化如下表:
则反应从开始到20min时,以CO浓度变化表示的平均反应速率
______ 。
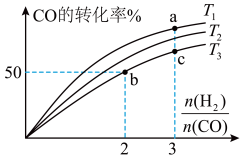
 对于反应
对于反应 来说:
来说:
 时,平衡常数
时,平衡常数 。
。 测得密闭容器中各物质达到平衡时物质的量浓度分别为:
测得密闭容器中各物质达到平衡时物质的量浓度分别为: ,
, ,
, ,
, ,则
,则
______  填“
填“ ”、“
”、“ ”或“
”或“ ”
” ,判断依据是
,判断依据是______ 。
 下列措施有利于提高反应混合气中
下列措施有利于提高反应混合气中 含量的是
含量的是______ 。
A.使用催化剂 升高温度
升高温度  及时导出CO
及时导出CO  增大反应体系的压强
增大反应体系的压强
 一定条件下,将
一定条件下,将 与
与 按物质的量之比1:1置于恒容密闭容器中反应,下列能说明该反应达到平衡状态的是
按物质的量之比1:1置于恒容密闭容器中反应,下列能说明该反应达到平衡状态的是______ 。
A.

B.体系中混合气体密度不变
C. 与
与 的转化率相等
的转化率相等
D. 与
与 物质的量之比不再改变
物质的量之比不再改变
E.反应体系压强不再改变
 以甲烷为燃料的新型电池得到广泛应用。下图是甲烷燃料电池工作原理的示意图。
以甲烷为燃料的新型电池得到广泛应用。下图是甲烷燃料电池工作原理的示意图。

 极上的电极反应式为
极上的电极反应式为______ 。
 以该燃料电池作电源,用石墨作电极电解硫酸铜溶液,当阳极收集到
以该燃料电池作电源,用石墨作电极电解硫酸铜溶液,当阳极收集到 标准状况
标准状况 气体时,消耗甲烷的体积为
气体时,消耗甲烷的体积为______  标准状况
标准状况 。
。
已知反应:
| 反应时间 | 0 | 5 | 10 | 15 | 20 | 25 |
| 压强 |
则反应从开始到20min时,以CO浓度变化表示的平均反应速率
A.使用催化剂
A.
B.体系中混合气体密度不变
C.
D.
E.反应体系压强不再改变

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网