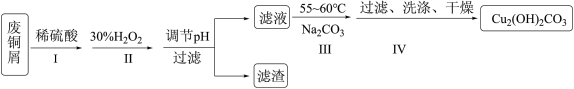解答题-工业流程题 适中0.65 引用1 组卷148
磷酸镁铵( )微溶于冷水、溶于热水和稀酸,可用作分析试剂、化肥和制药。实验室以精选氟磷灰石[含
)微溶于冷水、溶于热水和稀酸,可用作分析试剂、化肥和制药。实验室以精选氟磷灰石[含 、
、 、
、 ]为原料制备磷酸镁铵的一种工艺流程如图所示。
]为原料制备磷酸镁铵的一种工艺流程如图所示。
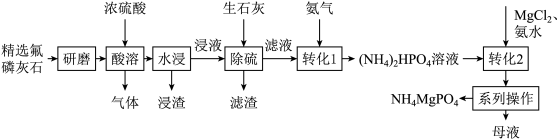
回答下列问题:
(1)“研磨”的目的是_______ ;“酸溶”操作不适合在陶瓷容器中进行的原因_______ 。
(2)浸渣和滤渣中含有一种相同成分,该物质的化学式为_______ ;常温下,该物质在水中的溶解度为_______  (已知:该物质溶度积常数为
(已知:该物质溶度积常数为 ,其饱和溶液密度取作水的密度)。
,其饱和溶液密度取作水的密度)。
(3)“除硫”操作为加入生石灰调节浸液的pH=0.5,调节pH过高导致的后果为_______ 。
(4)“转化1”中,为提高产品产率,需控制氨气与滤液中主要溶质( )的合理的物质的量之比为
)的合理的物质的量之比为_______ 。
(5)写出“转化2”中生成 的离子方程式:
的离子方程式:_______ 。
(6)“系列操作”具体指蒸发浓缩、冷却结晶、_______ (填操作)、冷水洗涤、干燥。

回答下列问题:
(1)“研磨”的目的是
(2)浸渣和滤渣中含有一种相同成分,该物质的化学式为
(3)“除硫”操作为加入生石灰调节浸液的pH=0.5,调节pH过高导致的后果为
(4)“转化1”中,为提高产品产率,需控制氨气与滤液中主要溶质(
(5)写出“转化2”中生成
(6)“系列操作”具体指蒸发浓缩、冷却结晶、
22-23高二上·陕西西安·期末
类题推荐
锂被誉为“金属味精”,以LiCoO2为正极材料的锂离子电池已被广泛用作便携式电源。工业上常以β-锂辉矿(主要成分为LiAlSi2O6,还含有FeO、MgO、CaO 等杂质)为原料来制取金属锂。其中一种工艺流程如下:

已知:①部分金属氢氧化物开始沉淀和完全沉淀时的pH:
②Li2CO3在不同温度下的溶解度如下表:
请回答下列问题:
(1)β-锂辉矿在处理前要粉碎,其主要目的是___________ ;用氧化物形式表示LiAlSi2O6的组成:___________ 。
(2)写出反应I中发生氧化还原反应的化学方程式:___________ 。
(3)调节pH=5的作用是除去___________ 。
(4)反应IV生成Li2CO3沉淀结束后,实验室中通常得到纯净的Li2CO3沉淀的操作名称蒸发浓缩,冷却结晶、___________ 、___________ 、干燥,为了提高所得Li2CO3沉淀的产率要使用___________ 洗涤(选填“热水”或“冷水”)。
(5)反应II加入碳酸钙,CaCO3是一种难溶物质,其Ksp=2.8×10-9。CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若混合前Na2CO3溶液的浓度为2.8 ×10—4mol/L,则生成沉淀所需原CaCl2溶液的最小浓度为___________ mol/L。

已知:①部分金属氢氧化物开始沉淀和完全沉淀时的pH:
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 2.7 | 3.7 | 9.6 |
| 完全沉淀pH | 3.7 | 4.7 | 11 |
| 温度/ °C | 0 | 10 | 20 | 50 | 75 | 100 |
| Li2CO3的溶解度/g | 1.539 | 1.406 | 1.329 | 1.181 | 0.866 | 0.728 |
(1)β-锂辉矿在处理前要粉碎,其主要目的是
(2)写出反应I中发生氧化还原反应的化学方程式:
(3)调节pH=5的作用是除去
(4)反应IV生成Li2CO3沉淀结束后,实验室中通常得到纯净的Li2CO3沉淀的操作名称蒸发浓缩,冷却结晶、
(5)反应II加入碳酸钙,CaCO3是一种难溶物质,其Ksp=2.8×10-9。CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若混合前Na2CO3溶液的浓度为2.8 ×10—4mol/L,则生成沉淀所需原CaCl2溶液的最小浓度为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网