解答题-原理综合题 适中0.65 引用1 组卷243
金属钛( )在航空航天、医疗器械等工业领域有着重要用途。回答下列问题:
)在航空航天、医疗器械等工业领域有着重要用途。回答下列问题:
(1)目前生产钛的方法之一是将金红石( )转化为
)转化为 ,再进一步还原
,再进一步还原 得到钛。
得到钛。 转化为
转化为 有直接氯化法和碳氯化法。在
有直接氯化法和碳氯化法。在 时反应的热化学方程式及其平衡常数如下:
时反应的热化学方程式及其平衡常数如下:
直接氯化: ,
,
碳氯化: ,
,
运用以上数据分析,你认为以上两个方法更优越的是__________ ,理由是__________ 。
(2)已知 ,
, 和
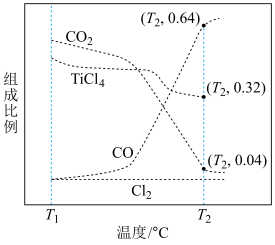
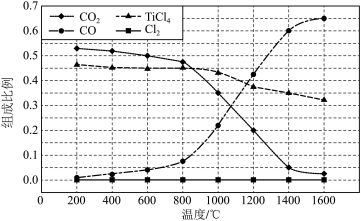
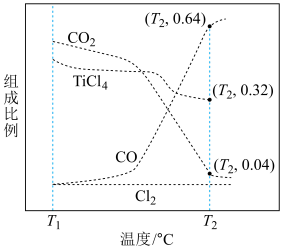
和 类似,只取决于反应体系的始态和终态。根据如图回答问题。
类似,只取决于反应体系的始态和终态。根据如图回答问题。

① 时,反应
时,反应
________ 自发进行(填“能”或“不能”)。
② 时,
时,
________  。
。
(3)钛酸锂是一种理想的嵌入型电极材料。某新型钛酸锂电池与普通石墨烯锂电池相比,电位比较高,安全性相较好,工作原理如图所示。
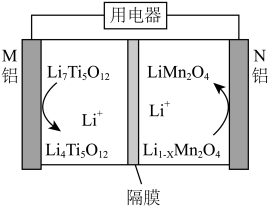
①电池的正极为______ (填“M”或“N”)
②放电时, 通过隔膜向
通过隔膜向______ 极(填“M”或“N”)移动。
③放电时,电极N的电极反应式为______ 。
(1)目前生产钛的方法之一是将金红石(
直接氯化:
碳氯化:
运用以上数据分析,你认为以上两个方法更优越的是
(2)已知

①
②
(3)钛酸锂是一种理想的嵌入型电极材料。某新型钛酸锂电池与普通石墨烯锂电池相比,电位比较高,安全性相较好,工作原理如图所示。

①电池的正极为
②放电时,
③放电时,电极N的电极反应式为
22-23高二上·福建南平·期末
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网