填空题 较易0.85 引用1 组卷142
比较下列微粒半径的大小(用“>”或“”填空):
(1)Na_____Mg_____Cl,______
(2)Li________Na_________K,______
(3)Na+______Mg2+________Al3+,______
(4)F-_____Cl-_________Br-,______
(5)Cl-______O2−______Na+____Mg2+,______
(6)Fe2+______ Fe3+
(1)Na_____Mg_____Cl,
(2)Li________Na_________K,
(3)Na+______Mg2+________Al3+,
(4)F-_____Cl-_________Br-,
(5)Cl-______O2−______Na+____Mg2+,
(6)Fe2+
2023高三·全国·专题练习
类题推荐
某同学探究元素的金属性、非金属性实验时,设计了一套实验方案,并记录了有关实验现象。请帮助他完成下列问题:
(1)由实验①②可知,金属性Na___ (填“>”或下“<”同)Mg。
(2)由实验③④可知,金属性Mg__ A1。
(3)由实验⑤可知,非金属性S___ C1,发生反应的离子方程式为__ 。
实验步骤 | 实验现象 |
| ①将一小块金属钠放入滴有酚酞溶液的冷水中 | 钠浮在水面上,熔成小球,四处游动,发出“嘶嘶”的响声,溶液变成红色 |
| ②将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 | 镁表面有细小气泡产生,溶液变成浅红色 |
| ③将用砂纸打磨过的镁条投入—定浓度的稀盐酸中 | 剧烈反应,迅速产生大量无色气体 |
| ④将用砂纸打磨过的铝条投入同体积同浓度的稀盐酸中 | 反应平缓,产生无色气体 |
| ⑤向新制的Na2S溶液中滴加新制氯水 | 生成淡黄色沉淀 |
(1)由实验①②可知,金属性Na
(2)由实验③④可知,金属性Mg
(3)由实验⑤可知,非金属性S
表是元素周期表的一部分,根据表中列出的10种元素,回答下列问题。
(1)单质化学性质最不活泼的是___ ;地壳中含量最多的元素是___ (填名称);
(2)单质常用作半导体材料的是___ ;Mg原子结构示意图为___ ;
(3)O和S中,原子半径较大的是;CH4和NH3中,热稳定性较强的是___ (填名称);
(4)新制氯水有漂白作用___ ,是因为其中含有___ (填“HCl”或“HClO”);
(5)元素最高价氧化物对应水化物中,碱性最强的是___ (填化学式),两性氢氧化物是___ ;
(6)某烃分子中含有6个碳原子,结构简式为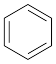 ,常用作有机溶剂。该有机物分子式为
,常用作有机溶剂。该有机物分子式为___ ,其中碳元素与氢元素的质量比m(C)∶m(H)=___ (相对原子质量:H-1 C-12)
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | C | N | O | Ne | ||||
| 3 | Na | Mg | Al | Si | S | Cl |
(2)单质常用作半导体材料的是
(3)O和S中,原子半径较大的是;CH4和NH3中,热稳定性较强的是
(4)新制氯水有漂白作用
(5)元素最高价氧化物对应水化物中,碱性最强的是
(6)某烃分子中含有6个碳原子,结构简式为
 ,常用作有机溶剂。该有机物分子式为
,常用作有机溶剂。该有机物分子式为组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


