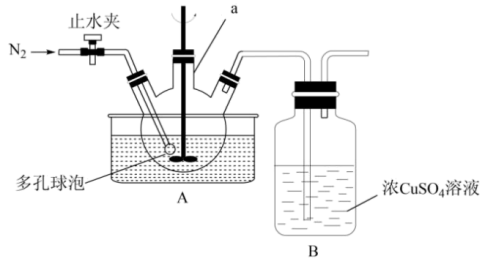
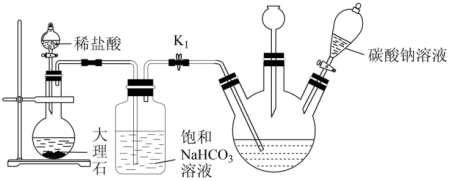
解答题-实验探究题 适中0.65 引用4 组卷478
醋酸铅[ ]常温下为白色固体,常温下易溶于水,难溶于乙醇、甲苯、四氯化碳等有机溶剂等。
]常温下为白色固体,常温下易溶于水,难溶于乙醇、甲苯、四氯化碳等有机溶剂等。 在制备时常常含有结晶水,形成
在制备时常常含有结晶水,形成 ,与水敏感化合物反应时,影响反应的产物。实验室用如下简易装置进行
,与水敏感化合物反应时,影响反应的产物。实验室用如下简易装置进行 脱水(加热装置省略),制备无水
脱水(加热装置省略),制备无水 。
。
二颈瓶中放入 和
和 甲苯,然后加热。当溶液温度为
甲苯,然后加热。当溶液温度为 时,固体全部溶解。加热至
时,固体全部溶解。加热至 时,开始有回流,分水器中溶液开始分层。
时,开始有回流,分水器中溶液开始分层。
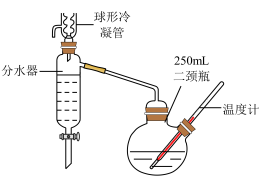
按要求回答下列问题:
(1)当_______ 时,脱水完成,可以停止加热。
(2)脱水完成,停止加热。烧瓶底部有大量白色粉末状固体析出,进一步获得无水 的操作为
的操作为_______ 。
(3)用 代替甲苯是否可行,理由是
代替甲苯是否可行,理由是_______ 。
(4)实验结束后,得白色粉末状固体的量为 ,则实验中无水
,则实验中无水 的产率为
的产率为_______ 。(用百分数表示)
(5)亚硫酸盐泛指二氧化硫和能产生二氧化硫的一类无机含硫化合物,具有漂白、抗氧化和防腐作用的食品添加剂,国标法中规定醋酸铅溶液用于蒸馏碘量法测定食品中亚硫酸盐的含量。此方法利用密闭容器中酸化样品并蒸馏,释放出其中的二氧化硫,用醋酸铅溶液吸收,然后在蒸馏后的溶液中依次加入盐酸、指示剂,再以碘标准溶液滴定。现利用 的碘标准溶液检验辣椒粉中亚硫酸盐的残留量。取
的碘标准溶液检验辣椒粉中亚硫酸盐的残留量。取 辣椒粉,进行上述操作,滴定平均消耗碘标准液
辣椒粉,进行上述操作,滴定平均消耗碘标准液 。
。
a.辣椒粉样品酸化时发生的离子方程式_______ ;
b.滴定操作中选择的指示剂为_______ ;
c.则辣椒粉中残留亚硫酸盐的含量_______  。(以
。(以 的质量进行计算,保留四位有效数字)
的质量进行计算,保留四位有效数字)
二颈瓶中放入

按要求回答下列问题:
(1)当
(2)脱水完成,停止加热。烧瓶底部有大量白色粉末状固体析出,进一步获得无水
(3)用
(4)实验结束后,得白色粉末状固体的量为
(5)亚硫酸盐泛指二氧化硫和能产生二氧化硫的一类无机含硫化合物,具有漂白、抗氧化和防腐作用的食品添加剂,国标法中规定醋酸铅溶液用于蒸馏碘量法测定食品中亚硫酸盐的含量。此方法利用密闭容器中酸化样品并蒸馏,释放出其中的二氧化硫,用醋酸铅溶液吸收,然后在蒸馏后的溶液中依次加入盐酸、指示剂,再以碘标准溶液滴定。现利用
a.辣椒粉样品酸化时发生的离子方程式
b.滴定操作中选择的指示剂为
c.则辣椒粉中残留亚硫酸盐的含量
2023·湖南·模拟预测
类题推荐
无水四氯化锡(SnCl4)常用作有机合成的氯化催化剂。实验室可用熔融的锡与氯气反应制备 SnCl4,装置如下图所示:
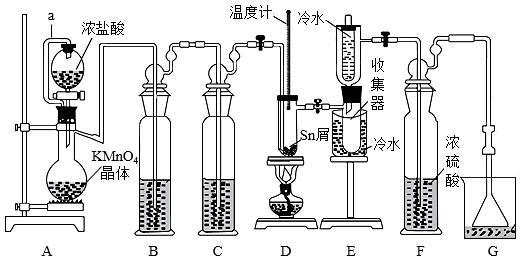
已知:①Sn、SnCl2、SnCl4有关的物理性质如下表:
②Sn的性质与Fe相似;SnCl4在空气中极易水解生成SnO2•xH2O;Cl2易溶于SnCl4。
回答下列问题:
(1)下列关于实验装置的说法正确的是____________ 。
A.整套实验装置先检漏,再连接,再添加药品,最后检查气密性
B.A 中盛放 KMnO4晶体的仪器名称为圆底烧瓶
C.B 中盛放饱和食盐水,C 中盛放浓硫酸,G 中盛放浓NaOH溶液
D.装置E中上方冷水的作用是冷凝回流SnCl4至收集器中
(2)当观察到装置F上方出现____________ 现象时才开始点燃酒精灯,待锡熔化后适当增大氯气流量,继续加热。此时继续加热的目的是____________ 。
(3)若上述装置中缺少装置 C(其它均相同),则 D 处具支试管中发生的主要副反应的化学方程式为________________________ 。
(4)收集器中收集到的液体略显黄色,原因是_________ ;提纯 SnCl4的方法是______ 。
A.加入 NaOH 萃取分液 B.加入足量锡再加热蒸馏
C.加入碘化钾冷凝过滤 D.加入饱和食盐水萃取
(5)经测定产品中含有少量的 SnCl2,可能的原因是____________ (用化学方程式表示)。 可用碘量法测定最后产品的纯度,发生如下反应:Sn2++I2=Sn4++2I-。准确称取一定样品放于锥形瓶中,加入少量浓盐酸溶解,再加水稀释,淀粉溶液作指示剂,用碘标准溶液滴定至终点,平行滴定三次后记录消耗标准液的平均体积。提示滴定到达终点的实验现象为____________ 。即使此法滴定的操作均正确,但测得的 SnCl4含量仍高于实际含量,其原因可能是____________ (用离子方程式表示,并配上必要的文字说明)。

已知:①Sn、SnCl2、SnCl4有关的物理性质如下表:
| 物质 | 熔点/oC | 沸点/oC | 颜色、状态 |
| Sn | 232 | 2260 | 银白色固体 |
| SnCl2 | 246 | 623 | 无色晶体 |
| SnCl4 | -30 | 114 | 无色液体 |
回答下列问题:
(1)下列关于实验装置的说法正确的是
A.整套实验装置先检漏,再连接,再添加药品,最后检查气密性
B.A 中盛放 KMnO4晶体的仪器名称为圆底烧瓶
C.B 中盛放饱和食盐水,C 中盛放浓硫酸,G 中盛放浓NaOH溶液
D.装置E中上方冷水的作用是冷凝回流SnCl4至收集器中
(2)当观察到装置F上方出现
(3)若上述装置中缺少装置 C(其它均相同),则 D 处具支试管中发生的主要副反应的化学方程式为
(4)收集器中收集到的液体略显黄色,原因是
A.加入 NaOH 萃取分液 B.加入足量锡再加热蒸馏
C.加入碘化钾冷凝过滤 D.加入饱和食盐水萃取
(5)经测定产品中含有少量的 SnCl2,可能的原因是
苯甲酸可用作食品防腐剂。实验室可通过甲苯氧化制苯甲酸,其反应原理如图:
实验步骤:
Ⅰ.向如图所示装置中加入甲苯、水和高锰酸钾,慢慢开启搅拌器,加热回流约 后停止加热并继续搅拌
后停止加热并继续搅拌 。
。 溶液,混合振荡,过滤、用少量热水洗涤滤渣。将含有苯甲酸钾
溶液,混合振荡,过滤、用少量热水洗涤滤渣。将含有苯甲酸钾 和甲苯的滤液按如下流程分离出苯甲酸和回收未反应的甲苯。
和甲苯的滤液按如下流程分离出苯甲酸和回收未反应的甲苯。 粗苯甲酸样品(杂质不与
粗苯甲酸样品(杂质不与 反应),配成溶液并置于
反应),配成溶液并置于 容量瓶中定容。移取
容量瓶中定容。移取 溶液,用
溶液,用 的
的 标准溶液滴定,平均消耗
标准溶液滴定,平均消耗 的
的 标准溶液。
标准溶液。
回答下列问题:
(1)由甲苯制得苯甲酸钾的反应类型为_______ 。
(2)仪器b的作用是_______ 。
(3)加入适量饱和亚硫酸氢钠溶液的目的是_______ ;该步骤中可以用来替代亚硫酸氢钠的是_______ (填字母)。
A. B.
B. C.
C.
(4)步骤Ⅱ中“用少量热水洗涤滤渣”中滤渣的主要成分是_______ 。
(5)下列说法不正确 的是_______。
(6)粗品中苯甲酸的质量分数为_______ 。

物质 | 相对分子质量 | 熔点/℃ | 沸点/℃ | 溶解性 |
甲苯 | 92 | 110.6 | 不溶于水,易溶于乙醇 | |
苯甲酸 | 122 | 122.4 | 248 | 微溶于冷水,易溶于乙醇、热水 |
Ⅰ.向如图所示装置中加入甲苯、水和高锰酸钾,慢慢开启搅拌器,加热回流约


回答下列问题:
(1)由甲苯制得苯甲酸钾的反应类型为
(2)仪器b的作用是
(3)加入适量饱和亚硫酸氢钠溶液的目的是
A.
(4)步骤Ⅱ中“用少量热水洗涤滤渣”中滤渣的主要成分是
(5)下列说法
| A.操作①是分液,操作②是蒸馏 |
| B.无色液体A是甲苯,白色固体是B苯甲酸 |
| C.为了得到更多的白色固体B,冷却结晶时温度越低越好 |
| D.可通过多次重结晶以提高苯甲酸的纯度 |
(6)粗品中苯甲酸的质量分数为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网