解答题-工业流程题 较难0.4 引用1 组卷329
镍钛钯废靶材含钛55%、镍25%、钯18%和杂质铝2%。从镍钛钯废靶材回收有关金属的工艺流程如下:
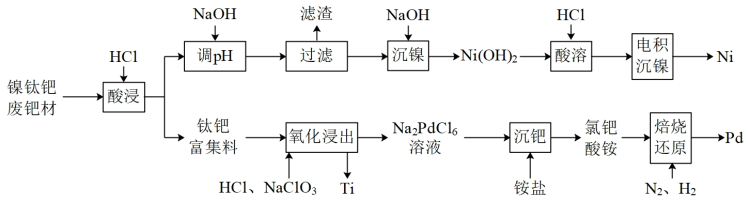
已知:Ⅰ.常温下,钛与钯均不溶于盐酸。
Ⅱ. 在溶液中存在配位平衡:
在溶液中存在配位平衡:
回答下列问题:
(1)镍元素在周期表中的位置为_______ ,请写出其基态原子的核外电子排布式_______ 。
(2)“调pH”除铝、钛时,pH对溶液中金属离子质量浓度影响如下表,根据表中数据判断除铝、钛时pH应调节至_______ 为宜。
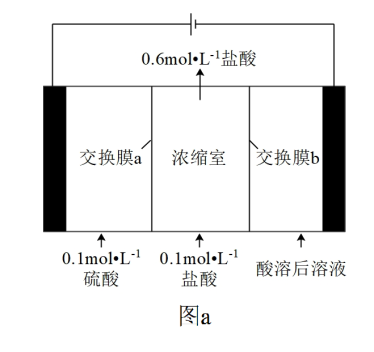
(3)“酸溶”所得溶液,经电积可得单质镍,电积沉镍装置如图a所示。电积装置中,交换膜b应为_______ 离子交换膜(填“阳”或“阴”)。电解时浓缩室溶液体积保持不变,当浓缩室得到 的盐酸时,阴极得到Ni的质量小于14.75g,其原因为
的盐酸时,阴极得到Ni的质量小于14.75g,其原因为_______ 。
(4)“氧化浸出”时,钯(Pd)被氧化生成配位离子 的离子方程式为
的离子方程式为_______ 。
(5)“沉钯”时,温度保持在55~65℃,温度不易过高,其原因除防止铵盐分解外,还有_______ 。“沉钯”时,铵盐最好选用_______ (填该物质的电子式),有利于钯的沉淀。
(6)氯钯酸铵 在“焙烧还原”时所用石英管冷凝壁上有大量白色固体析出,该固体可在
在“焙烧还原”时所用石英管冷凝壁上有大量白色固体析出,该固体可在_______ 操作中循环使用(填操作单元名称)。

已知:Ⅰ.常温下,钛与钯均不溶于盐酸。
Ⅱ.
回答下列问题:
(1)镍元素在周期表中的位置为
(2)“调pH”除铝、钛时,pH对溶液中金属离子质量浓度影响如下表,根据表中数据判断除铝、钛时pH应调节至
| pH | 溶液中金属离子质量浓度( | ||
| 1.1 | 6100 | 7780 | 46 |
| 2.1 | 5960 | 7430 | 3 |
| 3.4 | 212 | 6080 | 1 |
| 4.2 | 202 | 5870 | 1 |
| 5.2 | 107 | 3720 | 1 |

(3)“酸溶”所得溶液,经电积可得单质镍,电积沉镍装置如图a所示。电积装置中,交换膜b应为
(4)“氧化浸出”时,钯(Pd)被氧化生成配位离子
(5)“沉钯”时,温度保持在55~65℃,温度不易过高,其原因除防止铵盐分解外,还有
(6)氯钯酸铵
22-23高三下·河北石家庄·开学考试
类题推荐
一种从废钼催化剂(主要成分为MoO3、MoS2,含少量CoO、CoS、NiO、Fe2O3等)中回收有价值金属的工艺流程如图。
②溶液中金属离子开始沉淀和完全沉淀的pH如表:
③钼酸铵[(NH4)2MoO4]为白色晶体,具有很高的水溶性,不溶于乙醇。
回答下列问题:
(1)催化剂中含多种金属元素,其中铁在元素周期表中的位置:第______ 周期第_____ 族。基态Co原子的价电子排布式为______ 。
(2)钼酸铵[(NH4)2MoO4]中Mo元素的化合价为______ ;“焙烧”时MoS2转化为MoO3,该反应的化学方程式为______ 。
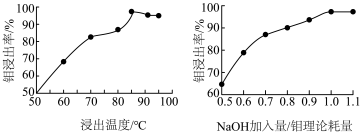
(3)“碱浸”时,浸出温度、NaOH加入量/钼理论耗量对钼浸出率的影响如图。______ 、NaOH加入量/钼理论耗量______ 。
(4)“除铁”时应调节溶液pH的范围为_______ 。
(5)若“沉钴镍”时调节溶液pH=9.5,则此时溶液中p =
=______ (pX=-lgX)。
(6)经过降温结晶、过滤、洗涤、干燥等操作得到(NH4)2MoO4•7H2O晶体,洗涤时所选用的最佳试剂为______ 。

②溶液中金属离子开始沉淀和完全沉淀的pH如表:
| 金属离子 | Fe3+ | Co2+ | Ni2+ |
| 开始沉淀时的pH | 2.2 | 6.4 | 7.2 |
| 沉淀完全时(c=1.0×10-5mol•L-1)的pH | 3.2 | 9.0 | 8.7 |
回答下列问题:
(1)催化剂中含多种金属元素,其中铁在元素周期表中的位置:第
(2)钼酸铵[(NH4)2MoO4]中Mo元素的化合价为
(3)“碱浸”时,浸出温度、NaOH加入量/钼理论耗量对钼浸出率的影响如图。
(4)“除铁”时应调节溶液pH的范围为
(5)若“沉钴镍”时调节溶液pH=9.5,则此时溶液中p
(6)经过降温结晶、过滤、洗涤、干燥等操作得到(NH4)2MoO4•7H2O晶体,洗涤时所选用的最佳试剂为
粗铜精炼废渣的主要成分为Co、Ca、Al、Zn、Cu、Fe等元素的化合物。为节约和利用资源,减轻废渣对环境的危害,常温下通过如下工艺流程回收Co、Zn、Cu等。
①该工艺条件下,溶液中金属离子开始沉淀和完全沉淀 时的pH如表所示:
时的pH如表所示:
②“酸浸氧化”时Co2+未被氧化, 与空气接触能被氧化;
与空气接触能被氧化;
③ 。
。
回答下列问题:
(1)“酸浸氧化”中,金属元素转化为相应的硫酸盐,其中NaClO3的作用为_______ (用离子方程式表示)。
(2)滤渣①中铁的存在形式为黄钠铁矾 ,用氧化物形式可表示为
,用氧化物形式可表示为_______ 。除铁沉淀外,滤渣①中还含有_______ (填化学式)。
(3)“沉铝”时,保持pH=4.7,为了提高沉淀分离的效率,可通过_______ 操作使铝的沉淀颗粒长大,防止胶体生成。
(4)“水解共沉”后,滤液③中主要含有的金属离子是Co2+、Na+、_______ ,其中Co2+浓度为_______ mol·L-1.
(5)“酸溶”时,有少量不易溶于稀硫酸的 存在,请用化学方程式解释
存在,请用化学方程式解释 产生的原因:
产生的原因:_______ 。
(6)“沉钴”时需控制溶液pH,请解释pH不宜过大或过小的原因:_______ 。

①该工艺条件下,溶液中金属离子开始沉淀和完全沉淀
| 金属离子 | Fe3+ | Fe2+ | Al3+ | Co2+ | Ca2+ | Zn2+ | Cu2+ |
| 开始沉淀时的pH | 1.2 | 7.0 | 3.5 | 6.6 | 11.7 | 5.4 | 4.9 |
| 完全沉淀时的pH | 3.2 | 9.0 | 4.7 | 9.1 | 13.9 | 8.0 | 6.7 |
③
回答下列问题:
(1)“酸浸氧化”中,金属元素转化为相应的硫酸盐,其中NaClO3的作用为
(2)滤渣①中铁的存在形式为黄钠铁矾
(3)“沉铝”时,保持pH=4.7,为了提高沉淀分离的效率,可通过
(4)“水解共沉”后,滤液③中主要含有的金属离子是Co2+、Na+、
(5)“酸溶”时,有少量不易溶于稀硫酸的
(6)“沉钴”时需控制溶液pH,请解释pH不宜过大或过小的原因:
废三元锂离子电池中含有镍、钻、锰、锂、铝等金属元素,是重要的二次资源。由某18650型废三元锂离子电池回收镍、钻、锰的工艺流程如下图所示:
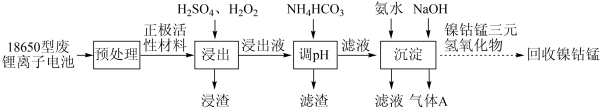
已知:①浸出液中各金属离子的质量浓度如下表。
② 能与
能与 、
、 、
、 形成配合物。
形成配合物。
Ⅰ.回答下列问题:
(1)“浸出”后得到浸出液的操作是___________ 。
(2)正极活性材料中的 在“浸出”过程中转化的化学方程式为
在“浸出”过程中转化的化学方程式为___________ 。
(3)镍、钴、锰的浸出率随时间、温度的变化如图1、图2所示。
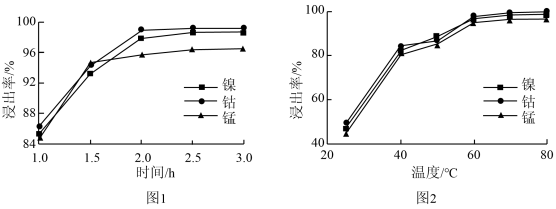
①综合考虑,选择浸出时间为___________ 。
②选择浸出温度范围为60-70℃,理由是___________ 。
(4)“调pH”中有沉淀生成,生成沉淀反应的离子方程式为___________ 。
(5)“沉淀”中气体A为___________ (填化学式)。沉淀后,分离获得镍钴锰三元氢氧化物沉淀并多次洗涤,判断沉淀洗净的方法是___________ 。
(6)已知25℃时,部分物质的溶度积常数如下:
要使滤液中 、
、 、
、 沉淀完全(通常认为溶液中离子浓度小于
沉淀完全(通常认为溶液中离子浓度小于 为沉淀完全)的pH应大于
为沉淀完全)的pH应大于___________ ( ,
, )。
)。
Ⅱ.“氢能”是21世纪的绿色能源,研发新型储氢材料是开发利用氢能的重要研究方向。
(7) 是一种储氢材料,可由
是一种储氢材料,可由 和
和 反应制得。
反应制得。
①基态 的未成对电子数有
的未成对电子数有___________ 个。
② 晶体由
晶体由 和
和 构成,
构成, 中B原子的杂化方式为
中B原子的杂化方式为___________ , 离子的空间构型为
离子的空间构型为___________ , 晶体含有的化学键有
晶体含有的化学键有___________ (填标号)。
A.离子键 B.极性键 C.非极性键 D配位键 E.金属键
(8)某储氢材料是第三周期金属元素M的氢化物,M的部分电离能如下表所示:
M是___________ (填元素符号),判断理由为___________ 。
(9)镧镍合金也是一种重要储氢材料。某种镧镍合金储氢后的晶胞结构如图所示,其化学式为___________ 。


已知:①浸出液中各金属离子的质量浓度如下表。
| 金属离子 | |||||
| 质量浓度( | 1600 | 5144 | 1495 | 842 | 254 |
Ⅰ.回答下列问题:
(1)“浸出”后得到浸出液的操作是
(2)正极活性材料中的
(3)镍、钴、锰的浸出率随时间、温度的变化如图1、图2所示。

①综合考虑,选择浸出时间为
②选择浸出温度范围为60-70℃,理由是
(4)“调pH”中有沉淀生成,生成沉淀反应的离子方程式为
(5)“沉淀”中气体A为
(6)已知25℃时,部分物质的溶度积常数如下:
| 物质 | |||
Ⅱ.“氢能”是21世纪的绿色能源,研发新型储氢材料是开发利用氢能的重要研究方向。
(7)
①基态
②
A.离子键 B.极性键 C.非极性键 D配位键 E.金属键
(8)某储氢材料是第三周期金属元素M的氢化物,M的部分电离能如下表所示:
| 738 | 1451 | 7733 | 10540 | 13630 |
(9)镧镍合金也是一种重要储氢材料。某种镧镍合金储氢后的晶胞结构如图所示,其化学式为

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


