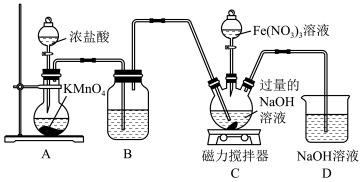
单选题 较易0.85 引用1 组卷140
高铁酸钾是一种高效的绿色消毒剂。实验室模拟湿法制备高铁酸钾晶体的流程如下:
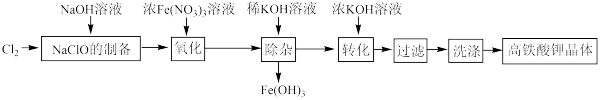
已知:① 可溶于水,强碱性溶液中较稳定,酸性、弱碱性时不稳定。
可溶于水,强碱性溶液中较稳定,酸性、弱碱性时不稳定。
② 溶解度小于
溶解度小于
下列说法错误的是

已知:①
②
下列说法错误的是
| A.制备NaClO过程中,每生成1 mol NaClO,理论消耗 |
| B.“氧化”过程中,发生反应 |
| C.用KOH代替NaOH有利于提高 |
| D.取最后一次洗涤液,加入稀 |
22-23高二上·山东日照·期末
类题推荐
高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,湿法制备高铁酸钾的工艺流程如下。下列说法正确的是
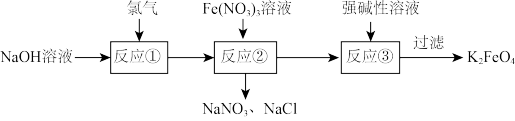

| A.若反应①产物n(NaC1O):n(NaClO3)=5:1,则n(NaCl):n(NaClO)=2:1 |
| B.反应②中Fe(NO3)3体现还原性 |
| C.反应③用NaOH溶液作强碱性溶液 |
| D.理论上,6.72L(STP)Cl2参加反应可得到0.1molK2FeO4 |
高铁酸钾是一种高效多功能的新型非氯绿色消毒剂,主要用于饮用水处理。工业上制备K2FeO4的方法:向KOH溶液中通入氯气,然后再加入Fe(NO3)3溶液:
①Cl2+KOH→KCl+KClO+KClO3+H2O(未配平);
②2Fe(NO3)3+3KClO+10KOH=2K2FeO4+6KNO3+3KCl+5H2O。
下列说法不正确的是
①Cl2+KOH→KCl+KClO+KClO3+H2O(未配平);
②2Fe(NO3)3+3KClO+10KOH=2K2FeO4+6KNO3+3KCl+5H2O。
下列说法不正确的是
| A.K2FeO4在消毒杀菌过程中还可以净水 |
| B.若反应①中n(ClO-):n( |
| C.反应①中每消耗4 mol KOH,吸收44.8 L Cl2 |
| D.若反应①的氧化产物只有KClO,则得到0.2 mol K2FeO4时最少消耗0.3 mol Cl2 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网