解答题-结构与性质 0.65 引用4 组卷635
碳、氮、氧元素的单质及化合物在很多领域有着广泛的应用。回答下列问题:
(1)基态N原子价电子排布式为_______ ;C、N、O的第一电离能由小到大的顺序是_______ 。
(2)N2F2(二氟氮烯)分子中的氮原子采用sp2杂化,则N2F2的结构式为_______ 。
(3) 、
、 、
、 的键角由大到小的顺序为
的键角由大到小的顺序为_______ 。
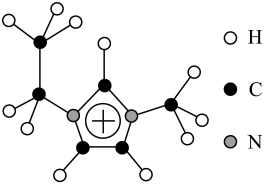
(4)由H、C、N组成的EMIM+结构如图,其环上所有原子共平面。大π键可用符号 表示,其中m表示参与形成大π键的原子数,n表示形成大π键的电子数,EMIM+中的大π键应表示为
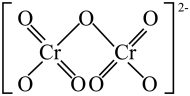
表示,其中m表示参与形成大π键的原子数,n表示形成大π键的电子数,EMIM+中的大π键应表示为_______ 。为使EMIM+以单个形式存在从而获得良好的溶解性,应避免与N原子相连的-CH3、-CH2CH3被H原子替代,其原因是_______ 。 的结构如图。1mol(NH4)2Cr2O7中σ键数目为
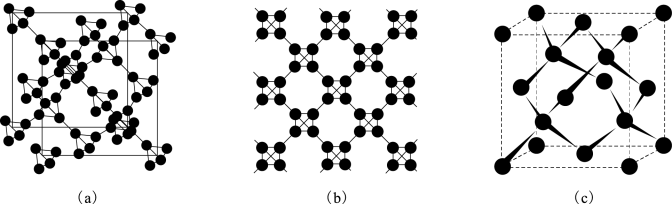
的结构如图。1mol(NH4)2Cr2O7中σ键数目为_______ NA。_______ 个碳原子,T-碳的密度为金刚石的一半,则T-碳晶胞和金刚石晶胞的棱长之比为_______ 。
(1)基态N原子价电子排布式为
(2)N2F2(二氟氮烯)分子中的氮原子采用sp2杂化,则N2F2的结构式为
(3)
(4)由H、C、N组成的EMIM+结构如图,其环上所有原子共平面。大π键可用符号
22-23高三上·山东德州·期末


