填空题 适中0.65 引用4 组卷300
为深刻理解强电解质和弱电解质的概念,某小组以室温下2mL2mol/L盐酸和2mL2mol/L醋酸为例,设计了如下角度对比分析。已知室温下醋酸的 ;
; 。请按要求回答下列问题。
。请按要求回答下列问题。
(1)写出 的电离方程式:
的电离方程式:_______ 。
(2)上述盐酸、醋酸中 分别为2mol/L、
分别为2mol/L、_______ 。
(3)室温下,在上述盐酸、醋酸中分别滴入1mol/L 溶液,观察到二者都有气泡冒出。可预测:
溶液,观察到二者都有气泡冒出。可预测:
_______  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(4)将上述盐酸、醋酸用注射器分别注入到各盛有0.03gMg条的两个锥形瓶中,塞紧橡胶塞。测得锥形瓶内气体的压强随时间的变化如图所示。
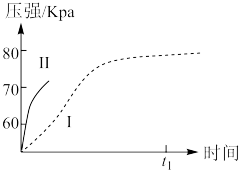
①能表示醋酸参与反应的曲线为_______ (填编号)。
②在图将曲线Ⅱ补充画至 
时刻 _______ 。
(5)分别向盛有上述盐酸、醋酸的烧杯中加2mL水,忽略混合溶液体积变化。则稀释后的盐酸、醋酸溶液中的 分别为
分别为_______ mol/L、_______ mol/L。
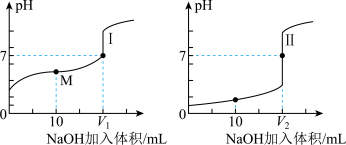
(6)中和上述醋酸溶液,需滴入2mol/LNaOH溶液的体积为_______ mL。当醋酸被中和至50%时,溶液中除 外各种粒子浓度由大到小的顺序为
外各种粒子浓度由大到小的顺序为_______ 。
(1)写出
(2)上述盐酸、醋酸中
(3)室温下,在上述盐酸、醋酸中分别滴入1mol/L
(4)将上述盐酸、醋酸用注射器分别注入到各盛有0.03gMg条的两个锥形瓶中,塞紧橡胶塞。测得锥形瓶内气体的压强随时间的变化如图所示。

①能表示醋酸参与反应的曲线为
②在图将曲线Ⅱ
(5)分别向盛有上述盐酸、醋酸的烧杯中加2mL水,忽略混合溶液体积变化。则稀释后的盐酸、醋酸溶液中的
(6)中和上述醋酸溶液,需滴入2mol/LNaOH溶液的体积为
21-22高二上·天津河西·期末
类题推荐
某小组以盐酸、醋酸为例探究其酸性的强弱。按要求回答下列问题。
(1)取相同体积、相同浓度的盐酸和醋酸,分别测其pH和导电能力,对比分析,在下表填写空白。已知:
③此温度下,CH3COOH的电离平衡常数Ka=___________ (填计算式,不化简)。
(2)在上述醋酸溶液中加入如下表所示物质,分析其中粒子的变化等,填写空白。
(3)向两个锥形瓶中各加入0.06g镁条,塞紧橡胶塞,然后用注射器分别注入2mL 2mol/L盐酸、2mol/L醋酸。
①反应前n(Mg)=___________ mol;充分反应后,剩余的n(Mg)=___________ mol。
②两锥形瓶内气体n随时间变化,对比分析后,在如下坐标中将示意曲线补充完整。___________

(1)取相同体积、相同浓度的盐酸和醋酸,分别测其pH和导电能力,对比分析,在下表填写空白。已知:
| 酸 | 0.1mol/L盐酸 | 0.1mol/L醋酸 | |
| pH(25℃) | 1 | 3 | |
| 导电能力 | 强 | 弱 | |
| 分析与结论 | ①微观解释(写出溶质在溶液中的存在形式,填粒子的化学式) | ||
| ②电离方程式 | |||
(2)在上述醋酸溶液中加入如下表所示物质,分析其中粒子的变化等,填写空白。
| 加入少量的物质 | 醋酸电离平衡移动方向 填“→”“←”或“不移动” | c(H⁺)/c(CH3COOH)比值变化 填“变大”“变小”或“不变” |
| ①CH3COONa(s) | ||
| ②水 |
(3)向两个锥形瓶中各加入0.06g镁条,塞紧橡胶塞,然后用注射器分别注入2mL 2mol/L盐酸、2mol/L醋酸。
①反应前n(Mg)=
②两锥形瓶内气体n随时间变化,对比分析后,在如下坐标中将示意曲线补充完整。

化学中,酸的电离平衡常数( )是评估酸性强弱的重要依据。几种酸的电离常数(25℃)如下表所示。
)是评估酸性强弱的重要依据。几种酸的电离常数(25℃)如下表所示。
回答下列问题:
(1)写出CH3COOH的电离方程式:_____ 。
(2)T℃下,CH3COOH的电离平衡常数值为 ,则T
,则T_____ 25℃(填“>”、“<”或“=”)。估算T℃下,0.1mol/LCH3COOH溶液中
_____ 。保持温度不变,将该溶液加水稀释至0.01mol/L,在稀释过程中,
_____ (填“增大”、“减小”或“不变”)。
(3)根据以上数据,写出将少量CO2通入NaClO溶液发生反应的离子方程式:_____ 。
(4)向相同的两个密闭容器中加入0.05g镁条,分别注入2mL2mol/L盐酸、2mL2mol/L醋酸,测得容器内压强随时间变化如图所示。反应为醋酸的曲线是_____ (填字母)。

| 酸 | CH3COOH | H2CO3 | HClO |
(1)写出CH3COOH的电离方程式:
(2)T℃下,CH3COOH的电离平衡常数值为
(3)根据以上数据,写出将少量CO2通入NaClO溶液发生反应的离子方程式:
(4)向相同的两个密闭容器中加入0.05g镁条,分别注入2mL2mol/L盐酸、2mL2mol/L醋酸,测得容器内压强随时间变化如图所示。反应为醋酸的曲线是

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网