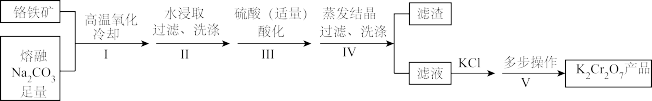解答题-工业流程题 适中0.65 引用1 组卷135
科研团队设计用含有少量 的铬铁矿[
的铬铁矿[ ]制备
]制备 晶体,流程如下:
晶体,流程如下:
已知:特定温度NaCl和 的溶解度如下表:
的溶解度如下表:
请回答:
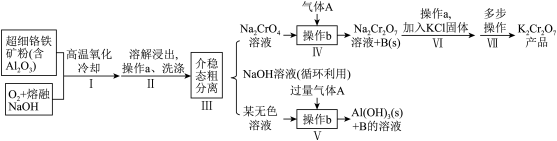
(1)步骤Ⅰ,将矿石制成超细铬铁矿粉有利于加快高温氧化的速率,其理由是___________ 。
(2)步骤Ⅱ中操作a的名称为___________ ,若分离出的固体主要含有 ,高温氧化过程中氧化剂与还原剂物质的量之比为
,高温氧化过程中氧化剂与还原剂物质的量之比为___________ 。
(3)物质B是侯氏制碱法的重要中间产物,则步骤Ⅳ中发生反应的离子方程式为:___________ ,可观察到溶液由黄色变为___________ 。
(4)步骤Ⅴ中如果使用稀硫酸替代“过量气体A”,同时希望“某无色溶液”中的铝元素全部以 形式存在,则合适的pH范围是
形式存在,则合适的pH范围是___________ <pH<7.7.(通常认为溶液中的离子浓度小于 为沉淀完全;
为沉淀完全; ,已知
,已知 )
)
(5)步骤Ⅶ,为了得到杂质较少的 产品,从下列选项中选出合理的操作(操作不能重复使用)并排序:
产品,从下列选项中选出合理的操作(操作不能重复使用)并排序:___________ 。
溶解加入的KCl→蒸发溶剂→___________→___________→___________→重结晶。
a、蒸发至溶液中出现大量晶体,停止加热
b、蒸发至溶液出现晶膜,停止加热
c、减压过滤
d、冷却至室温

已知:特定温度NaCl和
| 溶解度/g | 10℃ | 20℃ | 30℃ | 60℃ | 80℃ |
| NaCl | 35.8 | 35.9 | 36.1 | 37.1 | 38.0 |
| 7.0 | 12.3 | 18.1 | 45.6 | 73.0 |
(1)步骤Ⅰ,将矿石制成超细铬铁矿粉有利于加快高温氧化的速率,其理由是
(2)步骤Ⅱ中操作a的名称为
(3)物质B是侯氏制碱法的重要中间产物,则步骤Ⅳ中发生反应的离子方程式为:
(4)步骤Ⅴ中如果使用稀硫酸替代“过量气体A”,同时希望“某无色溶液”中的铝元素全部以
(5)步骤Ⅶ,为了得到杂质较少的
溶解加入的KCl→蒸发溶剂→___________→___________→___________→重结晶。
a、蒸发至溶液中出现大量晶体,停止加热
b、蒸发至溶液出现晶膜,停止加热
c、减压过滤
d、冷却至室温
22-23高二上·湖北·期末
类题推荐
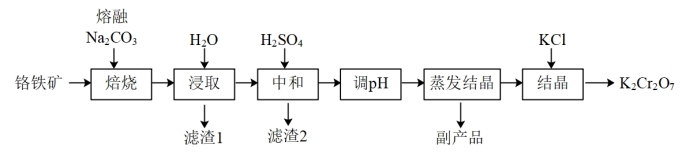
某兴趣小组用铬铁矿[Fe(CrO2)2] 制备K2Cr2O7晶体,流程如下: 8Na2CrO4+4NaFeO2+10CO2
8Na2CrO4+4NaFeO2+10CO2
2H++2CrO
 Cr2O
Cr2O +H2O
+H2O
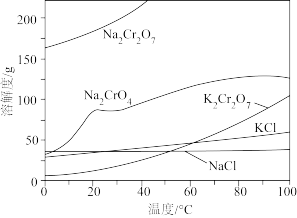
相关物质的溶解度随温度变化如下图。
(1)步骤I,将铬铁矿粉碎有利于加快高温氧化的速率,其理由是___ 。
(2)下列说法正确的是___________。
(3)步骤V,重结晶前,为了得到杂质较少的K2Cr2O7粗产品,从下列选项中选出合理的操作(操作不能重复使用)并排序:溶解KCl→___ (______)→(______)→(_____)→(_____)→重结晶。
a.50℃蒸发溶剂;b.100 ℃蒸发溶剂;c.抽滤;d.冷却至室温;e.蒸发至溶液出现晶膜,停止加热;f.蒸发至溶液中出现大量晶体,停止加热。

2H++2CrO
相关物质的溶解度随温度变化如下图。

(1)步骤I,将铬铁矿粉碎有利于加快高温氧化的速率,其理由是
(2)下列说法正确的是___________。
| A.步骤II,低温可提高浸取率 |
| B.步骤II,过滤可除去NaFeO2水解产生的Fe(OH)3 |
| C.步骤III,酸化的目的主要是使Na2CrO4转变为Na2Cr2O7 |
| D.步骤IV,所得滤渣的主要成分是Na2SO4和Na2CO3 |
a.50℃蒸发溶剂;b.100 ℃蒸发溶剂;c.抽滤;d.冷却至室温;e.蒸发至溶液出现晶膜,停止加热;f.蒸发至溶液中出现大量晶体,停止加热。
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网