解答题-实验探究题 适中0.65 引用2 组卷308
明矾 可做中药,性味酸涩、寒、有毒。利用废铝制备明矾,并测定其组成,实验过程如下。
可做中药,性味酸涩、寒、有毒。利用废铝制备明矾,并测定其组成,实验过程如下。
Ⅰ.制备明矾
实验步骤如图:
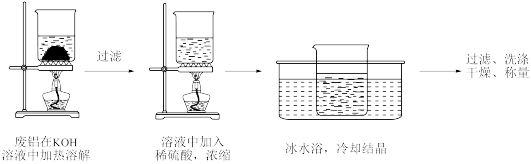
(1)溶解步骤中主要发生的离子反应方程式为_______ 。
(2)用蒸馏水洗涤晶体的操作过程是_______ 。
(3)生活中明矾可用作净水剂,结合离子方程式说明净水原理:_______ 。
Ⅱ.样品中硫酸根的测定
(一)绘制标准硫酸钡悬浊液吸光光谱图
①分别量取0、1.0、2.0、3.0、4.0mL浓度为500μg/mL的标准硫酸钾溶液移入10mL的比色管中,然后分别加入5mL浓度为1g/mL的 溶液,用蒸馏水定容。
溶液,用蒸馏水定容。
②用分光光度计测量标准系列(波长采用420nm),数据如下(忽略混合过程中的体积变化)。
③绘制硫酸钡悬浊液的吸光光谱图,绘制如下。
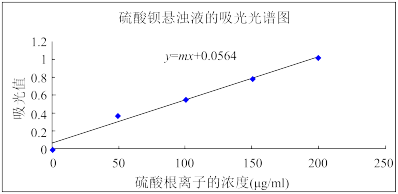
(4)上述实验数据中b=_______ ,m=_______ (保留1位有效数字)。
(二)测定样品中硫酸根浓度
①称取1.018g样品晶体配制成250mL的样品溶液。
②量取1.0mL样品溶液移入10mL的比色管中,然后加入5mL浓度为1g/mL的 溶液,用蒸馏水定容,测得样品的吸光值为0.858。
溶液,用蒸馏水定容,测得样品的吸光值为0.858。
(5)测得样品中硫酸根的质量分数为_______ %(保留2位有效数字)。
(6)实验测得硫酸根的含量小于理论值,可能的原因有_______(填标号)。
Ⅰ.制备明矾
实验步骤如图:

(1)溶解步骤中主要发生的离子反应方程式为
(2)用蒸馏水洗涤晶体的操作过程是
(3)生活中明矾可用作净水剂,结合离子方程式说明净水原理:
Ⅱ.样品中硫酸根的测定
(一)绘制标准硫酸钡悬浊液吸光光谱图
①分别量取0、1.0、2.0、3.0、4.0mL浓度为500μg/mL的标准硫酸钾溶液移入10mL的比色管中,然后分别加入5mL浓度为1g/mL的
②用分光光度计测量标准系列(波长采用420nm),数据如下(忽略混合过程中的体积变化)。
| 1.0 | 2.0 | 3.0 | 4.0 | ||
| 蒸馏水体积(mL) | 5 | a | b | c | 1 |
| 0 | 50 | 100 | 150 | 200 | |
| 吸光值A | 0 | 0.371 | 0.553 | 0.778 | 1.013 |

(4)上述实验数据中b=
(二)测定样品中硫酸根浓度
①称取1.018g样品晶体配制成250mL的样品溶液。
②量取1.0mL样品溶液移入10mL的比色管中,然后加入5mL浓度为1g/mL的
(5)测得样品中硫酸根的质量分数为
(6)实验测得硫酸根的含量小于理论值,可能的原因有_______(填标号)。
| A.实验Ⅰ制得样品中有 | B.实验中所用标准硫酸钾溶液浓度偏大 |
| C.样品溶液配制过程中,定容仰视读数 | D.样品溶液配制过程中,容量瓶未润洗 |
22-23高三下·湖南长沙·阶段练习
类题推荐
某小组以废铁屑(久置但未生锈)为原料制备Fe(NO3)3,并利用配制的Fe(NO3)3标准溶液对“硫酸亚铁补铁剂”中铁元素的含量进行测定,实验过程如下:
【实验Ⅰ】Fe(NO3)3·9H2O的制备___________ ;稀硝酸要足量的目的有:①确保铁元素转化成Fe3+,②___________ 。
(2)操作A为在足量稀硝酸存在下蒸发浓缩、冷却结晶、过滤、洗涤、干燥。操作A需要用到的玻璃仪器有烧杯、漏斗、酒精灯、干燥器、___________ 。
【实验Ⅱ】标准Fe(NO3)3溶液的配制。
准确称取0.8080g Fe(NO3)3·9H2O配成100mL 0.02000mol/L溶液。
(3)下列操作会导致所配Fe(NO3)3溶液浓度偏低的是___________(填字母)。
【实验Ⅲ】绘制Fe3+标准溶液与吸光度A(对特定波长光的吸收程度,数值与有色物质的浓度大小有关)的标准曲线。
①分别向6个100mL容量瓶中加入0.50、0.75、1.00、1.25、1.50、2.00mL实验Ⅱ中标定的浓度为0.0200mol·L-1的Fe(NO3)3标准溶液,然后分别加入1.50mL某浓度KSCN溶液,用蒸馏水定容。
②将配好的溶液加入10mL比色皿中,分别测定其吸光度,所得数据如下表所示:
___________ ,b=___________ 。
【实验Ⅳ】“硫酸亚铁补铁剂”中铁元素含量的测定
①取1.000g补铁剂样品,溶解后再加入足量H2O2溶液充分反应后配成100mL溶液。
②取1.0mL上一步所配溶液于100mL容量瓶中,加入1.50mL某浓度KSCN溶液,用蒸馏水定容。
③将最终配好的溶液加到10mL比色皿中,在与【实验Ⅲ】步骤②中相同条件下测得溶液吸光度A=0.35。
(5)“硫酸亚铁补铁剂”中铁元素的质量分数为___________ %。
(6)下列操作中有利于更准确测得补铁剂中的铁元素含量的有___________(填字母)。
【实验Ⅰ】Fe(NO3)3·9H2O的制备

(2)操作A为在足量稀硝酸存在下蒸发浓缩、冷却结晶、过滤、洗涤、干燥。操作A需要用到的玻璃仪器有烧杯、漏斗、酒精灯、干燥器、
【实验Ⅱ】标准Fe(NO3)3溶液的配制。
准确称取0.8080g Fe(NO3)3·9H2O配成100mL 0.02000mol/L溶液。
(3)下列操作会导致所配Fe(NO3)3溶液浓度偏低的是___________(填字母)。
| A.溶液未恢复室温就注入容量瓶定容 |
| B.定容时俯视液面 |
| C.摇匀后发现液面低于刻度线,于是加水至刻度线 |
| D.容量瓶底部残留少量的蒸馏水而未做干燥处理 |
【实验Ⅲ】绘制Fe3+标准溶液与吸光度A(对特定波长光的吸收程度,数值与有色物质的浓度大小有关)的标准曲线。
①分别向6个100mL容量瓶中加入0.50、0.75、1.00、1.25、1.50、2.00mL实验Ⅱ中标定的浓度为0.0200mol·L-1的Fe(NO3)3标准溶液,然后分别加入1.50mL某浓度KSCN溶液,用蒸馏水定容。
②将配好的溶液加入10mL比色皿中,分别测定其吸光度,所得数据如下表所示:
| 比色管编号 | S1 | S2 | S3 | S4 | S₅ | S6 |
| Fe(NO3)3溶液/mL | 0.50 | 0.75 | 1.00 | 1.25 | 1.50 | 2.00 |
| c(Fe3+)/(10-4mol·L-1) | 1 | 1.5 | 2 | 2.5 | 3 | 4 |
| 吸光度A | 0.12 | 0.17 | 0.22 | 0.27 | 0.32 | 0.42 |

【实验Ⅳ】“硫酸亚铁补铁剂”中铁元素含量的测定
①取1.000g补铁剂样品,溶解后再加入足量H2O2溶液充分反应后配成100mL溶液。
②取1.0mL上一步所配溶液于100mL容量瓶中,加入1.50mL某浓度KSCN溶液,用蒸馏水定容。
③将最终配好的溶液加到10mL比色皿中,在与【实验Ⅲ】步骤②中相同条件下测得溶液吸光度A=0.35。
(5)“硫酸亚铁补铁剂”中铁元素的质量分数为
(6)下列操作中有利于更准确测得补铁剂中的铁元素含量的有___________(填字母)。
| A.提前除去【实验Ⅰ】溶解铁屑所用硝酸中的Fe3+杂质 |
| B.用浓硝酸溶液代替【实验Ⅳ】中所用的H2O2溶液 |
| C.整个实验中均采用相同浓度的KSCN溶液 |
| D.对每一份溶液平行测定多次吸光度A,取平均值作结果 |
智能手机因其集成的高清摄像头和智能传感器而常被应用于化学实验。某实验小组利用实验室中的废铁屑(久置但未生锈)制备硝酸铁,并利用配制的硝酸铁标准溶液对“硫酸亚铁补铁剂”中铁元素的含量进行测定。实验过程如下:
实验Ⅰ: 的制备
的制备
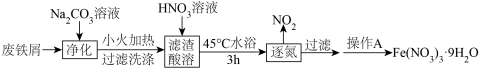
(1)请结合方程式解释在净化过程中加入 溶液并小火加热的目的是:
溶液并小火加热的目的是:___________ 。
(2)逐氮过程中使用氢氧化钠溶液吸收 ,写出该反应的化学方程式:
,写出该反应的化学方程式:___________ 。
(3)操作A包含的实验步骤有:___________ 、___________ 、过滤、洗涤、干燥。
实验Ⅱ:标准硝酸铁溶液的配制
准确称取 的
的 按如图步骤配成
按如图步骤配成 溶液。
溶液。
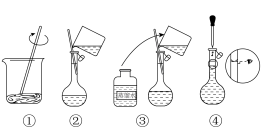
(4)智能手机连接热成像配件FLIROnePro可即时测定过程①中溶液温度。若将如图溶解所得溶液立即转移至容量瓶中并进行定容,则上述操作会导致配得溶液浓度___________ (填“偏高”、“偏低”或“无影响”)。
实验Ⅲ:绘制标准 溶液与灰度值的标准曲线
溶液与灰度值的标准曲线
①分别向7个 容量瓶中加入0、0.5、1.0、2.0、3.0、4.0、
容量瓶中加入0、0.5、1.0、2.0、3.0、4.0、 实验Ⅱ中标定的浓度为
实验Ⅱ中标定的浓度为 的
的 标准溶液,然后分别加入
标准溶液,然后分别加入 某浓度
某浓度 溶液,用蒸馏水定容。
溶液,用蒸馏水定容。
②将配好的溶液加入到 比色皿中,如图进行放置,在相同条件下用智能手机进行拍照,后用软件确定照片中各溶液相同位置的灰度数值,所得数据如下表所示:
比色皿中,如图进行放置,在相同条件下用智能手机进行拍照,后用软件确定照片中各溶液相同位置的灰度数值,所得数据如下表所示:
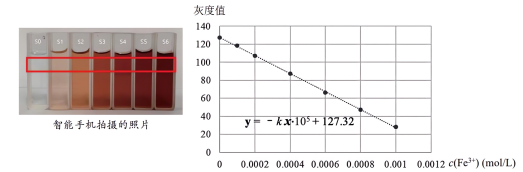
(5)上述实验数据处理中
___________ (保留1位有效数字)。
实验Ⅳ:“硫酸亚铁补铁剂”中铁元素含量的测定
①取补铁剂样品2.0g,加入 蒸馏水完全溶解,再加入足量
蒸馏水完全溶解,再加入足量 溶液,充分反应后配成
溶液,充分反应后配成 溶液。
溶液。
②取1.0mL①中所配溶液于 容量瓶中,加入1.5mL某浓度
容量瓶中,加入1.5mL某浓度 溶液,用蒸馏水定容。
溶液,用蒸馏水定容。
将最终配好的溶液加入到 比色皿中,在与实验Ⅲ步骤②中相同条件下拍照,软件处理获得溶液图片的灰度值为97.32。
比色皿中,在与实验Ⅲ步骤②中相同条件下拍照,软件处理获得溶液图片的灰度值为97.32。
(6)“硫酸亚铁补铁剂”中铁元素的质量分数为___________ %(保留2位有效数字)。
(7)下列操作中有利于更准确测得“硫酸亚铁补铁剂”中的铁元素含量的有___________。
实验Ⅰ:

(1)请结合方程式解释在净化过程中加入
(2)逐氮过程中使用氢氧化钠溶液吸收
(3)操作A包含的实验步骤有:
实验Ⅱ:标准硝酸铁溶液的配制
准确称取

(4)智能手机连接热成像配件FLIROnePro可即时测定过程①中溶液温度。若将如图溶解所得溶液立即转移至容量瓶中并进行定容,则上述操作会导致配得溶液浓度

实验Ⅲ:绘制标准
①分别向7个
②将配好的溶液加入到
| 比色管编号 | S0 | S1 | S2 | S3 | S4 | S5 | S6 |
| 0 | 0.5 | 1.0 | 2.0 | 3.0 | 4.0 | 5.0 | |
| 0 | 0.0001 | 0.0002 | 0.0004 | 0.0006 | 0.0008 | 0.001 | |
| 灰度值 | 127.3 | 119.4 | 107.1 | 87.3 | 65.3 | 47.2 | 29.2 |

(5)上述实验数据处理中
实验Ⅳ:“硫酸亚铁补铁剂”中铁元素含量的测定
①取补铁剂样品2.0g,加入
②取1.0mL①中所配溶液于
将最终配好的溶液加入到
(6)“硫酸亚铁补铁剂”中铁元素的质量分数为
(7)下列操作中有利于更准确测得“硫酸亚铁补铁剂”中的铁元素含量的有___________。
| A.提前除去实验Ⅰ溶解铁屑所用硝酸中的 |
| B.用浓硝酸溶液代替实验Ⅳ中所用的 |
| C.整个实验中所用的 |
| D.将配制的样品溶液和7个标准溶液放在一起在相同条件下同时拍照,再统一进行数据处理 |
实验室常利用甲醛法测定(NH4)2SO4样品中氮的质量分数,其反应原理为:4NH +6HCHO=3H++6H2O+(CH2)6N4H+[滴定时,1mol(CH2)6N4H+与1molH+相当],然后用NaOH标准溶液滴定反应生成的酸。某兴趣小组用甲醛法进行了如下实验:
+6HCHO=3H++6H2O+(CH2)6N4H+[滴定时,1mol(CH2)6N4H+与1molH+相当],然后用NaOH标准溶液滴定反应生成的酸。某兴趣小组用甲醛法进行了如下实验:
步骤Ⅰ:称取样品1.500g。
步骤Ⅱ:将样品溶解后,完全转移到250mL容量瓶中,定容,充分摇匀。
步骤Ⅲ:移取25.00mL样品溶液于250mL锥形瓶中,加入10mL20%的中性甲醛溶液,摇匀、静置5min后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点.按上述操作方法再重复2次。
(1)根据步骤Ⅲ填空:
①滴定时边滴边摇动锥形瓶,眼睛应观察___ 。
②达到滴定终点的标志是___ 。
③以下操作造成测得样品中氮的质量分数偏高的原因可能是___ 。
A.配制标准溶液的氢氧化钠中混有Na2CO3杂质
B.滴定终点读数时,俯视滴定管的刻度,其它操作均正确
C.盛装未知液的锥形瓶用蒸馏水洗过,水未倒尽
D.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
E.未用标准液润洗碱式滴定管
(2)滴定结果如下表所示:
若NaOH标准溶液的浓度为0.1010mol/L,则该样品中氮的质量分数为__ 。
步骤Ⅰ:称取样品1.500g。
步骤Ⅱ:将样品溶解后,完全转移到250mL容量瓶中,定容,充分摇匀。
步骤Ⅲ:移取25.00mL样品溶液于250mL锥形瓶中,加入10mL20%的中性甲醛溶液,摇匀、静置5min后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点.按上述操作方法再重复2次。
(1)根据步骤Ⅲ填空:
①滴定时边滴边摇动锥形瓶,眼睛应观察
②达到滴定终点的标志是
③以下操作造成测得样品中氮的质量分数偏高的原因可能是
A.配制标准溶液的氢氧化钠中混有Na2CO3杂质
B.滴定终点读数时,俯视滴定管的刻度,其它操作均正确
C.盛装未知液的锥形瓶用蒸馏水洗过,水未倒尽
D.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
E.未用标准液润洗碱式滴定管
(2)滴定结果如下表所示:
| 滴定次数 | 待测溶液的体积/mL | 标准溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
若NaOH标准溶液的浓度为0.1010mol/L,则该样品中氮的质量分数为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


