解答题-实验探究题 适中0.65 引用1 组卷336
近年来。研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。已知:SO2歧化反应的离子方程式:3SO2+2H2O=4H++2 +S↓
+S↓
(1)①I-可以作为水溶液中SO2歧化反应的催化剂,可能的歧化过程如下,将ii补充完整_______ 。
i.SO2+4I-+4H+=S↓+2I2+2H2O
ii.I2+2H2O+______=_______+_______+2I-
②请用碰操理论解释:作为该反应的催化剂加快反应速率的原因_______ 。加入催化剂该反应的反应热_______ (填变大、变小、不变)
(2)探究i,ii反应速率与SO2歧化反应速率的关系,实验如下:分别将18mLSO2饱和液加入到2mL下列试剂中,密闭放置观察现象(已知:I2易溶解在KI溶液中)
①B是A的对比实验,则a=_______ 。
②比较A、B、C,可得出的结论是_______ 。
③实验表明,SO2的歧化反应速率:D>A。结合i,ii反应速率解释原因:_______ 。
(1)①I-可以作为水溶液中SO2歧化反应的催化剂,可能的歧化过程如下,将ii补充完整
i.SO2+4I-+4H+=S↓+2I2+2H2O
ii.I2+2H2O+______=_______+_______+2I-
②请用碰操理论解释:作为该反应的催化剂加快反应速率的原因
(2)探究i,ii反应速率与SO2歧化反应速率的关系,实验如下:分别将18mLSO2饱和液加入到2mL下列试剂中,密闭放置观察现象(已知:I2易溶解在KI溶液中)
| 序号 | A | B | C | D |
| 试剂组成 | 0.4mol•L-1KI | amol•L-1KI 0.2mol•L-1H2SO4 | 0.2mol•L-1H2SO4 | 0.2mol•L-1KI 0.0002mol•L-1I2 |
| 实验现象 | 溶液变黄,一段时间后出现浑浊 | 溶液变黄,出现浑浊较A快 | 无明显现象 | 溶液由棕褐色很快褪色,出现浑浊较A快 |
②比较A、B、C,可得出的结论是
③实验表明,SO2的歧化反应速率:D>A。结合i,ii反应速率解释原因:
20-21高一下·辽宁沈阳·期中
类题推荐  歧化反应的方程式为
歧化反应的方程式为 ,
, 可以作为水溶液中
可以作为水溶液中 歧化反应的催化剂,可能的催化过程如下。将ii补充完整。
歧化反应的催化剂,可能的催化过程如下。将ii补充完整。
(1)i.
ii.
__________ =__________ +__________ 
(2)探究i、ii反应速率与 歧化反应速率的关系,实验如下:分别将18mL
歧化反应速率的关系,实验如下:分别将18mL 饱和溶液加入到2mL下列试剂中,密闭放置观察现象。(已知:
饱和溶液加入到2mL下列试剂中,密闭放置观察现象。(已知: 易溶解在KI溶液中)
易溶解在KI溶液中)
①B是A的对比实验,则
__________ 。
②比较A、B、C,可得出的结论是_________________________ 。
③实验表明, 的歧化反应速率
的歧化反应速率 。结合i、ii反应速率解释原因:
。结合i、ii反应速率解释原因:_____________________ 。
近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如下:

(1)反应Ⅰ:2H2SO4(l)=2SO2(g)+2H2O(g)+O2(g) ΔH1=+551 kJ·mol-1
反应Ⅲ:S(s)+O2(g)=SO2(g) ΔH3=-297 kJ·mol-1
反应Ⅱ的热化学方程式:________________ 。
(2)对反应Ⅱ,在某一投料比时,两种压强下,H2SO4在平衡体系中物质的量分数随温度的变化关系如图所示:
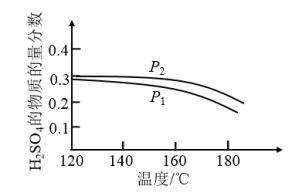
p2_______ p 1(填“>”或“<”)。
(3)I-可以作为水溶液中SO2歧化反应的催化剂,可能的催化过程如下。将ii补充完整。
i.SO2+4I-+4H+=S↓+2I2+2H2O
ii.I2+2H2O+_________ =_________ +_______ +2 I-
(4)探究i、ii反应速率与SO2歧化反应速率的关系,实验如下:分别将18 mL SO2饱和溶液加入到 2 mL下列试剂中,密闭放置观察现象。(已知:I2易溶解在KI溶液中)
①B是A的对比实验,则a=__________ 。
②比较A、B、C,可得出的结论是______________________ 。
③实验表明,SO2的歧化反应速率D>A,结合i、ii反应速率解释原因:________________ 。
(5)据文献报道,二氧化碳可以在酸性水溶液中用惰性电极电解制得乙烯,其原理如图所示。则b电极上的电极反应式为__________________ 。


(1)反应Ⅰ:2H2SO4(l)=2SO2(g)+2H2O(g)+O2(g) ΔH1=+551 kJ·mol-1
反应Ⅲ:S(s)+O2(g)=SO2(g) ΔH3=-297 kJ·mol-1
反应Ⅱ的热化学方程式:
(2)对反应Ⅱ,在某一投料比时,两种压强下,H2SO4在平衡体系中物质的量分数随温度的变化关系如图所示:

p2
(3)I-可以作为水溶液中SO2歧化反应的催化剂,可能的催化过程如下。将ii补充完整。
i.SO2+4I-+4H+=S↓+2I2+2H2O
ii.I2+2H2O+
(4)探究i、ii反应速率与SO2歧化反应速率的关系,实验如下:分别将18 mL SO2饱和溶液加入到 2 mL下列试剂中,密闭放置观察现象。(已知:I2易溶解在KI溶液中)
| 序号 | A | B | C | D |
| 试剂组成 | 0.4 mol·L-1 KI | a mol·L-1 KI0.2 mol·L-1 H2SO4 | 0.2 mol·L-1 H2SO4 | 0.2 mol·L-1 KI 0.0002 mol I2 |
| 实验现象 | 溶液变黄,一段时间后出现浑浊 | 溶液变黄,出现浑浊较A快 | 无明显现象 | 溶液由棕褐色很快褪色,变成黄色,出现浑浊较A快 |
①B是A的对比实验,则a=
②比较A、B、C,可得出的结论是
③实验表明,SO2的歧化反应速率D>A,结合i、ii反应速率解释原因:
(5)据文献报道,二氧化碳可以在酸性水溶液中用惰性电极电解制得乙烯,其原理如图所示。则b电极上的电极反应式为

近年来,研究人员提出用I—作为水溶液中SO2歧化反应的催化剂,实现含SO2工业污水的处理,其催化过程分两步完成:
i.SO2+4I—+4H+= S↓+2I2+2H2O
ii. I2+ 2H2O+SO2 = + 4H++ 2I—
+ 4H++ 2I—
为探究i、ii反应速率与 SO2歧化反应速率的关系,实验如下:分别将18mLSO2饱和溶液加入2mL下列试剂中,密闭放置,观察现象(已知:I2易溶解在KI溶液中)
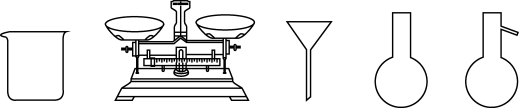
(1)KI的电子式为________ , 用KI固体配制50ml 0.4mol·L-1KI溶液,下图中的仪器需要使用到的有________ (填写名称)。
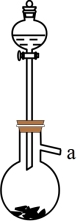
(2)实验室利用下图制备SO2气体的化学方程式为_______ 。
(3)水溶液中SO2歧化反应的离子方程式为________ 。
(4)实验①和②是对照实验,则a=_______ ,比较实验①和②可得出结论_______ 。
(5)实验③试剂X为________ 。比较实验②和③可知H+单独存在时不能催化SO2的歧化反应。
(6)实验表明,SO2歧化反应速率④>①,结合i和ii的反应速率,解释反应速率④>①的原因__________ 。
i.SO2+4I—+4H+= S↓+2I2+2H2O
ii. I2+ 2H2O+SO2 =
为探究i、ii反应速率与 SO2歧化反应速率的关系,实验如下:分别将18mLSO2饱和溶液加入2mL下列试剂中,密闭放置,观察现象(已知:I2易溶解在KI溶液中)
| 序号 | ① | ② | ③ | ④ |
| 试剂组成 | 0.4 mol·L-1 KI | a mol·L-1KI 0.2 mol·L-1 H2SO4 | x | 0.2 mol·L-1KI 0.002 mol·L-1 I2 |
| 实验现象 | 溶液变黄,一段时间后出现浑浊 | 溶液变黄,出现浑浊比①快 | 无明显现象 | 棕褐色溶液迅速褪色,变成黄色,出现浑浊比①快 |

(2)实验室利用下图制备SO2气体的化学方程式为

(3)水溶液中SO2歧化反应的离子方程式为
(4)实验①和②是对照实验,则a=
(5)实验③试剂X为
(6)实验表明,SO2歧化反应速率④>①,结合i和ii的反应速率,解释反应速率④>①的原因
(1)i.
ii.
(2)探究i、ii反应速率与
| 序号 | A | B | C | D |
| 试剂组成 | ||||
| 实验现象 | 溶液变黄,一段时间后出现浑浊 | 溶液变黄,出现浑浊较A快 | 无明显现象 | 溶液由棕褐色很快褪色,变成黄色,出现浑浊较A快 |
①B是A的对比实验,则
②比较A、B、C,可得出的结论是
③实验表明,
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


