解答题-实验探究题 适中0.65 引用1 组卷52
用氧化还原滴定法测定TiO2的质量分数:一定条件下,将TiO2溶解并还原为Ti3+,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。
(1)滴定Ti3+时可选用___________ 作指示剂,滴定过程中发生反应的离子方程式为___________ ,
(2)达到滴定终点的现象是___________ 。
(3)滴定前,有关滴定管的正确操作为(选出正确操作并按序排列)___________ 。
检漏→蒸馏水洗涤→( )→( )→( )→( )→( )→开始滴定。
A烘干
B.装入滴定液至零刻度以上
C.调整滴定液液面至零刻度或零刻度以下
D.用洗耳球吹出润洗液
E.排除气泡
F.用滴定液润洗2至3次
G.记录起始读数
(4)TiCl4两步反应可制得TiO2,第一步水解反应生成TiO2•xH2O,第一步水解反应的方程式为___________ 。
(1)滴定Ti3+时可选用
(2)达到滴定终点的现象是
(3)滴定前,有关滴定管的正确操作为(选出正确操作并按序排列)
检漏→蒸馏水洗涤→( )→( )→( )→( )→( )→开始滴定。
A烘干
B.装入滴定液至零刻度以上
C.调整滴定液液面至零刻度或零刻度以下
D.用洗耳球吹出润洗液
E.排除气泡
F.用滴定液润洗2至3次
G.记录起始读数
(4)TiCl4两步反应可制得TiO2,第一步水解反应生成TiO2•xH2O,第一步水解反应的方程式为
22-23高二上·浙江杭州·期中
类题推荐
绿矾 是一种重要的化工原料。为检测某部分被氧化的绿矾中亚铁离子的质量分数设计如下实验。
是一种重要的化工原料。为检测某部分被氧化的绿矾中亚铁离子的质量分数设计如下实验。
步骤一:精确称量部分被氧化的绿矾 ,加入适量硫酸溶解并配制成
,加入适量硫酸溶解并配制成 溶液。
溶液。
步骤二:取所配溶液 于锥形瓶中,用
于锥形瓶中,用 溶液滴定至终点。
溶液滴定至终点。
步骤三:重复步骤二2~3次,平均消耗 溶液的体积为
溶液的体积为 。
。
(1)步骤一中需要用到下列仪器中的_______(填选项字母)。
(2)步骤二中 溶液应用
溶液应用_______ (填“酸式”或“碱式”)滴定管盛装。滴定时发生反应的离子方程式为_______ 。
(3)滴定前,有关滴定管的正确操作为(选出正确操作并按序排列):检漏→蒸馏水洗涤→_____ →开始滴定。
A.装入 溶液至零刻度以上
溶液至零刻度以上
B.用 溶液润洗2至3次
溶液润洗2至3次
C.排除气泡
D.记录起始读数
E.调整液面至零刻度或零刻度以下
(4)步骤二中滴定至终点时的实验现象为_______ 。
(5)被氧化的绿矾中亚铁离子的质量分数为_______ ;若滴定终点时仰视读数,则测得亚铁离子的质量分数_______ (填“偏低”“偏高”或“不变”)。
步骤一:精确称量部分被氧化的绿矾
步骤二:取所配溶液
步骤三:重复步骤二2~3次,平均消耗
(1)步骤一中需要用到下列仪器中的_______(填选项字母)。
A. | B.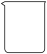 | C. | D.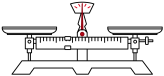 |
(3)滴定前,有关滴定管的正确操作为(选出正确操作并按序排列):检漏→蒸馏水洗涤→
A.装入
B.用
C.排除气泡
D.记录起始读数
E.调整液面至零刻度或零刻度以下
(4)步骤二中滴定至终点时的实验现象为
(5)被氧化的绿矾中亚铁离子的质量分数为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


