单选题 适中0.65 引用1 组卷184
在铜锌原电池中,锌板不纯时,少量氢气可以从锌板表面析出。解决方法是用棉花蘸取汞盐后擦拭锌板,在锌的表面形成锌汞齐(锌汞合金)。表面形成锌汞合金的锌板,单独浸泡在稀硫酸中,不再析出氢气,下列说法错误的是
| A.形成原电池后一定会加快氧化还原反应的速率 |
| B.锌板不纯时,析出少量氢气的原因是在锌电极上形成了原电池 |
| C.反应时,电子从Zn电极通过外电路向Cu电极转移 |
| D.负极的电极反应方程式: Zn-2e-=Zn2+ |
22-23高二上·浙江杭州·期中
类题推荐
H2S燃料电池示意图如图所示,其工作原理为2H2S(g)+O2(g)=S2(s)+2H2O(l) △H=-632kJ/mol。下列说法错误的是( )
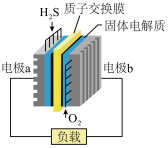

| A.电路中每通过4mol电子,电池会产生632kJ热量 |
| B.电池工作时,电子从电极a经导线流向电极b |
| C.电极a上发生的电极反应为2H2S-4e-=S2+4H+ |
| D.每32gO2参与反应,有4molH+经质子交换膜进入正极区 |
锌-空气电池(如图所示)是金属空气电池的一种,电解质溶液为KOH溶液。下列说法不正确的
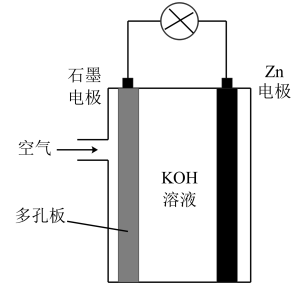

| A.工作时正极发生的反应是O2+4e-+2H2O=4OH- |
| B.正极区溶液的pH减小,负极区溶液的pH增大 |
| C.电池的总反应为 |
| D.电池工作时,电子流动方向:Zn电极→石墨电极 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


