解答题-实验探究题 适中0.65 引用1 组卷192
含氯消毒剂有多种,ClO2可用于自来水消毒,84消毒液用于家庭、宾馆的消毒。
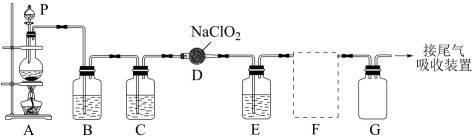
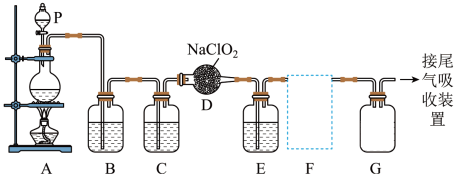
I.实验室可用亚氯酸钠固体与Cl2制备ClO2:2NaClO2Cl22ClO2 2NaCl,装置如图所示:
2NaCl,装置如图所示:
(已知:ClO2易溶于水,而微溶于CCl4,且密度大于空气;Cl2易溶于CCl4)
(1)A装置中发生反应的离子方程式为_______ 。为获得干燥且纯净的Cl2,B、C中盛装的液体依次是_______ 、_______ 。
(2)F中可用_______ 法收集ClO2。
(3)E装置的作用是_______ 。
II.84消毒液是生活中常见的一种消毒剂,常用于环境的消毒,其主要成分是NaClO。
(4)84消毒液使用时除了要按一定比例稀释,对消毒时间也有要求,一般在10~20分钟左右。结合有关知识解释原因:_______ 。
(5)次氯酸钠可以用于去除废水中的铵态氮,配平下列离子方程式,并标出电子转移情况 _______ 。
_______NH +_______ClO﹣=_______N2+_______Cl﹣+_______H2O+_______H+
+_______ClO﹣=_______N2+_______Cl﹣+_______H2O+_______H+
(6)下图是某同学模仿氯碱工业,在家中用电解食盐水法自制出与“84消毒液”相同成分(NaClO溶液)的消毒液。

该方法制备消毒液的总化学方程式为:_______ 。
(7)专家指出,将84消毒液与洁厕灵(主要成分HCl)一起合并使用,可能会导致使用者的呼吸道伤害。写出发生反应的化学方程式为:_______ 。
I.实验室可用亚氯酸钠固体与Cl2制备ClO2:2NaClO2Cl22ClO2

(已知:ClO2易溶于水,而微溶于CCl4,且密度大于空气;Cl2易溶于CCl4)
(1)A装置中发生反应的离子方程式为
(2)F中可用
(3)E装置的作用是
II.84消毒液是生活中常见的一种消毒剂,常用于环境的消毒,其主要成分是NaClO。
(4)84消毒液使用时除了要按一定比例稀释,对消毒时间也有要求,一般在10~20分钟左右。结合有关知识解释原因:
(5)次氯酸钠可以用于去除废水中的铵态氮,配平下列离子方程式,并
_______NH
(6)下图是某同学模仿氯碱工业,在家中用电解食盐水法自制出与“84消毒液”相同成分(NaClO溶液)的消毒液。

该方法制备消毒液的总化学方程式为:
(7)专家指出,将84消毒液与洁厕灵(主要成分HCl)一起合并使用,可能会导致使用者的呼吸道伤害。写出发生反应的化学方程式为:
22-23高一上·上海浦东新·期末
类题推荐
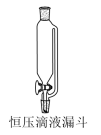
含氯消毒剂有多种,ClO2可用于自来水消毒,84消毒液用于家庭、宾馆的消毒。实验室可用亚氯酸钠固体与Cl2制备ClO2:2NaClO2 +Cl2 =2 ClO2 +2NaCl,装置如图所示:
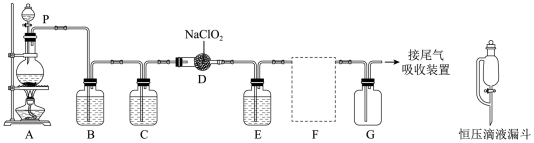
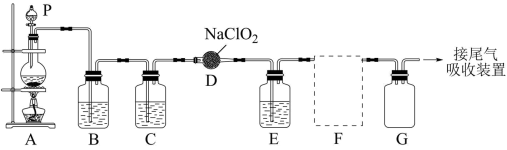
(1)有同学认为应将P换为恒压滴液漏斗,与仪器P对比,恒压滴液漏斗的优点是______ 。
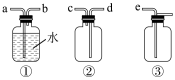
(2)B、C、E中盛装的液体依次是___________ (填编号) 。
(3)F处应选用的收集装置是___________ (填序号),其中与E装置导管相连的导管口是______ (填接口字母)
(4)一种有效成分为NaClO2、 NaHSO4、NaHCO3的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到ClO2溶液。上述过程中,生成ClO2的反应属于歧化反应,每生成lmol ClO2消耗NaClO2的量为______ mol;
(5)用于环境杀菌消毒的NaClO溶液须稀释并及时使用,若暴露在空气中时间过长且见光,将会导致消毒作用减弱,该过程的发生的化学方程式有___________ 和___________ 。 (已知: H2CO3:Ka1=4.5×10-7 Ka2=4.7 ×10-11,HClO: Ka =3.0 ×10-8)

(1)有同学认为应将P换为恒压滴液漏斗,与仪器P对比,恒压滴液漏斗的优点是
(2)B、C、E中盛装的液体依次是
| A.浓硫酸 | B.饱和食盐水 | C.NaOH溶液 | D.CCl4 |

(4)一种有效成分为NaClO2、 NaHSO4、NaHCO3的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到ClO2溶液。上述过程中,生成ClO2的反应属于歧化反应,每生成lmol ClO2消耗NaClO2的量为
(5)用于环境杀菌消毒的NaClO溶液须稀释并及时使用,若暴露在空气中时间过长且见光,将会导致消毒作用减弱,该过程的发生的化学方程式有
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网