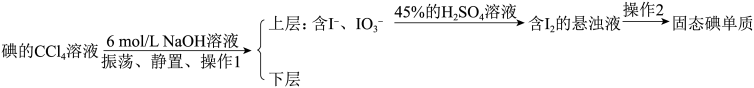解答题-工业流程题 适中0.65 引用2 组卷305
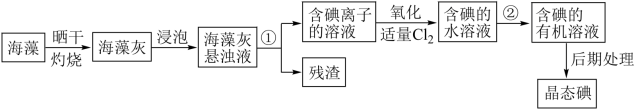
海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如图:
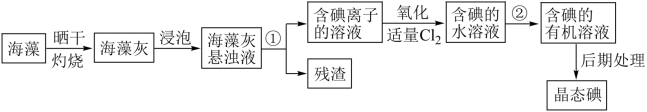
(1)灼烧海藻灰要在______ 中进行,其放在三角架上时还需要放上_____ 。
(2)写出氧化步骤中主要反应的离子方程式:_____ 。
(3)操作②步骤中可供选择的有关试剂是_____ ,该操作步骤叫_____ 。
A.酒精 B.四氯化碳 C.醋酸 D.甘油(易溶于水)
(4)实验室中取25mL该含碘离子的溶液,用0.1mol/L的FeCl3溶液测量其中I-的浓度,反应的离子方程式为:I-+Fe3+——I2+Fe2+(未配平),若消耗FeCl3溶液22.5mL,则含碘离子的溶液中I-的浓度为:_____ 。
(5)流程中后期处理用反萃取法
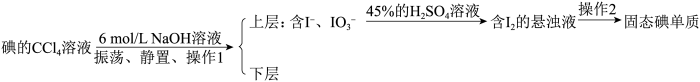
①碘单质与浓NaOH溶液发生的反应为:3I2+6NaOH=5NaI+NaIO3+3H2O,像这种将富集在四氯化碳中的碘单质利用化学转化法重新富集在水中的方法即为反萃取法。指出上述反应中氧化剂与还原剂的物质的量之比为_____ ,反萃取法比直接蒸馏法的优点有_____ 。
②写出I-、IO 与45%H2SO4溶液反应的离子方程式:
与45%H2SO4溶液反应的离子方程式:_____ 。

(1)灼烧海藻灰要在
(2)写出氧化步骤中主要反应的离子方程式:
(3)操作②步骤中可供选择的有关试剂是
A.酒精 B.四氯化碳 C.醋酸 D.甘油(易溶于水)
(4)实验室中取25mL该含碘离子的溶液,用0.1mol/L的FeCl3溶液测量其中I-的浓度,反应的离子方程式为:I-+Fe3+——I2+Fe2+(未配平),若消耗FeCl3溶液22.5mL,则含碘离子的溶液中I-的浓度为:
(5)流程中后期处理用反萃取法
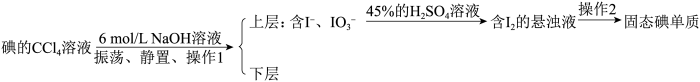
①碘单质与浓NaOH溶液发生的反应为:3I2+6NaOH=5NaI+NaIO3+3H2O,像这种将富集在四氯化碳中的碘单质利用化学转化法重新富集在水中的方法即为反萃取法。指出上述反应中氧化剂与还原剂的物质的量之比为
②写出I-、IO
22-23高一上·上海·期末
类题推荐
海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如下:

(1)指出提取碘的过程中有关的实验操作名称:①_______ ;②_______ ;若碘中混有食盐,最简单的方法分离是_______ 。
(2)提取碘的过程中,可供选择的有关试剂是_______。
(3)要测量含碘离子的溶液中I-的浓度,取25mL该溶液,先加几滴_______ ,再逐滴滴入0.1mol/LFeCl3溶液,当溶液颜色变为_______ 时I-被全部氧化:2I-+2Fe3+=I2+2Fe2+。
(4)①若实验室只有FeCl3固体,要配制500mL0.1mol/L的FeCl3溶液,所需仪器有:托盘天平、药匙、烧杯、玻璃棒、_______ 、胶头滴管。在配制过程中未洗涤烧杯和玻璃棒,则FeCl3溶液浓度会_______ ,(填“偏低”、“偏高”、“无影响”,下同):在定容时俯视刻度线和液面,则浓度会_______ 。
②若消耗FeCl3溶液22.5mL,则含碘离子的溶液中I-的浓度为:_______ 。
(5)碘单质与浓NaOH溶液发生的反应为:3I2+6NaOH=5NaI+NaIO3+3H2O,像这种将富集在四氯化碳中的碘单质利用化学转化法重新富集在水中的方法即为反萃取法。指出上述反应中氧化剂与还原剂的物质的量之比为_______ 。

(1)指出提取碘的过程中有关的实验操作名称:①
(2)提取碘的过程中,可供选择的有关试剂是_______。
| A.酒精 | B.四氯化碳 | C.醋酸 | D.甘油(易溶于水) |
(4)①若实验室只有FeCl3固体,要配制500mL0.1mol/L的FeCl3溶液,所需仪器有:托盘天平、药匙、烧杯、玻璃棒、
②若消耗FeCl3溶液22.5mL,则含碘离子的溶液中I-的浓度为:
(5)碘单质与浓NaOH溶液发生的反应为:3I2+6NaOH=5NaI+NaIO3+3H2O,像这种将富集在四氯化碳中的碘单质利用化学转化法重新富集在水中的方法即为反萃取法。指出上述反应中氧化剂与还原剂的物质的量之比为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网