解答题-实验探究题 适中0.65 引用3 组卷388
某小组通过实验探究氧化还原反应的规律。
已知:氧化还原反应电位传感器可以测量不同溶液的电位值,根据电位值大小可比较物质的氧化性/还原性强弱;数值越大,氧化性越强,数值越小,还原性越强。
测得几种物质的电位值如表所示。(注:实验中进行酸化时均用稀硫酸)
根据表中数据,回答下列问题:
(1)浓度均为0.1mol•L-1的下列三种溶液,氧化性由强到弱的顺序为_____ (填序号)。
①FeCl3 ②酸性KMnO4 ③酸性NaNO3
(2)影响物质氧化性强弱的因素有_____ 、_____ 。
(3)已知Fe3+与I-不能共存,由此推测下列一定不能大量共存的离子组是_____ 。
a.Fe3+、Br- b.Fe3+、S2- c.NO 、H+、I- d.H+、MnO
、H+、I- d.H+、MnO 、I-
、I-
(4)向等浓度的NaBr和KI混合溶液滴加少量酸性KMnO4溶液,发生反应的离子方程式为_____ 。(已知MnO 在酸性环境下的产物为Mn2+)
在酸性环境下的产物为Mn2+)
(5)往淀粉-KI溶液中逐滴加入氯水,观察到溶液先变蓝后褪色。小组同学就溶液褪色的原因,提出两种猜想,并设计如下实验进行验证。
猜想1:______。
猜想2:I2被氯水继续氧化
查阅资料:HClO不能漂白淀粉与I2结合形成的蓝色物质。
①猜想1为______ ,实验1所用试剂a为______ ,实验1的现象为______ 。
②实验3所用试剂b是一种可溶性含碘化合物,该反应的离子方程式为______ 。
已知:氧化还原反应电位传感器可以测量不同溶液的电位值,根据电位值大小可比较物质的氧化性/还原性强弱;数值越大,氧化性越强,数值越小,还原性越强。
测得几种物质的电位值如表所示。(注:实验中进行酸化时均用稀硫酸)
| 物质 | H2O2 | H2O2(酸化) | FeCl3 | KMnO4(酸化) | NaNO3(酸化) | NaBr | KI | Na2S |
| 浓度 | 5% | 5% | 0.1mol•L-1 | |||||
| 电位值/mV | 276 | 683 | 671 | 1130 | 603 | 362 | 116 | -361 |
(1)浓度均为0.1mol•L-1的下列三种溶液,氧化性由强到弱的顺序为
①FeCl3 ②酸性KMnO4 ③酸性NaNO3
(2)影响物质氧化性强弱的因素有
(3)已知Fe3+与I-不能共存,由此推测下列一定不能大量共存的离子组是
a.Fe3+、Br- b.Fe3+、S2- c.NO
(4)向等浓度的NaBr和KI混合溶液滴加少量酸性KMnO4溶液,发生反应的离子方程式为
(5)往淀粉-KI溶液中逐滴加入氯水,观察到溶液先变蓝后褪色。小组同学就溶液褪色的原因,提出两种猜想,并设计如下实验进行验证。
猜想1:______。
猜想2:I2被氯水继续氧化
查阅资料:HClO不能漂白淀粉与I2结合形成的蓝色物质。
| 序号 | 实验操作 | 试剂 | 现象 | 结论 |
| 1 | 分别取少量褪色的溶液于三支试管中,并加入对应试剂,观察实验现象 | a | ______ | 猜想1不正确 |
| 2 | 淀粉溶液 | 溶液不变蓝 | 猜想2正确(I2被氧化为IO | |
| 3 | b+稀H2SO4 | 溶液变蓝 |
②实验3所用试剂b是一种可溶性含碘化合物,该反应的离子方程式为
22-23高一上·广东佛山·期末
类题推荐
某小组通过实验探究氧化还原反应的规律。
已知:氧化还原反应电位传感器可以测量不同溶液的电位值,根据电位值大小可比较物质的氧化性/还原性强弱;数值越大,氧化性越强;数值越小,还原性越强。测得几种物质的电位值如表所示。(注:实验中进行酸化时均用稀硫酸)
根据表中数据,回答下列问题:
(1)浓度相同的下列三种溶液,氧化性由强到弱的顺序为_______ (填序号)。
① ②酸性
②酸性 ③酸性
③酸性
(2)已知 与
与 不能共存,由此推测下列能大量共存的离子组是
不能共存,由此推测下列能大量共存的离子组是_______ 。
a. b.
b. c.
c. d.
d.
(3)向等浓度的 和
和 混合溶液滴加少量酸性
混合溶液滴加少量酸性 溶液(对应还原产物为
溶液(对应还原产物为 ),发生反应的离子方程式为
),发生反应的离子方程式为_______ 。
(4)已知常温下 遇淀粉变蓝。现往淀粉
遇淀粉变蓝。现往淀粉 溶液中逐滴加入氯水(含
溶液中逐滴加入氯水(含 ),观察到溶液先变蓝后褪色。小组同学就溶液褪色的原因,提出两种猜想,并设计如下实验进行验证。猜想1:_______;猜想2:
),观察到溶液先变蓝后褪色。小组同学就溶液褪色的原因,提出两种猜想,并设计如下实验进行验证。猜想1:_______;猜想2: 被
被 继续氧化(为
继续氧化(为 )。
)。
①猜想1为_______ ,实验1所用试剂 为
为_______ 。
②试剂b是一种可溶性含碘化合物,该反应的离子方程式为_______ 。
(5)已知下列四种氧化剂(均可氧化 )对应的还原产物情况如下:
)对应的还原产物情况如下:
请判断,等数量的四种氧化剂微粒分别与足量 作用,得到
作用,得到 最多的是
最多的是_______ 。
(6)结合上述信息思考:对于 混合溶液,若控制性氧化
混合溶液,若控制性氧化 而不氧化
而不氧化 ,请提出两种合理的氧化方案:①加入
,请提出两种合理的氧化方案:①加入_______ ;②加入_______ 。
(7) 具有很强的氧化性(还原产物为
具有很强的氧化性(还原产物为 ),常被用作消毒剂,其消毒的效率(以单位质量得到的电子数表示)是
),常被用作消毒剂,其消毒的效率(以单位质量得到的电子数表示)是 的
的_______ 倍(保留两位有效数字)。
已知:氧化还原反应电位传感器可以测量不同溶液的电位值,根据电位值大小可比较物质的氧化性/还原性强弱;数值越大,氧化性越强;数值越小,还原性越强。测得几种物质的电位值如表所示。(注:实验中进行酸化时均用稀硫酸)
| 物质 | ||||||
| 浓度 | ||||||
| 电位值 | 171 | 1130 | 603 | 662 | 116 | |
(1)浓度相同的下列三种溶液,氧化性由强到弱的顺序为
①
(2)已知
a.
(3)向等浓度的
(4)已知常温下
| 序号 | 实验操作 | 试剂 | 观察实验现象 | 结论 |
| 1 | 分别取少量褪色后溶液于三支试管中,并加入对应试剂 | a | 溶液变蓝 | 猜想1不正确 |
| 2 | 淀粉溶液 | 溶液不变蓝 | 猜想2正确 | |
| 3 | 溶液变蓝 |
②试剂b是一种可溶性含碘化合物,该反应的离子方程式为
(5)已知下列四种氧化剂(均可氧化
| 氧化剂 | ||||
| 还原产物 |
(6)结合上述信息思考:对于
(7)
KI是中学化学常用的还原剂,某小组设计实验探究I-的性质。回答下列问题:
实验(一)探究影响氧化剂与KI反应的因素。
FeCl3、CuCl2、AgNO3溶液分别与KI反应,实验及现象如表所示:
已知:CuI为难容于水的白色固体。常温下,Ksp(AgI)=8. 5×10-17 ,Ksp(CuI)=1.2×10-12。
(1)实验②中的氧化产物为_______ (填化学式)。
(2)实验③中氧化剂与还原剂的物质的量之比为_______ 。
(3)已知:Ag+的氧化性比Fe3+的强,但氧化剂的氧化性强弱除受本身性质影响外,还与温度、浓度、溶液的酸碱度等外界条件有关。分析实验①③,试解释实验①中溶液没有变蓝的主要原因可能是_______ 。
实验(二)探究氯气与KI反应的产物。
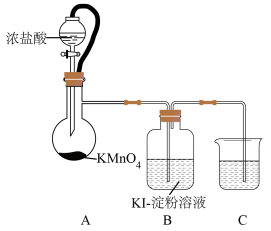
资料显示:I2和I-在溶液中会发生反应I2+I
 ,部分离子颜色如表所示。
,部分离子颜色如表所示。
(4)A中发生反应的化学方程式为_______ 。
(5)反应一段时间后,B中溶液颜色变为浅棕色,为了探究B溶液中的含碘物质,设计如下实验:
①操作I的目的是排除_______ (填离子符号)的干扰。
②写出 在水溶液中与Cl2反应生成
在水溶液中与Cl2反应生成 的离子方程式:
的离子方程式:_______ 。
③由以上实验可推断B中溶液颜色变成浅棕色的原因可能是生成了_______ (填离子符号),这两种离子混合后溶液呈浅棕色。
实验(一)探究影响氧化剂与KI反应的因素。
FeCl3、CuCl2、AgNO3溶液分别与KI反应,实验及现象如表所示:
| 实验操作 | 实验及现象 |
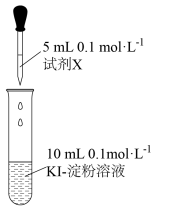 | ①X为AgNO3溶液,产生黄色沉淀,溶液不变蓝 |
| ②X为CuCl2溶液,过滤,得到蓝色溶液和白色沉淀 | |
| ③X为FeCl3溶液,溶液变蓝,没有沉淀产生;再滴加K3[Fe(CN)6 ]溶液,产生沉淀,过滤,沉淀为蓝色 |
(1)实验②中的氧化产物为
(2)实验③中氧化剂与还原剂的物质的量之比为
(3)已知:Ag+的氧化性比Fe3+的强,但氧化剂的氧化性强弱除受本身性质影响外,还与温度、浓度、溶液的酸碱度等外界条件有关。分析实验①③,试解释实验①中溶液没有变蓝的主要原因可能是
实验(二)探究氯气与KI反应的产物。

资料显示:I2和I-在溶液中会发生反应I2+I
| 离子 | ||||
| 颜色 | 棕黄色,遇淀粉变蓝 | 红色 | 黄色 | 无色 |
(5)反应一段时间后,B中溶液颜色变为浅棕色,为了探究B溶液中的含碘物质,设计如下实验:
| 实验操作 | 实验现象 |
| I.取反应后B中的溶液10mL,分成两等份,第一份滴入1滴碘水;第二份滴入1滴淀粉溶液 | 第一份溶液变蓝色;第二份溶液颜色没有变化 |
| II.将I2溶于KI溶液中配制得碘总浓度为0.1mol·L-1的溶液,取该溶液2mL,向其中滴加1滴淀粉溶液,再通入少量氯气 | 加淀粉后溶液变蓝,通氯气后蓝色褪去,溶液显浅棕色 |
| III.向II反应后的溶液中继续通入氯气 | 溶液几乎变为无色 |
②写出
③由以上实验可推断B中溶液颜色变成浅棕色的原因可能是生成了
某小组通过实验探究氧化还原反应的规律。
已知:氧化还原反应电位传感器可以测量不同溶液的电位值,根据电位值大小可比较物质的氧化性/还原性强弱;数值越大,氧化性越强;数值越小,还原性越强。测得几种物质的电位值如表所示。(注:实验中进行酸化时均用稀硫酸)
根据表中数据,回答下列问题:
(1)浓度相同的下列三种溶液,氧化性由强到弱的顺序为_________ (填序号)。
甲. 乙.酸性
乙.酸性 丙.酸性
丙.酸性
(2)结合上述信息思考:对于 、
、 混合溶液,若控制性氧化
混合溶液,若控制性氧化 而不氧化
而不氧化 ,请提出两种合理的氧化方案:①加入
,请提出两种合理的氧化方案:①加入_________ ;②加入_________ 。
(3)向等浓度的 和
和 混合溶液滴加少量酸性
混合溶液滴加少量酸性 溶液(对应还原产物为
溶液(对应还原产物为 ),发生反应的离子方程式为
),发生反应的离子方程式为_________ 。
(4)已知下列四种氧化剂(均可氧化 )对应的还原产物情况如下:
)对应的还原产物情况如下:
请判断,等物质的量的四种氧化剂分别与足量 作用,得到
作用,得到 最多的是
最多的是___________ 。
(5)造纸、印刷等工业废水中含有大量的硫化物(主要成分为 ),可用如图转化方式除去。
),可用如图转化方式除去。
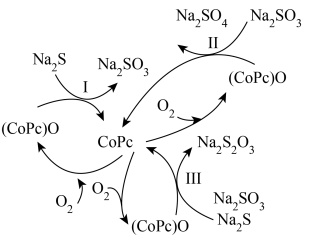
①反应Ⅰ和Ⅱ的转移电子数相等时,还原剂物质的量之比为___________ 。
②在废水处理整个过程中,催化剂为___________ ,氧化剂为___________ 。
③反应Ⅲ中 与
与 等物质的量反应,写出反应的化学方程式
等物质的量反应,写出反应的化学方程式_________________ 。
已知:氧化还原反应电位传感器可以测量不同溶液的电位值,根据电位值大小可比较物质的氧化性/还原性强弱;数值越大,氧化性越强;数值越小,还原性越强。测得几种物质的电位值如表所示。(注:实验中进行酸化时均用稀硫酸)
| 物质 | ||||||
| 浓度 | 0.10M(M为物质的量浓度的单位) | |||||
| 电位值 | 171 | 1130 | 603 | 662 | 116 | -361 |
(1)浓度相同的下列三种溶液,氧化性由强到弱的顺序为
甲.
(2)结合上述信息思考:对于
(3)向等浓度的
(4)已知下列四种氧化剂(均可氧化
| 氧化剂 | ||||
| 还原产物 |
(5)造纸、印刷等工业废水中含有大量的硫化物(主要成分为

①反应Ⅰ和Ⅱ的转移电子数相等时,还原剂物质的量之比为
②在废水处理整个过程中,催化剂为
③反应Ⅲ中
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


