解答题-实验探究题 较难0.4 引用1 组卷436
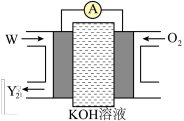
化合物( )可用于电讯器材、高级玻璃的制造。W、X、Y、Z为短周期元素,原子序数依次增加,且加和为21,
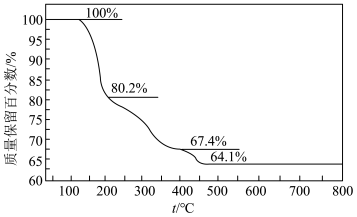
)可用于电讯器材、高级玻璃的制造。W、X、Y、Z为短周期元素,原子序数依次增加,且加和为21, 分子的总电子数为奇数,常温下为酸雨成因的一种气体。该化合物的热重曲线如图所示,在
分子的总电子数为奇数,常温下为酸雨成因的一种气体。该化合物的热重曲线如图所示,在 以下热分解时无刺激性气体逸出。
以下热分解时无刺激性气体逸出。
回答下列问题(使用相应的元素符号或化学式 ):
(1)元素Q比W元素核内质子数多18,基态Q原子中核外电子占据最高能层符号为_______ ,该能层最多能容纳_______ 个电子。
(2)W与Y形成的一种 分子,用电子式表示该物质的形成过程:
分子,用电子式表示该物质的形成过程:_______ ,该分子与 混合时能发生反应,生成两种环境友好的分子,因而成为火箭推进剂的原料,写出该反应化学方程式:
混合时能发生反应,生成两种环境友好的分子,因而成为火箭推进剂的原料,写出该反应化学方程式:_______ 。
(3)化合物 ( )中存在的主要化学键有
)中存在的主要化学键有_______ 。
a.氢键 b.极性共价键 c.范德华力 d.离子键
(4)X与Y的最高价氧化物的水化物酸性:_______>_______(填化学式)。______
(5)下列说法正确的是_______(填字母)。
(6)用化学方程式表示该化合物热分解的总反应_______ 。

回答下列问题(使用相应的
(1)元素Q比W元素核内质子数多18,基态Q原子中核外电子占据最高能层符号为
(2)W与Y形成的一种
(3)化合物 (
a.氢键 b.极性共价键 c.范德华力 d.离子键
(4)X与Y的最高价氧化物的水化物酸性:_______>_______(填化学式)。
(5)下列说法正确的是_______(填字母)。
| A.盛满 |
| B.YZ可用向上排空气法收集 |
| C.W、X、Y、Z的单质常温下均为固体 |
| D. |
22-23高二上·湖北武汉·期末
类题推荐
现有原子序数依次递增且都小于36的X、Y、Z、Q、W五种元素,其中X是原子半径最小的元素,Y原子在基态时其最外层电子数是其内层电子数的2倍,Q原子在基态时其2p原子轨道上有2个未成对电子,W元素的原子中3d能级上有4个未成对电子。回答下列问题:
(1)化合物ZX3的沸点比化合物YX4的高,其主要原因是_______ 。
(2)元素W能形成多种配合物,其中W(CO)5在常温下呈液态,熔点为-20.5 ℃,沸点为103 ℃,易溶于非极性溶剂,据此可判断W(CO)5晶体属于_______ (填晶体类型)晶体,该晶体中W的化合价为_______ 。
(3)下列说法正确的是_______(填字母)。
(4)Q和Na形成的一种只含有离子键的离子化合物的晶胞结构如图所示,与一个阴离子距离最近且相等的所有阳离子为顶点构成的几何体为_______ 。已知该晶胞的密度为ρg·cm-3,阿伏加德罗常数的值为NA,则晶胞边长为_______ cm。(用含ρ、NA的代数式表示)
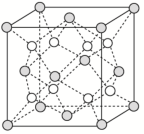
(1)化合物ZX3的沸点比化合物YX4的高,其主要原因是
(2)元素W能形成多种配合物,其中W(CO)5在常温下呈液态,熔点为-20.5 ℃,沸点为103 ℃,易溶于非极性溶剂,据此可判断W(CO)5晶体属于
(3)下列说法正确的是_______(填字母)。
| A.分子晶体中,共价键的键能越大,该分子晶体的熔、沸点越高 |
| B.电负性顺序:X<Y<Z<Q |
| C.因为CaO的晶格能比KCl的大,所以KCl比CaO的熔点低 |
| D.H2YO3的分子结构中含有一个非羟基氧,故其为中强酸 |

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网