填空题 适中0.65 引用1 组卷259
下图是短周期元素①~⑤在元素周期表中的位置。

(1)②在周期表中的位置是第___________ 周期第___________ 族,其与 反应的化学方程式是
反应的化学方程式是___________ 。
(2)③的一种核素的中子数是10,表示该核素的符号是___________ 。
(3)非金属性:④___________ ⑤(填“>”或“<”),从原子结构角度解释其原因:___________ 。
(4)②、⑤两种元素形成的化合物有重要的用途,用电子式表示它的形成过程___________ 。
(5)下列关于①的说法正确的是___________ 。
a、原子结构示意图为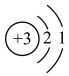
b、在同周期中,①最高价氧化物的水化物的碱性最强
c、在同主族的元素中,①的金属性最强

(1)②在周期表中的位置是第
(2)③的一种核素的中子数是10,表示该核素的符号是
(3)非金属性:④
(4)②、⑤两种元素形成的化合物有重要的用途,用电子式表示它的形成过程
(5)下列关于①的说法正确的是
a、原子结构示意图为

b、在同周期中,①最高价氧化物的水化物的碱性最强
c、在同主族的元素中,①的金属性最强
22-23高一上·北京通州·期末
类题推荐
如图是元素①~⑥在元素周期表中的位置。
(1)①的原子结构示意图是_______ ,②形成单质的电子式是_______ 。
(2)③在周期表中的位置是_______ 。①和③可以形成化合物,请用电子式表示该化合物形成的过程_______ 。
(3)③、④、⑤、⑥形成的简单离子中,半径最小的是_______ (填离子符号)。
(4)非金属性:②_______ ③(填“>”或“<”),从原子结构角度解释其原因_______ 。
(5)⑤最高价氧化物的水化物可以与⑥的单质反应,请写出反应的离子方程式_______ 。
(6)下列关于①的说法正确的是_______ 。
a.在同主族元素中,①最高价氧化物的水化物的碱性最强
b.①在空气中加热生成的产物是过氧化物
c.①可以与水反应生成氢气
(7)已知电负性的数值表示原子对电子吸引能力的相对大小。以下是几种原子的电负性数值:
x的范围是_______ 。请根据以上数据推测,在目前已知的118种元素中,电负性最大的元素为_______ (填元素符号)。
| ① | ② | ③ | ④ | ||||
| ⑤ | ⑥ | ||||||
(2)③在周期表中的位置是
(3)③、④、⑤、⑥形成的简单离子中,半径最小的是
(4)非金属性:②
(5)⑤最高价氧化物的水化物可以与⑥的单质反应,请写出反应的离子方程式
(6)下列关于①的说法正确的是
a.在同主族元素中,①最高价氧化物的水化物的碱性最强
b.①在空气中加热生成的产物是过氧化物
c.①可以与水反应生成氢气
(7)已知电负性的数值表示原子对电子吸引能力的相对大小。以下是几种原子的电负性数值:
| 元素 | 铝 | 硅 | 磷 | 硫 | 氯 |
| 电负性 | 1.5 | 1.8 | 2.1 | x | 3.0 |
下图是元素①~⑤在元素周期表中的位置。
(1)⑤在周期表中的位置是第_______ 周期第_______ 族,其最高价氧化物对应的水化物与②的最高价氧化物对应的水化物反应的离子方程式是_______ 。
(2)③的一种核素的中子数是9,表示该核素的符号是_______ 。
(3)非金属性:④_______ ⑤(填“>”或“<”),从原子结构角度解释其原因:_______ 。
(4)②、⑤两种元素形成的化合物有重要的用途,用电子式表示它的形成过程_______ 。
(5)下列关于①的说法正确的是_______ (填字母)。
a.原子结构示意图为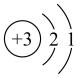
b.其单质可以和水反应生成
c.在同主族的元素中,①的金属性最强
(6)为研究②单质(X)的性质,进行如下实验:
下列说法中,正确的是_______(填字母)。
| ① | ③ | ④ | |||||
| ② | ⑤ | ||||||
(1)⑤在周期表中的位置是第
(2)③的一种核素的中子数是9,表示该核素的符号是
(3)非金属性:④
(4)②、⑤两种元素形成的化合物有重要的用途,用电子式表示它的形成过程
(5)下列关于①的说法正确的是
a.原子结构示意图为

b.其单质可以和水反应生成
c.在同主族的元素中,①的金属性最强
(6)为研究②单质(X)的性质,进行如下实验:
| 实验 | ||
| 装置 | 液体a | 现象 |
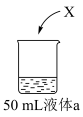 | 蒸馏水 | Ⅰ.X浮在液面上,剧烈反应,产生少量白雾 |
| Ⅱ.X浮在液面上,反应比Ⅰ中剧烈,产生白雾 | ||
| 浓盐酸 | Ⅲ.X浮在液面上,反应比Ⅰ中缓慢,产生大量白雾,烧杯底部有白色固体 | |
| A.Ⅰ中现象说明X与水反应放热 |
| B.Ⅱ中反应的离子方程式为 |
| C.Ⅲ中白雾比Ⅱ中多,说明Ⅲ中反应放热比Ⅱ中更多 |
| D.推测Ⅲ中反应缓慢可能与 |
如图是元素①~⑥在元素周期表中的位置。
(1)①的原子结构示意图是___________ 。
(2)③在周期表中的位置是___________ 。
(3)③、④、⑤、⑥形成的简单离子中,半径最小的是___________ (填离子符号)。
(4)非金属性:②___________ ③(填“>”或“<”),从原子结构角度解释其原因___________ 。
(5)⑤的最高价氧化物的水化物可以与⑥的单质反应,请写出反应的离子方程式___________ 。
(6)下列关于①的说法正确的是___________ 。
a.在同主族元素中,①最高价氧化物的水化物的碱性最强
b.①在空气中加热生成的产物是过氧化物
c.①可以与水反应生成氢气
(7)已知电负性的数值表示原子对电子吸引能力的相对大小。以下是几种原子的电负性数值:
x的范围是___________ 。请根据以上数据推测,在目前已知的118种元素中,电负性最大的元素为___________ (填元素符号)。
| ① | ② | ③ | ④ | ||||
| ⑤ | ⑥ | ||||||
(2)③在周期表中的位置是
(3)③、④、⑤、⑥形成的简单离子中,半径最小的是
(4)非金属性:②
(5)⑤的最高价氧化物的水化物可以与⑥的单质反应,请写出反应的离子方程式
(6)下列关于①的说法正确的是
a.在同主族元素中,①最高价氧化物的水化物的碱性最强
b.①在空气中加热生成的产物是过氧化物
c.①可以与水反应生成氢气
(7)已知电负性的数值表示原子对电子吸引能力的相对大小。以下是几种原子的电负性数值:
| 元素 | 铝 | 硅 | 磷 | 硫 | 氯 |
| 电负性 | 1.5 | 1.8 | 2.1 | x | 3.0 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


