解答题-实验探究题 适中0.65 引用1 组卷127
用BaS溶液和HCl为原料制备BaCl2·2H2O,并定量测定产品中BaCl2·2H2O的含量。
步骤Ⅰ:制备BaCl2·2H2O
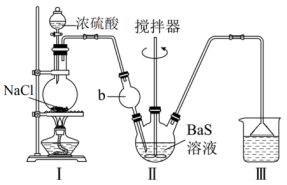
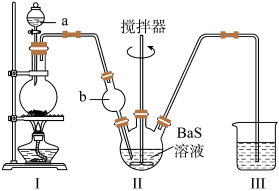
按图所示装置进行实验,得到BaCl2溶液,再经一系列步骤获得BaCl2·2H2O。
(1)盛装氯化钠的装置名称______ 。
(2)装置Ⅰ中发生化学反应的方程式______ 。
(3)装置b的作用是______ 。
(4)烧杯中盛放的溶液是______ ;用途是______ 。
步骤Ⅱ:产品中BaCl2·2H2O的含量测定
①称取BaCl2·2H2O产品0.5000g,用100mL水溶解,酸化,加热至近沸;
②在不断搅拌下,向①所得溶液中逐滴加入热的0.100mol•L-1H2SO4溶液;
③60℃水浴加热40min,待沉淀完全后,经过滤、洗涤、烘干等步骤,称量白色固体,质量为0.4660g。
回答下列问题:
(5)步骤②中发生反应的离子方程式_______ 。
(6)判断沉淀已完全的方法_______ 。
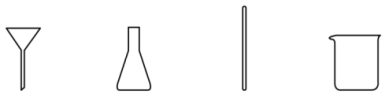
(7)在过滤操作中,下列玻璃仪器不需要用到的是______ (填名称)。
(8)产品中BaCl2·2H2O的质量为_____ g(保留三位有效数字)。
(9)若在洗涤过程中有部分沉淀被洗掉,则计算的产率比实际产率_____ (填“高、或低”)。
步骤Ⅰ:制备BaCl2·2H2O

按图所示装置进行实验,得到BaCl2溶液,再经一系列步骤获得BaCl2·2H2O。
(1)盛装氯化钠的装置名称
(2)装置Ⅰ中发生化学反应的方程式
(3)装置b的作用是
(4)烧杯中盛放的溶液是
步骤Ⅱ:产品中BaCl2·2H2O的含量测定
①称取BaCl2·2H2O产品0.5000g,用100mL水溶解,酸化,加热至近沸;
②在不断搅拌下,向①所得溶液中逐滴加入热的0.100mol•L-1H2SO4溶液;
③60℃水浴加热40min,待沉淀完全后,经过滤、洗涤、烘干等步骤,称量白色固体,质量为0.4660g。
回答下列问题:
(5)步骤②中发生反应的离子方程式
(6)判断沉淀已完全的方法
(7)在过滤操作中,下列玻璃仪器不需要用到的是

(8)产品中BaCl2·2H2O的质量为
(9)若在洗涤过程中有部分沉淀被洗掉,则计算的产率比实际产率
22-23高三上·天津河东·期末
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网